黑色素瘤通常具有较好的免疫原性,对于手术切除治疗和检查点阻断疗法均有反应;然而,这种肿瘤的复发问题仍然非常常见。为了更好地理解并最终防止肿瘤复发,Micevic和Daniels等人最近发现了一种主要是肿瘤特异性的L-7Rhi CD8+ T细胞群体,这种细胞在淋巴结中长期存在,并能对复发的黑色素瘤产生强烈的细胞毒性记忆反应。这种细胞状态经表观遗传调控,并且可以通过药物表观遗传调节来增强。这些结果最近发表在《PNAS》上。
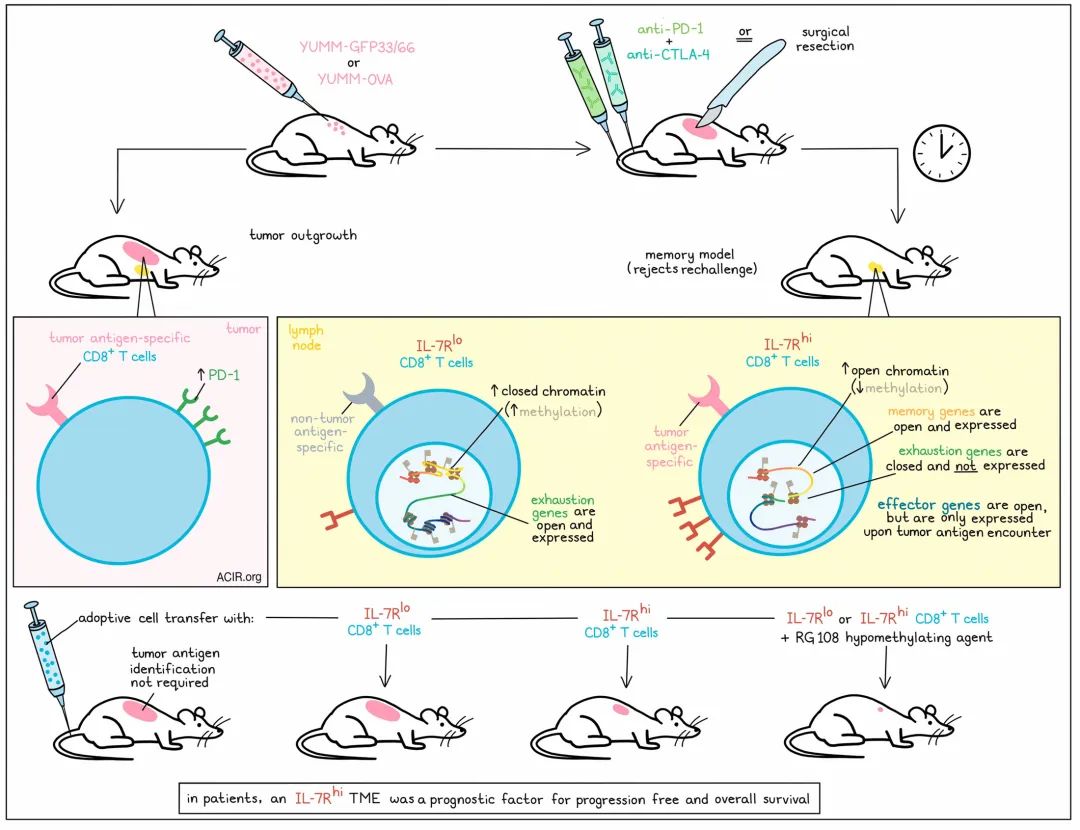
为了研究免疫记忆和黑色素瘤复发问题,Micevic和Daniels等人使用了表达LCMV gp33-41和gp66-77抗原及荧光标记(YUMM-GFP33/66)或OVA(YUMM-OVA)的YUMM1.77黑色素瘤模型。这些模型对手术切除或联合免疫检查点阻断疗法(抗PD-1和抗CTLA-4)有积极反应,形成了免疫记忆,以一种特定于肿瘤并依赖于T细胞的方式排斥肿瘤的再次发生。利用这个模型,研究人员在肿瘤引流淋巴结(tdLNs)和脾脏中检测到扩增的优势抗原特异性T细胞,这些细胞在肿瘤挑战后扩增,并在肿瘤切除后的6周内在tdLNs中按比例扩增。阻断淋巴细胞从淋巴结中流出会中止记忆反应。来自淋巴器官的CD8+ T细胞的批量RNA测序揭示了记忆样的转录谱特征,包括IL7r的高表达。(”tumor challenge”通俗地理解即指的是对肿瘤进行的一种挑战性测试或实验。在肿瘤研究中,科学家们经常使用不同方法或药物来刺激或引发肿瘤的生长或复发,从而评估治疗手段的有效性或研究肿瘤的特性。这个过程可以帮助我们了解肿瘤对治疗的反应以及发展新的治疗策略。)
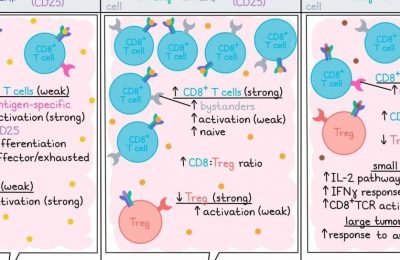
鉴于IL-7R标记了几种细胞状态,并且对T细胞的发育、存活和记忆分化至关重要,研究人员进一步调查了其在记忆模型中tdLN群体中的表达情况。尽管来自肿瘤进展中小鼠的肿瘤特异性CD8+ TILs细胞显示出PD-1的表达增加,但在记忆模型小鼠的淋巴结中,超过90%的肿瘤特异性T细胞具有高表达的IL-7R标记。相比之下,在这个模型中,只有3%的非肿瘤特异性CD8+ T细胞表达IL-7R,这表明IL-7R可以作为记忆环境中肿瘤特异性T细胞的标记。在初始肿瘤挑战期间而不是在再次挑战期间去阻断IL-7R,会降低功能性记忆反应和生存率,这表明IL-7R在免疫记忆的建立中起着关键作用。
接下来,研究人员使用单细胞RNA测序和聚类分析进一步表征具有高IL-7R表达的CD8+ T细胞群。该细胞群表现出中央记忆和细胞毒性样的T细胞表型特征,并表达Ccr7、Sell、Cd27、Cd28、Tcf7、Eomes和Bcl-2。它还具有最高的整体细胞毒性评分(与NK细胞簇一起),并表达多种内在的细胞毒性介质,包括Nkg7。有趣的是,与CD8+ T细胞效应子标志物有关的基因(如Gzmb、Prf1和Ifng)在IL-7Rhi CD8+ T细胞群中并没有高度表达。
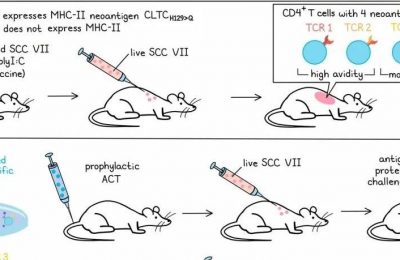
由于IL-7R高表达与肿瘤抗原特异性之间的强烈重叠性,研究人员将IL-7Rhi细胞作为细胞转移治疗(ACT)的候选细胞进行评估。与阴性对照组相比,IL-7Rlo细胞的转移效果相似,而IL-7Rhi细胞(从具有免疫记忆的小鼠的淋巴结中分离出来)的转移则可使肿瘤生长减缓并延长生存时间达50%,并在一部分小鼠中实现治愈效果。重要的是,这种方法不需要鉴定任何特定的肿瘤抗原。
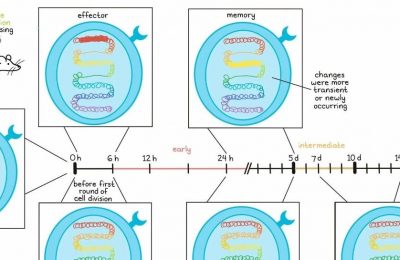
从表观遗传学的角度来看,研究人员观察到在IL-7Rhi细胞中,与IL-7Rlo细胞相比,Tcf7启动子上的DNA甲基化显著降低,这与甲基化会抑制基因表达的原理一致。此外,与与记忆形成相关的基因Il7r和Tcf7以及其他相关位点相比,染色质在转录起始位点附近更为开放,而在与细胞衰竭相关的基因附近更为关闭。有趣的是,研究人员还观察到,尽管在记忆状态下这些细胞并未主动表达细胞毒性分子,但染色质在与细胞毒性和产生多种分子(如IFNγ、IL-2、TNFɑ、粒酶A、粒酶B和穿孔素)有关的基因附近仍然保持开放。而当这些细胞群体重新受到挑战时,这些细胞毒性分子被发现上调表达,这表明IL-7Rhi细胞在表观遗传上具有对肿瘤再次挑战的准备性。
通过体外使用低甲基化剂RG108处理TILs,可以增加它们对Tcf7和Il7r的表达。为了探究这是否能增强细胞转移治疗(ACT),研究人员在体外使用RG108处理IL-7Rhi或IL-7Rlo CD8+ T细胞群体,然后将它们转移至未经免疫的小鼠体内。随后,小鼠被YUMMER1.7(一种高抗原负载的YUMM1.7肿瘤细胞变体,但没有主要抗原[CMV或OVA])挑战。与未处理的IL-7Rhi细胞相比,接种RG108处理后的IL-7Rhi细胞能够提供更强的保护免疫力,延长小鼠的中位生存时间,并使75%的小鼠实现肿瘤清除。此外,经过RG108处理的IL-7Rlo细胞也能够提供增强的抗肿瘤免疫力,消除了之前观察到的IL-7Rhi和IL-7Rlo细胞群体之间的差异。
为了研究这些发现的转化意义,Micevic和Daniels等人在大规模的黑色素瘤患者队列中分析了TME中的IL-7R表达。与小鼠相似,人类IL-7Rhi CD8+ T细胞表现出Tcf7启动子的低甲基化,与IL-7Rlo组相比,对应着更高的TCF7表达。人类IL-7Rhi CD8+ T细胞也表达了在小鼠模型中观察到的类似记忆性的甲基化标记。
为了确定IL-7R表达是否与持久的治疗反应和生存相关,研究人员将一大批晚期黑色素瘤患者分为IL-7Rhi和IL-7Rlo组。与IL-7Rlo组相比,IL-7Rhi队列富集了与T细胞信号传导和免疫应答相关的基因表达,并显示出延长的无进展生存期(755天 vs. 523天)和总生存期(2,421天 vs. 875天)。这种相关性不能归因于其他预后因素,并且确定IL-7R表达是总体生存期的独立预后因素。有趣的是,TCF7与生存期无相关性,这表明IL-7R表达不仅仅是增加干细胞特性的体现。在大规模的肺癌患者队列和60例接受检查点抑制剂治疗的黑色素瘤患者队列中也观察到类似的结果。
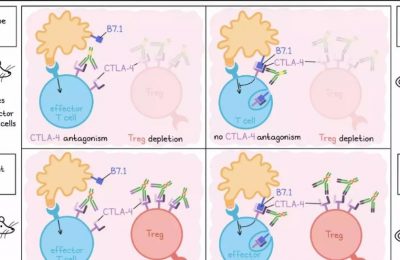
为了了解IL-7R如何影响对抗CTLA-4和PD-1的治疗反应,研究人员对携带肿瘤的小鼠进行了双重检查点阻断治疗。尽管同时阻断IL-7R和接受免疫治疗不会影响抗PD-1和抗CTLA-4诱导的缓解,但它确实导致肿瘤复发增加,这表明IL-7R信号在维持持久性抗肿瘤免疫中起着关键作用。
总的来说,Micevic和Daniels等人的研究结果表明高IL-7R表达是表观遗传调控的,并在限制肿瘤复发中发挥重要作用。IL-7Rhi CD8+ T细胞群体在淋巴结中长期存在,在那里它们保持准备状态,随时准备应对任何重新出现的肿瘤细胞。此外,IL-7Rhi CD8+ T细胞在临床上具有广泛应用前景,因为它们主要针对肿瘤,可以通过低甲基化剂增强,并且可以在不需要鉴定特定肿瘤抗原的情况下实现有效的细胞转移治疗。
作者面对面
本周,共同第一作者Andrew Daniels和Goran Micevic回答了我们的问题。

共同第一作者Goran Micevic(左)和Andrew Daniels(右)
对你们来说,这项研究最令人惊讶的发现是什么?
AD:对我们来说,最令人惊讶的发现之一是使用低甲基化剂对T细胞进行预处理,可以显著提高它们的抗肿瘤功能。低甲基化剂不仅能够增强T细胞在转移至未经免疫的小鼠之前表达功能标志物的效力,而且在完全不表达这些标志物的大量T细胞中也能够产生几乎相同的疗效。
GM:阻断IL-7R以消除强有力的功能性记忆表型的能力也是令人震惊的。
研究意义如何?
AD:这些发现为临床创新提供了一个令人兴奋的领域。近年来,我们对在肿瘤环境中发生的T细胞大量再编程的一些表观遗传机制有了更好的理解。我们认为,细胞转移疗法是可以从这些创新中获益的关键治疗方式之一。
GM:进一步的研究将需要确定关键的表观遗传驱动因素和最佳的靶向方法。关于成功的抗肿瘤记忆反应的解析仍然存在重要问题,包括时间表、信号、细胞间相互作用以及发生这些反应的区域。
在工作之外,你最近了解到的最酷的事情是什么?
AD:对我来说,最近一直在关注采集蘑菇!你可以采集到许多无法栽培的美味品种,因为它们与树木之间形成了复杂的关系以获取养分。这使得采集成为一个非常酷的机会!
GM:我最近了解到,海洋硅藻,也就是单细胞藻类,产生了我们使用的大部分氧气!就像T细胞一样,它们虽小却强大。这个描述也适用于我的三岁孩子,并提醒我珍惜生活中那些令人惊奇的“小事物”。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏