杂志名称:Cell Metab.
发表日期:2024.02.08
DOI:10.1016/j.cmet.2024.01.012.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38350448/
影响因子:29.0
内容简介
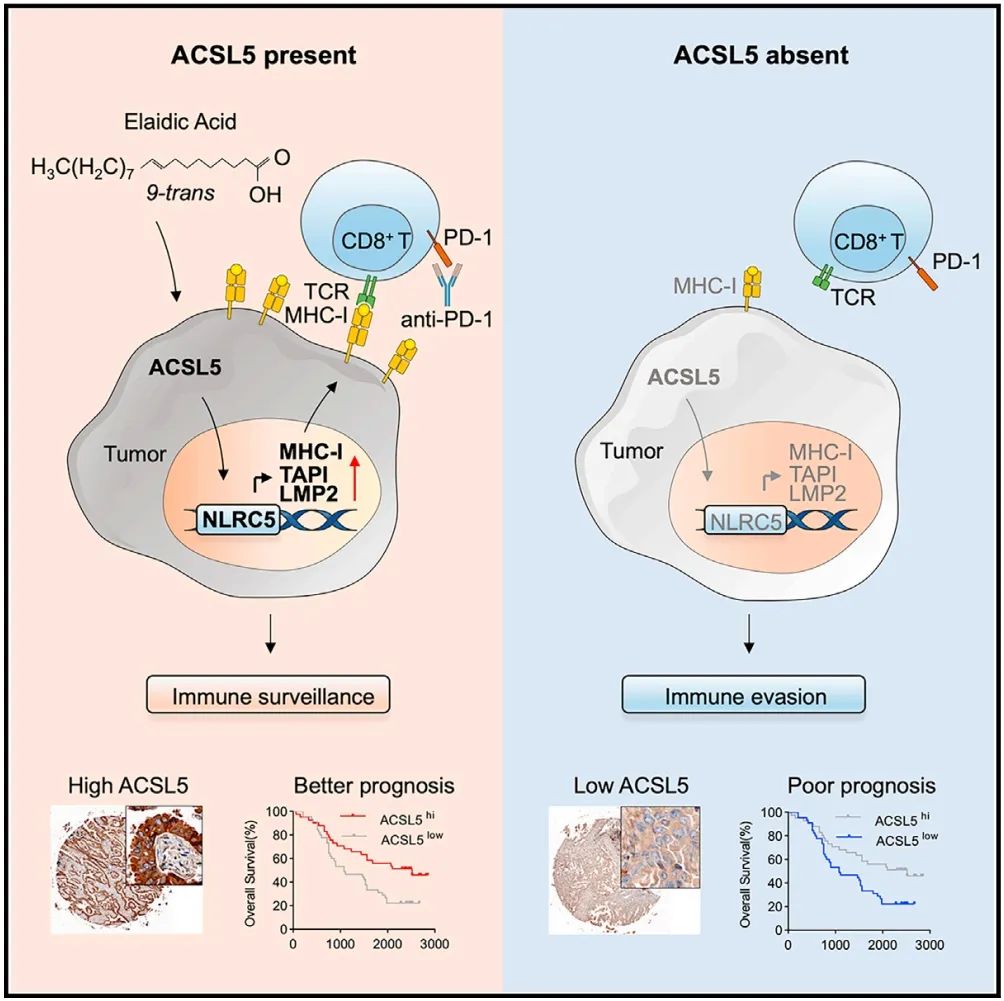
长链脂肪酸(LCFAs)及其激活酶,酰辅酶A(CoA)合成酶长链家族(ACSL)在肿瘤微环境中的免疫调节作用仍然不甚明了。我们发现,ACSL5作为一种依赖免疫的肿瘤抑制因子发挥作用。ACSL5表达使肿瘤对PD-1阻断疗法在体内敏感,并通过调节主要组织相容性复合体I类(MHC-I)介导的抗原呈递,在体外增强CD8+ T细胞介导的细胞毒性。通过筛选ACSL5的潜在底物,我们进一步确定了长期被认为对人体健康有害的反式长链脂肪酸——反式油酸(EA)——可以增强MHC-I表达。补充EA可以抑制肿瘤生长并增强PD-1阻断疗法的敏感性。在临床上,ACSL5表达与肺癌患者的生存率正相关,血浆EA水平也可以预测免疫治疗的效率。我们的发现为通过针对ACSL5或通过饮食补充EA来进行代谢重编程,从而增强免疫疗法提供了基础。
创新性及研究意义
这篇文章的核心创新性在于揭示了长链脂肪酸(LCFAs)及其激活酶ACSL5在肿瘤微环境中的免疫调节作用,特别是ACSL5在调节肿瘤抗原呈递中的关键作用。研究发现,ACSL5不仅是一个依赖免疫的肿瘤抑制因子,而且其表达能够增强PD-1阻断疗法的效果,并在体外增强CD8+ T细胞介导的细胞毒性。
研究的另一个创新点是识别出长期被认为对人体有害的反式油酸(EA)实际上能通过ACSL5增强MHC-I的表达,从而有助于抑制肿瘤生长并提高PD-1阻断疗法的敏感性。这一发现颠覆了对反式油酸的传统看法,并指出通过饮食补充EA可能是一种新的肿瘤治疗策略。
研究的意义在于为肿瘤免疫治疗提供了新的角度和方法。通过瞄准ACSL5或通过饮食补充EA来进行代谢重编程,有可能增强免疫疗法的效果。此外,研究还表明ACSL5表达和血浆EA水平可作为肺癌患者预后的生物标志物,为临床治疗提供了新的参考依据。这些发现为开发新的抗肿瘤策略提供了科学依据,具有重要的研究意义和临床应用前景。
数据图
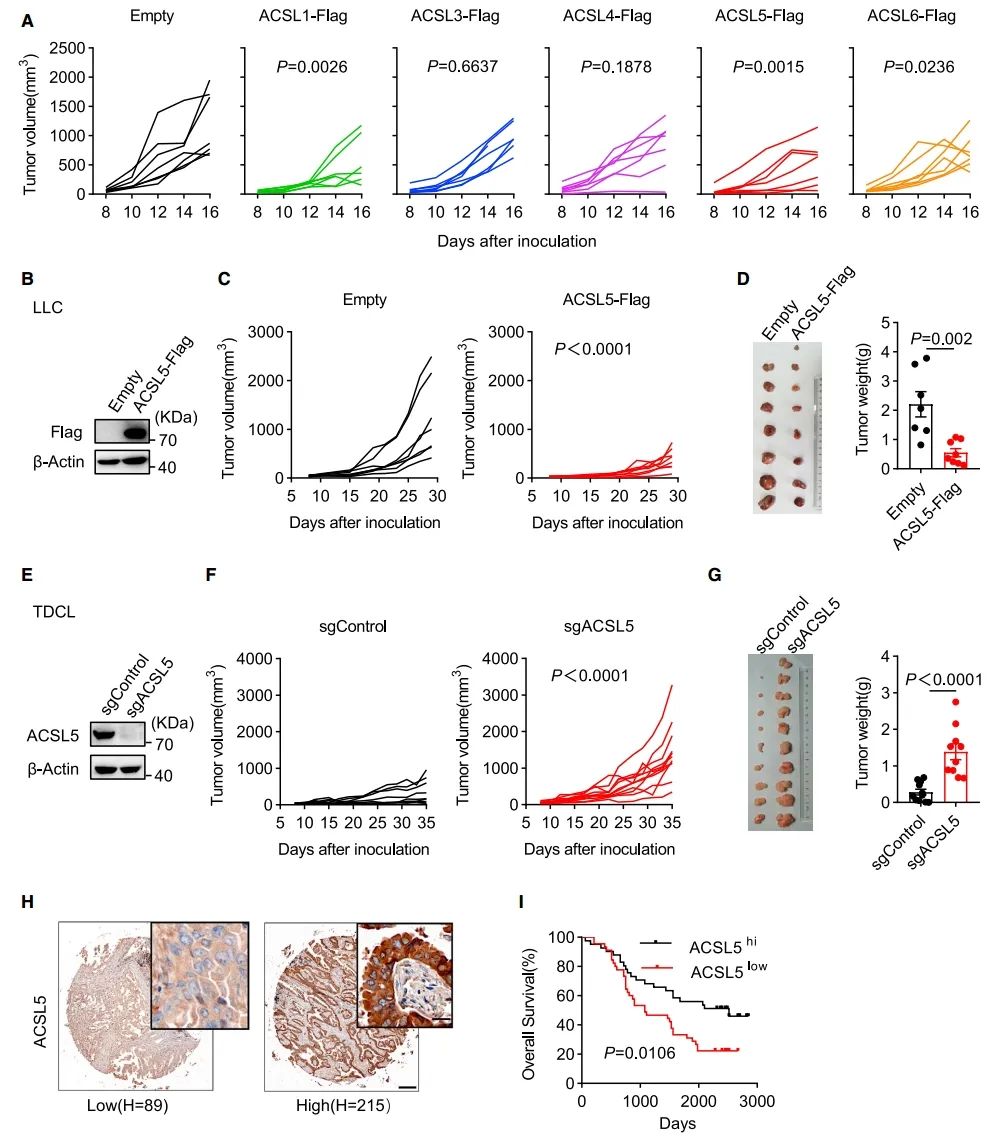
图 1:ACSL5表达对体内肿瘤生长的抑制作用
(A) 描述C57BL/6小鼠体内表达某种ACSL成员的B16F10肿瘤的个体生长情况(每组7只小鼠)。
(B–D) 展示了对照组和表达ACSL5-FLAG的LLC细胞中ACSL5的免疫印迹分析结果(B)。此外,还展示了小鼠体内LLC肿瘤的个体生长情况(C),以及在实验终点时测量的肿瘤重量(D)(每组7或8只小鼠)。
(E–G) 展示了sgControl和sgACSL5敲减的TDCL细胞中ACSL5的免疫印迹分析结果(E)。图中还显示了小鼠体内TDCL肿瘤的个体生长情况(F)以及在实验终点时的肿瘤重量(G)(每组9或10只小鼠)。
(H) 展示了人类LUAD标本中ACSL5免疫组化(IHC)染色的代表性图片。比例尺,下方200毫米,上方20毫米。
(I) 显示了表达高(41例)或低(45例)ACSL5的LUAD患者的Kaplan-Meier生存曲线。
数据表示为均值 ± 标准误。图(A)、(C)和(F)中的p值是通过双向ANOVA确定的,图(D)和(G)中的是通过双尾t检验确定的,图(I)中的是通过对数秩检验确定的。
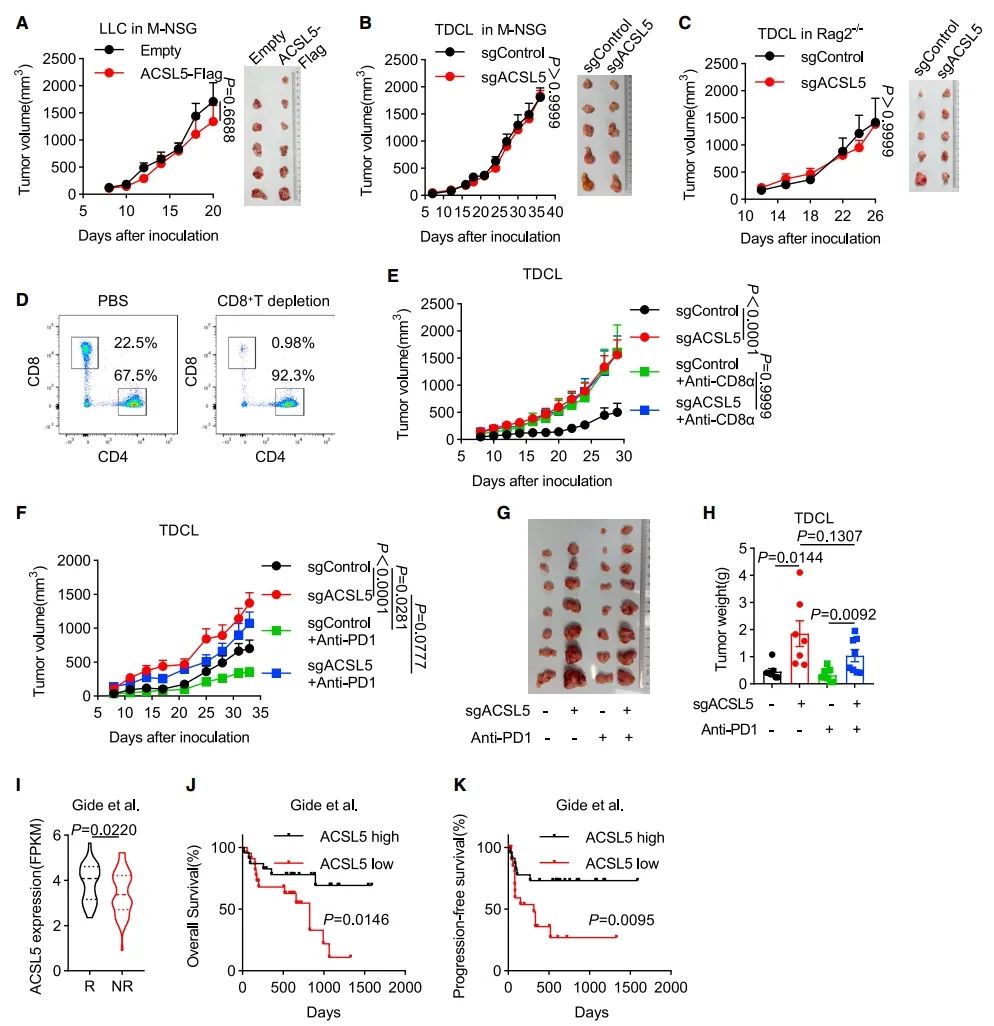
图 2:肿瘤ACSL5介导对ICB治疗的敏感性
(A) 在M-NSG小鼠中,表达ACSL5-FLAG的LLC肿瘤的生长情况。每组5或6只小鼠。
(B 和 C) 在M-NSG小鼠(B,每组5只)或Rag2-/-小鼠(C,每组5只)中,sgACSL5 TDCL肿瘤的生长情况。
(D) 通过流式细胞术分析经过抗CD8α抗体处理的小鼠脾细胞中CD8+ 和CD4+ T细胞亚群。
(E) 在经抗CD8α抗体处理的小鼠中,sgACSL5 TDCL肿瘤的生长情况(每组7或8只小鼠)。
(F–H) 携带sgControl或sgACSL5 TDCL肿瘤的小鼠接受了抗PD-1抗体治疗。监测了肿瘤体积(F和G),并在实验终点时测量了肿瘤重量(H)(每组7或8只小鼠)。
(I–K) 小提琴图比较接受ICB治疗的黑色素瘤患者中应答者与非应答者之间ACSL5的表达情况(I)。为这些ACSL5表达高或低的肿瘤患者绘制的Kaplan-Meier总生存率(J)和无进展生存期(K)曲线。
数据表示为均值 ± 标准误差。图(A)–(C)、(E)和(F)中的p值通过双向ANOVA确定,图(H)中的通过双尾t检验确定,图(I)中的通过Mann-Whitney检验确定,图(J)和(K)中的通过对数秩检验确定。
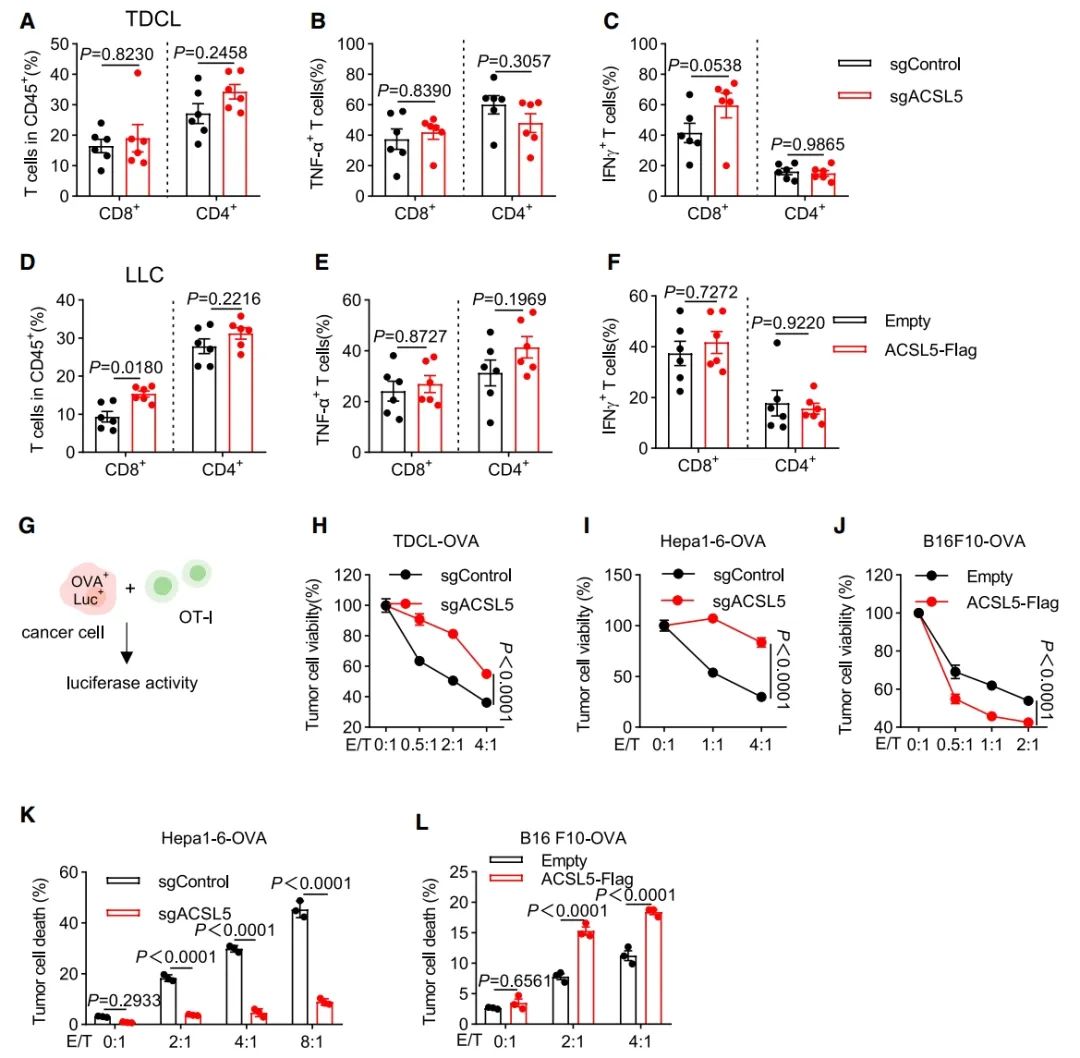
图 3:ACSL5增强肿瘤对CTL介导的细胞毒性的敏感性
(A–F) 在sgControl或sgACSL5 TDCL肿瘤(A–C)以及表达ACSL5-FLAG的LLC肿瘤(D–F)中,T细胞浸润的概况。图展示了CD45+群体中T细胞的百分比(A和D),以及表达TNF-α(B和E)或IFN-γ(C和F)的T细胞的百分比(n = 6个肿瘤)。
(G) 描述了OVA+Luc+肿瘤细胞与OT-I细胞共培养的实验设计。
(H–J) 在指定的效应细胞对肿瘤细胞比例(E:T)下,共培养了30小时(H)或48小时(I和J)的指定OVA+Luc+肿瘤细胞与OT-I细胞的相对存活率(n = 3)。
(K和L) 在与不同比例的OT-I细胞共培养48小时后,OVA+Luc+ Hepa1-6(K)或B16F10(L)的细胞死亡情况(n = 3)。
数据表示为均值 ± 标准误。图(A)–(F)和(H)–(L)中的p值通过双向ANOVA计算得出。
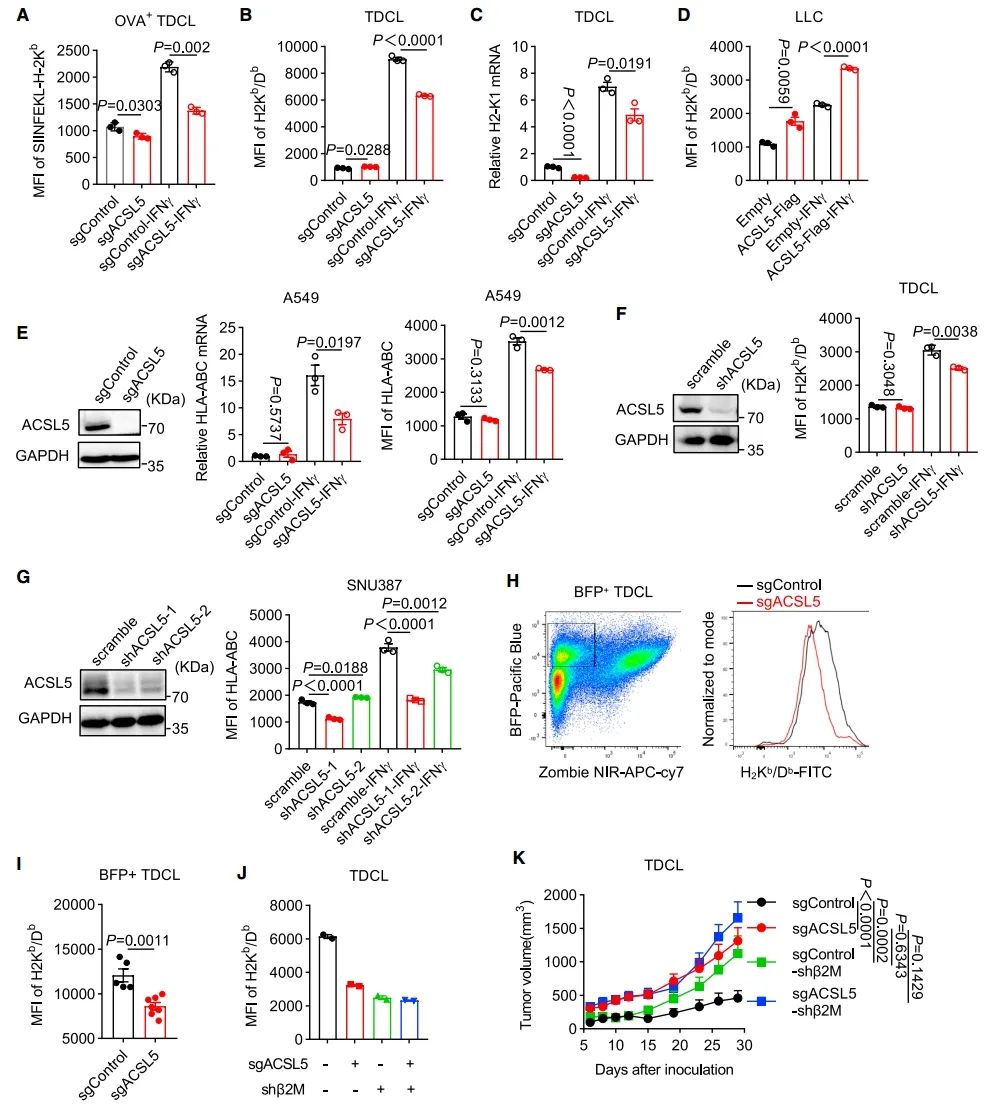
图 4:ACSL5缺失降低了细胞表面MHC-I的表达
(A) 在IFN-γ处理下,sgControl和sgACSL5 OVA+Luc+ TDCL细胞表面的SIINFEKL-H-2Kb水平(n = 3)。
(B 和 C) sgControl和sgACSL5 TDCL细胞表面的H-2Kb/Db水平(B)或总H2-K1 mRNA水平(C)(n = 3)。
(D) 对照组和表达ACSL5-FLAG的LLC细胞表面的H-2Kb/Db水平(n = 3)。
(E) sgControl和sgACSL5 A549细胞中ACLS5的免疫印迹(左)。这些细胞中HLA-ABC mRNA水平(中)和细胞表面丰度(右)被定量化(n = 3)。
(F) 在IFN-γ作用下,表达scramble或shACSL5的TDCL细胞表面的H-2Kb/Db水平(n = 3)。
(G) 表达scramble或shACSL5的SNU387细胞表面的HLA-ABC水平(n = 3)。
(H 和 I) 从sgControl或sgACSL5 TDCL肿瘤中分离的BFP+肿瘤细胞的表面H-2Kb/Db丰度(I, n = 5或7)。带有H-2Kb/Db染色的活细胞BFP+肿瘤细胞的分选策略(H)。
(J 和 K) 在IFN-γ处理下,表达scramble或shb2m的sgControl或sgACSL5 TDCL细胞的表面H-2Kb/Db丰度(J, n = 2)。这些TDCL肿瘤在C57BL/6小鼠中的生长(K, n = 9每组)。
数据表示为均值 ± 标准误。图(A)–(F)和(I)中的p值通过双尾t检验计算,图(G)中的通过单向ANOVA计算,图(K)中的通过双向ANOVA计算。
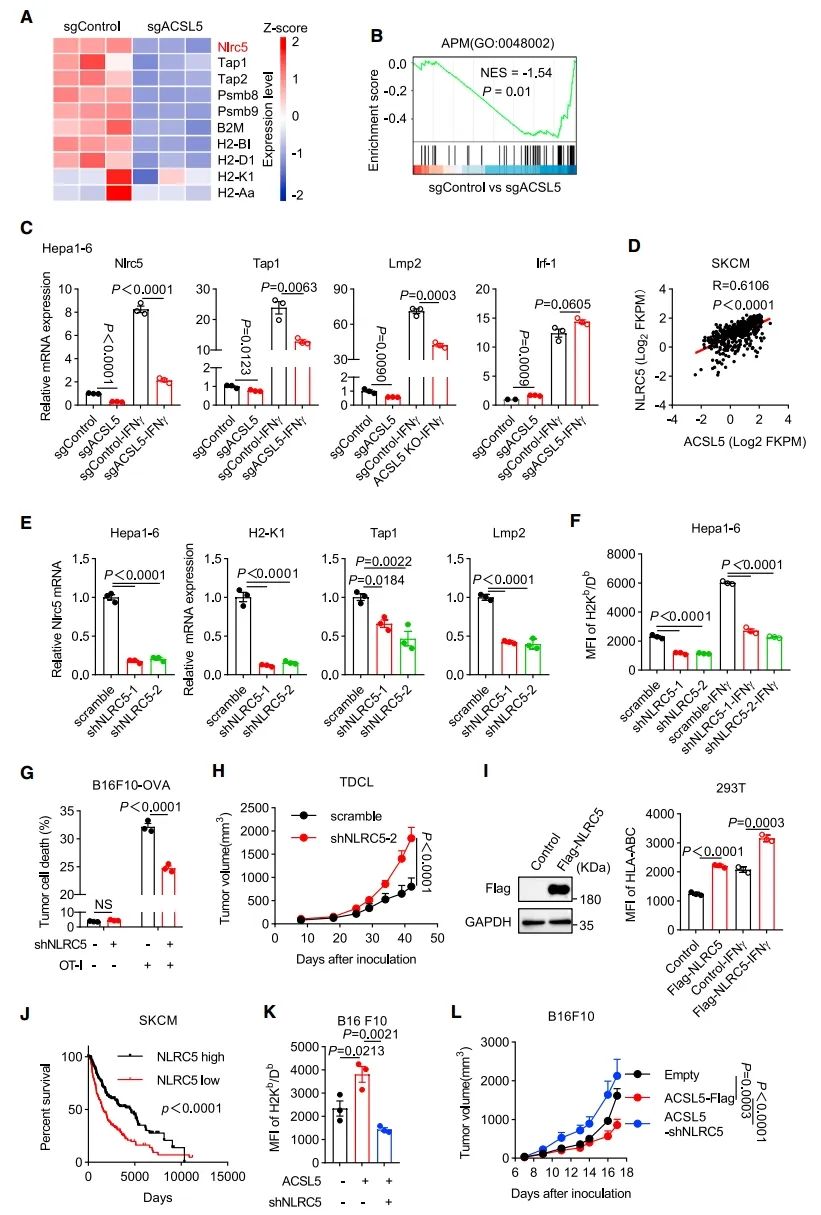
图 5:ACSL5调控NLRC5介导的抗原呈递
(A) sgControl与sgACSL5 Hepa1-6细胞中不同表达的抗原呈递机制(APM)相关基因的热图。
(B) APM特征的富集图。
(C) 在IFN-γ作用下,sgControl或sgACSL5 Hepa1-6细胞中关键APM基因的相对mRNA水平(n = 3)。
(D) 在SKCM TCGA数据集中,ACSL5与NLRC5 mRNA之间的相关性。
(E 和 F) 在表达scramble或shNLRC5的Hepa1-6细胞中,关键APM基因的相对mRNA水平(E)和细胞表面H2Kb/Db水平(F)(n = 3)。
(G) 经scramble或shNLRC5处理的OVA+ B16F10细胞与OT-I细胞共培养后的细胞死亡率(n = 3)。
(H) 在C57BL/6小鼠中表达shNLRC5的TDCL肿瘤的生长(n = 5每组)。
(I) 在293T细胞中转染NLRC5表达质粒后,带有FLAG标签的NLRC5的免疫印迹(左)。这些细胞的细胞表面HLA-ABC水平被测定(右,n = 3)。
(J) 高表达与低表达NLRC5的黑色素瘤患者的总生存率的Kaplan-Meier曲线。
(K 和 L) 在IFNg处理的B16F10细胞中,表达空质粒、ACSL5-FLAG或ACSL5-FLAG加shNLRC5的细胞表面H2Kb/Db水平(K,n = 3)。这些肿瘤在C57BL/6小鼠中的生长(L,n = 8, 7, 或 6每组)。
数据表示为均值 ± 标准误。图(C)和(I)中的p值通过双尾t检验确定,图(D)通过Pearson相关系数确定,图(E)、(F)和(K)通过单向ANOVA确定,图(G)、(H)和(L)通过双向ANOVA确定,图(J)通过对数秩检验确定。
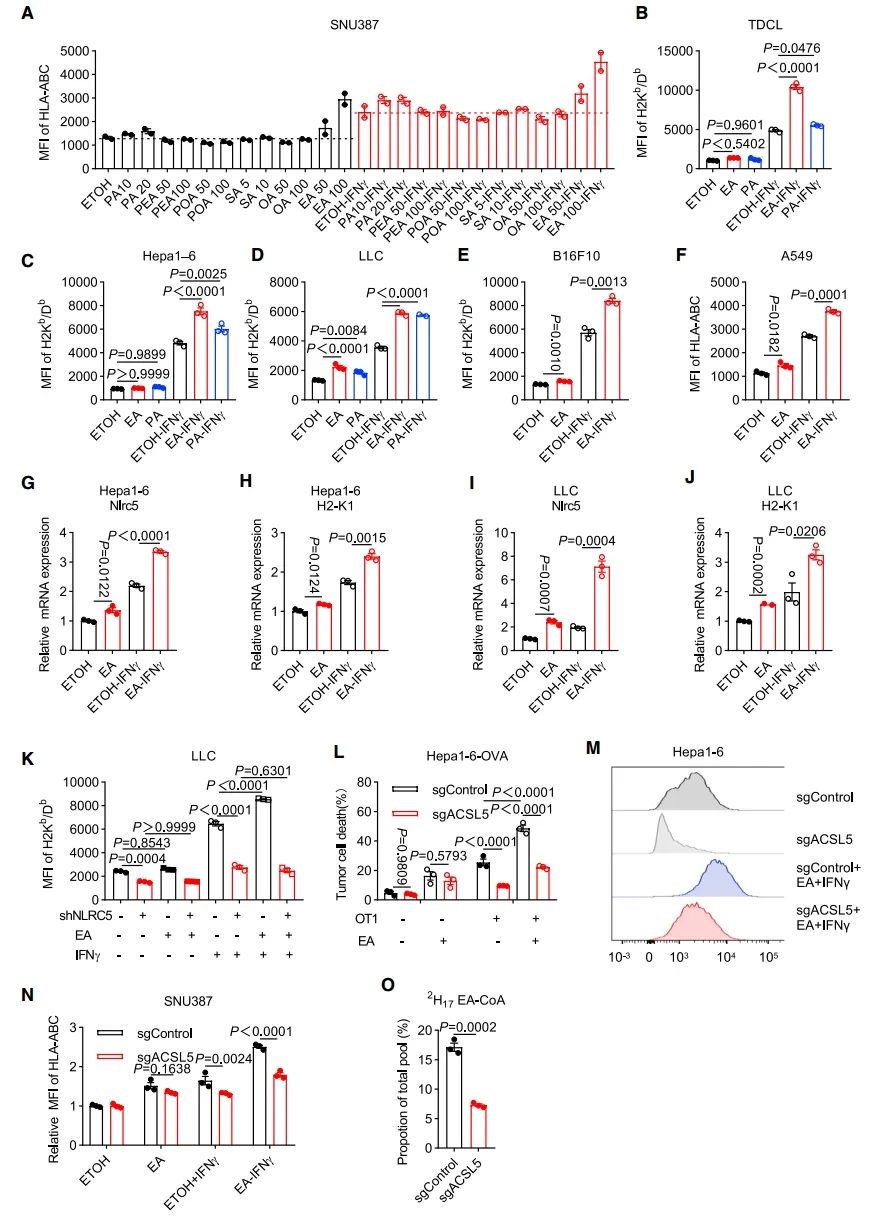
图 6:EA通过ACSL5-NLRC5轴促进肿瘤抗原呈递并增强肿瘤对CTL介导的细胞毒性的敏感性
(A) 在IFN-γ处理后,SNU387细胞经不同浓度的长链脂肪酸(LCFAs)处理后的细胞表面HLA-ABC水平(n = 2)。
(B–E) 在EA或PA处理后接IFN-γ处理的指定肿瘤细胞的H2Kb/Db细胞表面表达(n = 3)。
(F) 经EA和IFN-γ处理的A549细胞的细胞表面HLA-ABC水平(n = 3)。
(G–J) 指定Hepa1-6(G和H)或LLC细胞(I和J)中Nlrc5(G和I)和H2-K1(H和J)的相对mRNA水平(n = 2–3)。
(K) scramble或shNLRC5表达的LLC细胞的H2Kb/Db细胞表面表达(n = 3)。
(L) 经EA处理后与OT-I共培养(E:T = 2:1)的指定Hepa1-6细胞的细胞死亡情况(n = 3)。
(M) 指定Hepa1-6细胞上H-2Kb/Db表面染色的代表性图像。
(N) 在EA和IFN-γ处理下指定SNU387细胞中HLA-ABC丰度的变化倍数(n = 3)。
(O) 经2H17-EA(50 mM)处理24小时的Hepa1-6细胞中2H17-EA-CoA的相对含量(n = 3)。
数据表示为均值 ± 标准误。图(B)–(D)和(K)中的p值通过单向ANOVA计算,图(E)–(J)和(O)中的通过双尾t检验计算,图(L)和(N)中的通过双向ANOVA计算。
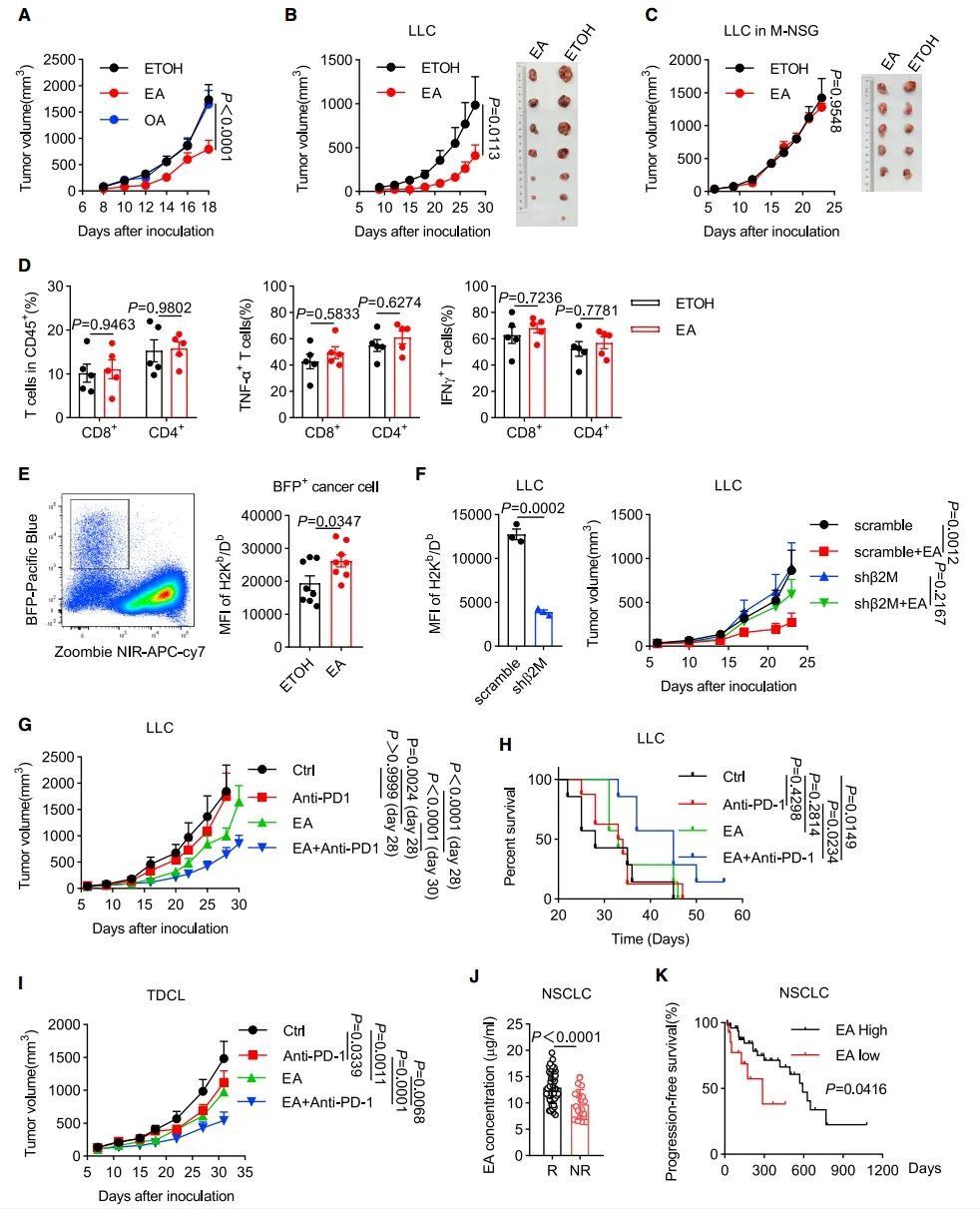
图 7:EA抑制肿瘤生长并增强ICB治疗的敏感性
(A) 在补充了乙醇(ETOH)、EA或OA(10 mg/kg)的C57BL/6小鼠中,B16F10肿瘤的生长情况(n = 9或10每组)。
(B 和 C) 在补充了ETOH或5 mg/kg EA的C57BL/6(B,n = 7或6每组)或M-NSG小鼠(C,n = 5每组)中,LLC肿瘤的生长情况。
(D) EA处理的B16F10肿瘤中T细胞浸润的概况(n = 5)。
(E) 从对照组或EA处理的B16F10肿瘤中分离的BFP+肿瘤细胞表面的H-2Kb/Db丰度(n = 8个肿瘤)。
(F) 表达scramble或shb2m的LLC细胞表面的H-2Kb/Db水平(左)。这些肿瘤在接受EA处理的小鼠中的生长情况(n = 9或10每组)。
(G 和 H) EA补充对LLC肿瘤中PD-1阻断治疗的效果。监测了肿瘤体积(G, n = 7或8),并绘制了生存曲线(H)。
(I) 在C57BL/6小鼠携带TDCL肿瘤中,EA加PD-1阻断的联合治疗(n = 9或10每组)。
(J) 在对ICB治疗为应答者(n = 47)或非应答者(n = 22)的患者血浆中,EA浓度的情况。
(K) 对血浆EA水平高或低的NSCLC患者,无进展生存期的Kaplan-Meier曲线。
数据表示为均值 ± 标准误。图(A)–(D)、(F, 右)、(G)和(I)中的p值通过双向ANOVA计算,图(E)和(F, 左)中的通过双尾t检验计算,图(H)和(K)中的通过对数秩检验计算,图(J)中的通过Mann-Whitney检验计算。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏