OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

1.肿瘤微环境中调节性T细胞的代谢
Guoliang Cui – HI-TRON/德国癌症研究中心DKFZ,迈因茨/海德堡,德国
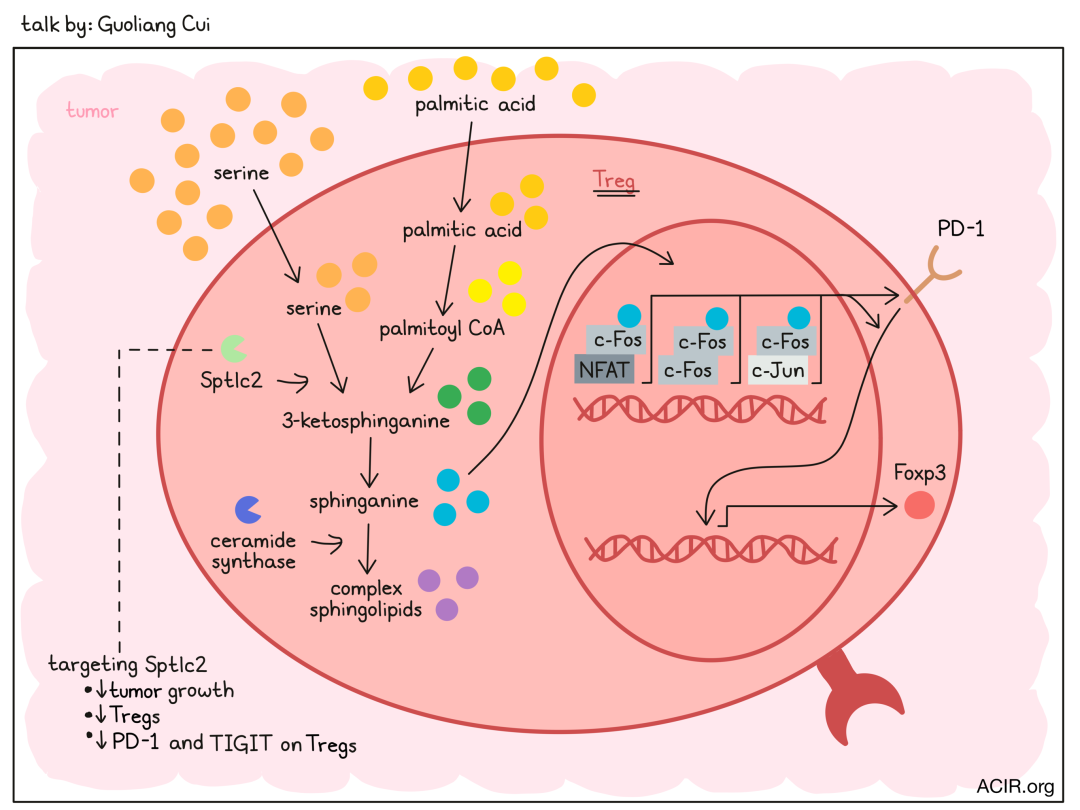
为了系统性地阐明影响调节性T细胞(Treg)在肿瘤微环境中积聚的代谢途径,崔国亮及其团队使用了一种商业化试剂盒,检测出肿瘤中存在的630种代谢物,并对三种不同的小鼠肿瘤类型进行了分析。他们采用无偏倚的计算方法,确认了鞘脂代谢途径的重要性,并发现鞘脂新生合成的底物,即棕榈酸(棕榈酰辅酶A的前体)和丝氨酸,在肿瘤微环境中富集。在这一途径的早期步骤中,酶丝氨酸棕榈酰转移酶长链底物2(Sptlc2)催化棕榈酰-CoA和丝氨酸的缩合,生成3-酮鞘氨醇,此后转化为鞘氨醇,进一步生成更复杂的鞘脂。
与脾脏中的Tregs相比,肿瘤浸润的Tregs在蛋白水平上表现出更高的Sptlc2,这表明Tregs能够适应并响应肿瘤微环境中底物的变化。在SptlcFl/FlFoxp3YFP-Cre小鼠中,特异性地消除Treg中的Sptlc2导致肿瘤生长减缓,肿瘤中Tregs的数量减少,以及肿瘤中Tregs上PD-1和TIGIT的表达降低。在一系列精妙的实验中,崔和同事们发现,只有当肿瘤微环境中丝氨酸富集时,特异性地消除Treg中的Sptlc2才会影响肿瘤生长。通过抑制鞘氨醇向复杂鞘脂转化的鞘烷醇合酶,证明了鞘脂代谢途径对CD4+细胞中的Foxp3和调节性T细胞中的PD-1的表达至关重要。
为了理解这一机制,崔进一步展示了,鞘脂代谢途径的代谢产物鞘氨醇可以直接与c-Fos蛋白结合,作为一种“分子粘合剂”,稳定c-Fos同源二聚体和与其他转录调节因子(如NFAT2和c-Jun)形成的c-Fos异源二聚体,促进c-Fos结合到染色质可接触区域的靶基因上,包括编码PD-1和PD-1信号通路部分的基因。增加的PD-1和PD-1信号的表面表达随后诱导Foxp3的表达和Treg的分化。总的来说,崔提供了证据,证明肿瘤微环境中丝氨酸水平的增加通过鞘脂代谢途径的代谢产物和c-Fos–PD-1信号通路,促进了Treg的积聚,这可能为消除肿瘤Treg细胞提供了新的策略。
2.慢性感染和癌症期间T细胞的生存方式:对免疫治疗的意义
Rafi Ahmed-美国亚特兰大埃默里大学医学院
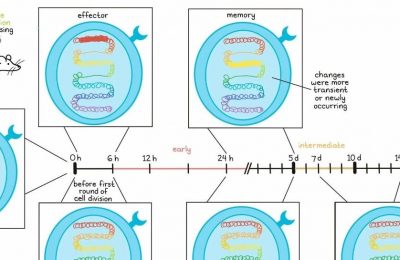
在他的主题演讲中,Rafi Ahmed概述了他在CD8+ T细胞表型、发展过程和功能的研究,这些研究初步在某些病毒感染中发现,后来也在癌症中得到应用。相较于初次感染后的激活反应——在此情况下,具有高度细胞毒性的T细胞在病毒暴露后迅速增多(然后衰退),并通常可以完全控制感染——长期存在的病毒会激发一种分化机制,形成一种“慢性资源细胞”,这种细胞保留了干细胞样的、未分化的特性,这些特性主要表现在休眠细胞上,而这些细胞保持了在淋巴组织内增殖和定居的潜力。
这些干细胞样的CD8+ T细胞在感染的最初几周内由天然T细胞产生。在任何特定的时刻,这些细胞慢慢自我更新,并分化成为具有高度功能的效应细胞,这些细胞离开淋巴组织,通过血液流通,定位并杀死表达抗原的细胞,从而控制慢性感染并抑制病毒。在PD-1轴阻断之后,这些新分化出来的细胞被释放,从而产生抗病毒或抗肿瘤的免疫反应。这种增强的细胞增殖和效应功能之后,会迅速分化为末端、接近死亡的表型,此时效应能力较弱,并在靶细胞和淋巴组织中保持存在。
伴随着这些表型变化的是,细胞因子/趋化因子及其受体、效应分子、刺激和抑制免疫调节分子的表达也发生变化,同时关键的经典转录因子(例如TCF1和TOX)也发生改变,这些变化现在已经被详细描述。在回顾了慢性病毒感染和癌症的重要研究后,Ahmed展示了新的工作成果,其中包括:(1)在人类HPV阳性头颈癌的淋巴样结构中存在这种干细胞样的PD-1+TCF1+CD8+ T细胞;(2)在HPV靶向细胞中有一个高度选择性的TCR库,有趣的是,特异性对HPV E2和E5蛋白而非经典的E6和E7致癌蛋白的T细胞最丰富,这为疫苗和TCR工程化的T细胞提供了新的机会;(3)复制了干细胞特性和功能的表型特征。最后,他描述了一些令人激动的结果,这些结果证明通过将IL-2(依赖于高亲和力的CD25 IL-2受体亚基)添加到抗PD-1轴治疗中,可以产生具有更高功能能力、更低耗竭标志,并且其转录谱与资源型干细胞样的CD8+ T细胞不同的效应细胞。
这些结果表明,向末期感染或癌症患者的治疗中添加IL-2可能会提高抗PD-1轴治疗的效果。此外,这也证实了干细胞样的CD8+ T细胞在免疫反应中的关键作用,它们是维持长期抗感染或抗癌免疫反应的重要因素。这种理解不仅有助于我们更好地理解免疫系统如何应对慢性病毒感染和癌症,而且也为发展新的免疫疗法提供了新的思路。
3.靶向树突状细胞治疗癌症
Miriam Merad-美国纽约西奈山伊坎医学院
肿瘤免疫微环境(Tumor Immune Microenvironment,TIME)中的炎症细胞对疾病的进程具有直接影响。为了揭示并利用这背后的机制,Miriam Merad专注于研究树突状细胞和巨噬细胞的作用。树突状细胞负责将免疫荷载(immune cargo)传递到淋巴结以启动T细胞反应,而巨噬细胞既能控制炎症以促进修复,也能引发免疫抑制。Merad利用了术前环境,详细描述了她和一个多学科团队共同建立的TARGET平台(新辅助研究小组评估治疗方法)的优势,该平台能对基线和免疫扰动后的TIME进行评估。
在已经发表的来自TARGET平台的研究中,肝细胞癌患者对PD-1阻断治疗的反应与否,导致了其免疫细胞数量和种类的差异。在对PD-1阻断反应的患者中,扩增了一部分PD-1hiIL-21+CXCL13+类似淋巴滤泡辅助性的CD4+ T细胞和效应性CD8+ T细胞,而在未反应者中,终末耗竭的CD8+ T细胞和调节性T细胞(Tregs)的水平较高。
虽然在治疗前就存在并在治疗后扩增的T细胞在响应者和非响应者的肿瘤病灶中都有高度浸润,但其表型轨迹各异。为了研究导致不同反应的局部因素,Merad使用了PIC-Seq技术,这是一种能鉴定从肿瘤组织中分离出的物理相互作用细胞表型的技术。
有趣的是,响应者中发现了免疫调节性mregDCs、CXCL13+CD4+ T细胞和前体CD8+ T细胞之间的三重相互作用,并与CD8+效应细胞的富集有关,但在非响应者中也存在。mregDCs和CD4+ T细胞共享多个受体-配体对,在响应者中导致了效应性CD8+细胞的产生,但在非响应者中则导致了终末细胞的形成,这引发了一个问题:在不同的生态位中,mregDCs是如何不同地发挥功能并导致如此不同结果的。
先前的研究表明,细胞碎片的摄取能诱导出mregDC表型,这个过程会中止更多碎片的摄取,同时引发了对获取到的cargo的抗原呈递能力。尽管这个转变过程与众多已知的调控细胞迁移的分子无关,但mregDCs存在于正常和炎症组织中,并表现出胆固醇生物合成的能力。
Merad的报告指出,树突状细胞的成熟依赖于胆固醇向细胞表面的运动,抑制胆固醇的转运会降低其成熟。她的团队发现,肝细胞癌中的mregDCs在病灶中的数量偏高,而且它们的胆固醇合成能力也更强。这些mregDCs在病灶中的存在,通过与免疫调节性T细胞共享的配体,能够抑制T细胞的活性。这项发现为我们提供了一个新的治疗思路:通过抑制mregDCs的胆固醇合成能力,可能可以使T细胞的反应性恢复,从而增强免疫疗法的效果。
4.癌症免疫治疗的机制基础
Ira Mellman – 美国加利福尼亚州旧金山市Genentech公司
癌症免疫周期是描述生成和维持对肿瘤的自发免疫反应的关键步骤的一个理论。这个理论也帮助我们找出可能破坏有效免疫反应的关键环节,以便进行干预和修正。Ira Mellman首先借助这个周期,解释了免疫检查点抑制剂如何通过T细胞产生抗肿瘤反应,以及T细胞如何深受肿瘤免疫微环境(TIME)的影响。
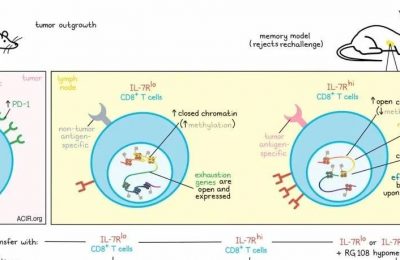
研究已经证实,长期的肿瘤抗原暴露最终会导致功能不全且寿命短的“耗竭”T细胞的产生。人们曾经以为抗PD-1轴疗法能逆转或预防T细胞耗竭,但对耗竭的表观遗传学的理解使得这种观点无法成立。现在,人们认为早期中断抑制性PD-1轴功能可以导致更多新生T细胞的激活和改善分化。
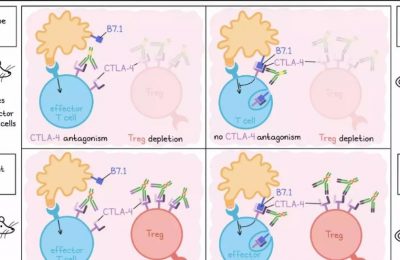
已有研究表明,PD-1信号阻断了关键的CD28共刺激信号,PD-L1阳性的树突状细胞对抗PD-1轴的效应非常关键。Mellman进一步描述了他近期的工作,他发现TIGIT是CD226共刺激受体的内源性竞争物,阻断其对PVR(CD226的激活配体)的阻断可以阻止最大程度的T细胞刺激。这些研究表明同时阻断两条通路将是最佳选择。
在非小细胞肺癌患者中,联合PD-L1和TIGIT阻断在2期临床试验中显示出提高总生存率的可能,目前正在等待3期研究的最终结果。机制上,联合阻断能显著上调CD226,并在特异性抗原和大量的CD8+ T细胞中下调TOX,从而改善肿瘤浸润淋巴细胞的质量。TOX的表达降低需要CD226信号传导。
大规模的单细胞分析清晰地描述了多种T细胞状态和关键标记物,包括位于从幼稚细胞到死亡细胞连续谱上的细胞,如标记为Slamf6的T干细胞记忆细胞,标记为干扰素途径的效应细胞,标记为CCL5的临时效应样细胞,以及一群晚期效应器/耗竭细胞。
TCR测序的分析结果显示,同时阻断PD-L1和TIGIT能显著增强抗原特异性T细胞在引流淋巴结(dLN)、血液和肿瘤中的数量。逆时序分析揭示,虽然单个检查点疗法有一定的改善(例如在dLN中增加效应细胞的数量,促进效应细胞从dLN向肿瘤迁移,以及减少耗竭的细胞组分),但是联合阻断PD-L1和TIGIT可以进一步优化这些影响。这种联合阻断导致TSCM和T效应样细胞在dLN中的扩增,并使具有多种功能的寡克隆细胞通过血液进入肿瘤。在肿瘤内部,他们观察到效应记忆细胞和CTLs的出现,但它们最终分化成终末耗竭细胞的程度有限。这种有限的耗竭分化似乎依赖于共刺激通路。
初步数据显示,TIGIT抗体上的Fc结构域可能对髓系细胞产生信号作用,使其分泌促炎因子,限制Treg的抑制作用,并激活NK细胞。这些发现表明可能存在多条活跃的通路,这与我们从2期联合治疗试验中获取的生物标志物数据相吻合。
最后,Mellman描述了一种创新的高通量实验方法(即将发表),该方法在小鼠耳朵上创建了一系列可以种植肿瘤细胞的”井”。可以分别监测每个”井”中细胞的生长,并可以测试检查点阻断或添加生长因子等干预措施的效果。他们发现,不同的肿瘤细胞株在植入时表现出不同的行为,这表明肿瘤细胞可能具有自主的效应。值得注意的是,即使使用同一种肿瘤细胞样本进行种植,不同”井”之间的肿瘤细胞生长和T细胞浸润也存在差异。这表明局部细胞环境在肿瘤生长中起着关键作用,尽管所有的”井”都受到了类似的T细胞反应。
5.揭示胰腺癌对T细胞介导的细胞毒性作用的肿瘤内在抵抗机制
Judit Díaz-Gómez – 巴塞罗那Vall d’Hebron肿瘤研究所(VHIO)
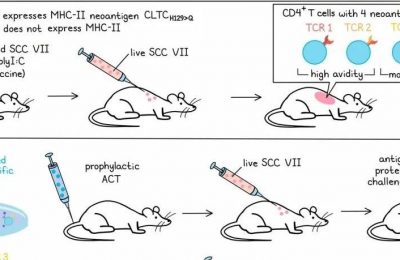
为了找到可能使胰腺癌对免疫疗法更敏感的新途径,Judit Diaz-Gomez及其团队利用全基因组的CRISPR/Cas9敲除筛选技术,寻找限制特异性新抗原TCR转导T细胞杀伤患者源胰腺癌细胞系TCL-4177的基因。他们主要关注那些在被敲除后,能增强T细胞杀伤效应的基因。研究人员发现了35个能够抑制T细胞介导的杀伤效应的基因,这些基因以前并未被研究过。
将这些基因绘制在全蛋白组分析网络中,他们发现自噬和泛素化途径、染色质重塑、囊泡转运、蛋白质折叠以及ESCRT复合体都参与了肿瘤的内在抵抗机制。目前为止,他们已经独立验证了10个涉及四个不同途径的基因中的7个,并且发现沉默其中四个基因能增强T细胞对另一种胰腺肿瘤细胞系TCL-CABA的杀伤效应,这些T细胞具有不同的(未知)特异性。
其中最有前景的候选基因ITGB1和MARCH5已经在临床数据中得到了回顾性分析,结果显示,ITGB1或MARCH5的低表达与胰腺导管腺癌患者的总体生存率改善有关。目前,他们正在对更多的候选基因进行进一步的分析和验证,并进行相关的机理研究。
6.CLN-617是一种首创的融合蛋白,能在注射的肿瘤中特异性保留IL-2和IL-12,并强力触发全身性抗肿瘤免疫反应
Naveen Mehta – Cullinan Oncology, 美国剑桥
多项证据表明,IL-2 和 IL-12 不仅是强大的抗肿瘤细胞因子,且在信号通路上是相联系的,同时它们的活性也是协同的。然而,当它们在临床上通过全身给药时,各自都会受到毒性的限制。为了克服这些限制,研究人员根据三个原则设计了 CLN-617:(1)细胞因子主要以自分泌/旁分泌的方式起作用,因此应进行局部给药; (2)局部注射的细胞因子需要进行修改以限制全身暴露并增强保留效果; (3)细胞因子通常与其他细胞因子协同作用。因此,他们设计了一种单分子,该分子编码未修饰的人源 IL-2 和 IL-12,并与胶原结合域(hLAIR2)和人血清白蛋白链接,以在肿瘤中保留注射的 CLN-617。
CLN-617 以单位 nM级别 的亲和力结合胶原,并在体外试验中保持了完全的 IL-2 和 IL-12 刺激活性。对小鼠版本的 CLN-617(mCLN-617)进行肿瘤内注射后,肿瘤内的浓度超过了全身观察到的最大浓度的 10 倍以上。在多种肿瘤模型中,包括对抗 PD-1 轴疗法耐药的模型中,单次肿瘤内(i.t.)注射后,单药疗法改善了生存率。例如,在 MC38 中,与全身抗 PD-1 相比,i.t. mCLN-617 观察到 10/10 的完全反应(CRs)。该疗法也被很好地耐受。在初始肿瘤植入后的 60 天,对存活的小鼠进行再挑战实验,显示出强烈的记忆反应。此外,在皮下双侧和肝转移模型中,尤其是与抗 PD-1 疗法结合使用时,显示出强大的远端杀伤效应。重要的是,对注射和未注射肿瘤的分析都显示出增强的 CD8+:Treg 比例,并且在血液中观察到肿瘤特异性 CD8+ T 细胞的显著诱导,显示出系统性效果。预计将于 2023 年开始临床研究,与 PD-1 轴阻断疗法进行联合治疗。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏