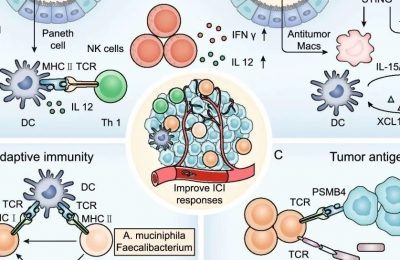
36.2 卵巢癌的肿瘤免疫治疗挑战
在美国,每年有近9万名女性被诊断为妇科恶性肿瘤,超过2.8万名女性因该疾病而去世。对于早期发现的患者,手术、放疗和化疗的综合治疗通常可以治愈。然而,卵巢癌常常在晚期才被确诊,尽管接受了适当的治疗,许多患者仍会复发。即使采用了改进的细胞减灭术和基于铂类/紫杉烷的化疗,卵巢癌的预后依然不佳,5年生存率仅为38%。
复发性卵巢癌的有效治疗靶点包括DNA损伤修复机制和血管内皮生长因子(VEGF)及其受体(VEGFR)的信号通路。贝伐单抗是一种人源化抗VEGF单克隆IgG1抗体,已在辅助治疗中显示出延长无进展生存期的效果。最新数据表明,VEGF和VEGFR通路通过增加DNA损伤和肿瘤突变负荷来调节免疫反应。突变负荷的增加会导致新抗原的表达增多,这与结直肠癌和黑色素瘤患者对免疫检查点抑制剂的临床应答密切相关。
大约50%的高级别上皮性卵巢癌患者在同源重组修复(HRR)中存在获得性或遗传性功能缺陷,这一过程对于高保真DNA双链断裂的修复至关重要。此外,所有高级别上皮性卵巢癌均表现出与p53功能丧失相关的基因组不稳定性。聚(ADP-核糖)聚合酶(PARP)1在DNA损伤修复中发挥多种作用,包括通过碱基切除修复途径修复DNA单链断裂。奥拉帕尼是一种PARP抑制剂,已被证明可延长BRCA突变型肿瘤患者的生存期。
临床前研究表明,PARP抑制剂可以通过局部抗原释放,增强肿瘤对抗辐射或DNA损伤剂的全身抗肿瘤反应,特别是在自发性或遗传性DNA缺陷的背景下。因此,PARP抑制剂或其他DNA修复抑制剂所引发的DNA损伤增加,不仅会导致更高的突变负担,还能扩大新抗原的多样性,从而可能增强免疫系统对肿瘤的识别和攻击。
PARP抑制剂还与免疫调节密切相关。Huang等人的研究显示,在BRCA1突变的卵巢癌异种移植模型中,PARP抑制剂talazoparib (BMN 673)能够增加腹膜中的CD8+ T细胞和自然杀伤细胞的数量,同时促进干扰素γ和肿瘤坏死因子α的产生。
这些数据表明,PARP抑制剂可能在复发性卵巢癌的治疗中,与免疫检查点抑制剂协同产生临床益处。目前,PD-L1抑制剂MEDI4736 (durvalumab)与奥拉帕尼联合治疗正在实体瘤和复发性卵巢癌患者中进行I/II期临床研究。
血管生成途径与免疫反应和DNA修复机制之间存在相互作用。肿瘤缺氧可导致参与DNA损伤修复的基因和蛋白质的下调,从而进一步加剧DNA损伤、基因组不稳定性和细胞死亡。在临床前和临床研究中,VEGF已被证明能够抑制抗肿瘤免疫反应,包括抑制树突状细胞的成熟、抑制T细胞反应、增加调节性T细胞的增殖以及促进骨髓源性抑制细胞(MDSCs)的积累。此外,在小鼠和人类肿瘤细胞系以及脾脏的MDSCs中,缺氧条件通过缺氧诱导因子-1α依赖机制上调了PD-L1的表达。血管生成抑制剂在妇科癌症中的疗效已经得到了证实,例如贝伐单抗和口服VEGFR 1-3酪氨酸激酶抑制剂cediranib均显示出延长无进展生存期的效果。
虽然最初认为上皮性卵巢癌对免疫治疗的反应不佳,但实际上,研究表明免疫系统在控制上皮性卵巢癌细胞生长方面发挥了关键作用。这一观点得到了多个研究结果的支持:卵巢癌中TILs水平的增加与预后改善相关,肿瘤中含有T细胞的患者5年生存率为38%,而肿瘤中不含T细胞的患者5年生存率仅为4.5%。在另一项关于卵巢癌中T细胞亚型的研究中,肿瘤浸润的CD8+淋巴细胞频率更高,以及CD8+淋巴细胞与调节性T细胞(Tregs)的比例增加,也与生存率的提高相关。
此外,肿瘤反应性抗体和T细胞已从上皮性卵巢癌患者的外周血中分离出来,提示存在自发性的抗肿瘤免疫反应。同时,卵巢癌中过表达的肿瘤抗原如CA-125、叶酸受体α (FRalpha)、NY-ESO-1和MAGE-A3,可以用于诱导适应性免疫反应。这些发现为探索上皮性卵巢癌的不同免疫治疗策略提供了坚实的理论依据。
36.2.1 增强肿瘤抗原识别的治疗方法
旨在增强免疫系统识别肿瘤的策略主要分为两类:疫苗和先天免疫激活剂。后者包括TLR激动剂、I型干扰素(IFN)以及溶瘤病毒。
36.2.1.1 疫苗
针对上皮性卵巢癌中表达的独特组织分化抗原的研究,推动了多种疫苗接种方法的发展。这些方法包括由特定肽和蛋白质组成的简单疫苗制剂,以及更为复杂的策略,如工程化细胞疫苗、树突状细胞(DC)疫苗、病毒载体疫苗和溶瘤病毒。大多数研究集中于上皮性卵巢癌中已知的癌睾丸抗原(如NY-ESO-1)和蛋白质(如p53、survivin、HER-2和MUC1)的过表达。例如,有研究显示43%的晚期卵巢癌患者表达NY-ESO-1。
2014年发表的一项II期研究评估了22例上皮性卵巢癌患者(82%为浆液性组织学类型且NY-ESO-1阳性)在标准治疗(减脂手术和铂基化疗)后接种HLA-A*0201限制性NY-ESO-1b肽的效果。研究结果显示,中位总生存期为48个月,中位疾病进展时间为21个月(95% CI, 16-29个月)。
虽然许多研究已证明这些疫苗策略能够诱导免疫应答,但很少有研究显示其显著的临床益处。这可能是因为这些策略尚不足以克服对自身抗原的免疫耐受,并有效激活抗原特异性T细胞。然而,尽管如此,这些方法在与其他疗法联合使用时,可能仍具有潜在的价值。
36.2.1.2 先天免疫激活剂
通过抗原呈递细胞(APCs)增强肿瘤抗原呈递的另一种策略是利用靶向先天免疫应答的药物。APCs的抗原加工和呈递过程需要激活信号,这一信号可以通过激活模式识别受体(PRRs)如Toll样受体(TLRs)来实现。TLRs能够识别多种病原体的共有特征分子,还能感知肿瘤微环境中的“危险信号”,这些信号由凋亡细胞释放的内源性分子构成。
TLR8的小分子激动剂VTX2337 (motolimod)与阿霉素脂质体联合使用在晚期上皮性卵巢癌患者中的I期研究显示了良好的安全性、免疫激活效果和临床获益。目前,一些II期研究正在评估motolimod与其他免疫疗法或脂质化阿霉素的联合效果。
活化的APCs会产生I型干扰素(IFN),这在抗病毒免疫应答中发挥重要作用,同时也是APCs呈递肿瘤抗原的必要条件。尽管I型IFN已在多种癌症类型中进行了评估,并被批准用于切除黑色素瘤患者的辅助治疗,但Alberts等人的研究显示,全身或腹腔给药IFNα在上皮性卵巢癌患者中的疗效有限,并且伴有较高的毒性。
溶瘤病毒因其特性能够选择性地在癌细胞中复制,而不影响正常组织。除了作为肿瘤消融剂,溶瘤病毒还通过释放肿瘤抗原、PRR配体和危险信号,及产生I型IFN,从多个层面激活先天免疫反应。几项在上皮性卵巢癌患者中使用溶瘤病毒的临床试验显示,溶瘤病毒在部分患者中具有良好的安全性和持久的临床益处。
总的来说,通过先天免疫系统增强肿瘤抗原呈递的策略已被证明是安全的,但目前其疗效仍有限。未来,可能需要通过联合治疗来增强这些药物在上皮性卵巢癌患者中的效果,即结合靶向T细胞活化和适应性免疫应答的疗法,以进一步强化由疫苗或先天免疫激活剂诱导的T细胞应答。
36.2.2 增强T细胞活化的治疗方法
T细胞的存活、增殖和活化受多种因素的调控,包括细胞因子以及一系列免疫刺激和抑制受体。已有一些研究探索了靶向T细胞的药物在上皮性卵巢癌免疫治疗中的应用,涵盖了旨在激活T细胞的药物以及过继性T细胞疗法等策略。
36.2.2.1 细胞因子
细胞因子白介素(IL)-2和IL-12是有效的T细胞增殖和细胞毒性激活剂,作为抗癌药物的用途已在多种癌症类型中进行了探索,包括卵巢癌。然而,这些药物的系统性给药受到毒性的限制。在一项针对持续或复发性上皮性卵巢癌患者的I/II期研究中,腹腔注射IL-2的总体缓解率为25.7%,但该治疗方案伴随着显著的毒性。
为了克服这一问题,研究者探索了另一种IL-12的递送策略,即使用表达IL-12的质粒。在最近的一项研究中,22例复发性上皮性卵巢癌患者接受了腹腔内注射EGEN-001(由脂聚合物制备的IL-12质粒),结果显示35%的患者病情稳定。
36.2.2.2 免疫检查点
对调节T细胞活化的共刺激和共抑制受体的识别,推动了针对这些受体的抗体的开发。特别是,靶向抑制性受体如细胞毒性T淋巴细胞相关抗原4(CTLA-4)、程序性死亡1(PD-1)及其配体(PD-L1)的抗体已进入临床开发的后期阶段。其中,靶向CTLA-4的药物伊匹木单抗(ipilimumab)已被批准用于转移性黑色素瘤,靶向PD-1的药物纳武利尤单抗(nivolumab)和帕姆珠单抗(pembrolizumab)则已被批准用于多种类型的转移性肿瘤。
基于这些发现,免疫检查点抑制疗法在上皮性卵巢癌患者中的应用得到了探索。虽然CTLA-4靶向抗体在转移性黑色素瘤中显示出疗效,但作为单一药物,其在上皮性卵巢癌中的疗效迄今仍然有限。
在一项针对11例接受GVAX(表达粒细胞-巨噬细胞集落刺激因子的自体肿瘤细胞疫苗)治疗的上皮性卵巢癌患者的研究中,伊匹木单抗治疗导致其中1例患者获得了超过4年的客观反应。然而,新的临床数据表明,靶向PD-1和PD-L1可能是治疗上皮性卵巢癌的更有前景的策略。Hamanishi及其同事发表了一项关于抗PD-1抗体纳武利尤单抗的II期研究,研究对象为20例经过重度预处理的晚期抗铂上皮性卵巢癌患者。其中75%为浆液性癌,15%为子宫内膜样癌,10%为透明细胞癌。患者每两周接受1或3 mg/kg剂量的纳武利尤单抗(两个10例患者队列),最多接受6个周期(每个周期4次给药)或直到疾病进展为止。研究显示,8例(40%)患者发生了3级或4级治疗相关不良事件。最佳总缓解率为15%,包括两名在3 mg/kg队列中获得持久完全缓解的患者。疾病控制率为45%。研究结束时,中位无进展生存期为3.5个月(95% CI, 1.7-3.9个月),中位总生存期为20个月(95% CI, 7.0个月至未达到)。
此外,pd-l1抑制剂阿维鲁单抗(avelumab)和帕姆珠单抗(pembrolizumab)也显示出相似的活性,缓解率范围为11%至17%,疾病控制率高达65%。目前,这些药物正在进行更大规模的研究。
在动物模型中,联合使用CTLA-4和PD-1阻断剂显示出相加甚至协同的抗肿瘤活性。最近的一项III期研究评估了CTLA-4阻断剂伊匹木单抗与PD-1阻断剂纳武利尤单抗联合治疗黑色素瘤患者的疗效,结果显示,与单独使用其中任何一种药物相比,联合治疗显著提高了缓解率和无进展生存期。这一结果促使美国食品和药物管理局(FDA)最近批准了该联合疗法用于治疗黑色素瘤,尽管这一方案确实伴随着较高的3级毒性发生率。目前,一项由NRG肿瘤组进行的随机II期研究正在比较纳武利尤单抗与帕姆珠单抗联合治疗与单独使用纳武利尤单抗的效果,以确定这种联合疗法在复发性上皮性卵巢癌患者中的疗效和安全性。
36.2.2.3 过继T细胞疗法
过继性细胞疗法(ACTs)依赖于从肿瘤中分离并在体外扩增大量自体肿瘤反应性T细胞。早期研究报道了ACT在上皮性卵巢癌中的显著疗效,尽管这些研究由于选择了能够分离出足够数量TILs的患者,可能存在一定的选择偏差。
更多的研究正在探索ACT在上皮性卵巢癌治疗中的应用。作为替代策略,工程化T细胞技术无需分离TILs。通过这种方法,外周血中的自体淋巴细胞可以被转导以表达特定肿瘤抗原的MHC肽识别T细胞受体或识别肿瘤相关表面抗原的嵌合抗原受体(CAR)。
这些策略在临床前研究中显示出有效性,其中表达MUC16特异性CAR的工程化T细胞已被证明能够完全根除原位卵巢异种移植物。针对这一策略的I期临床研究目前正在开发中。
此外,针对其他卵巢癌相关蛋白如叶酸受体α和间皮素的过继性T细胞转移技术,已有多项I期和II期临床试验正在进行中。
36.2.3 阻断免疫抑制其他路径的治疗策略
尽管早期的临床数据令人鼓舞,但免疫检查点阻断疗法在上皮性卵巢癌中的疗效并不普遍。因此,开发预测性生物标志物和联合疗法显得尤为重要。为了增强疗效,研究者正尝试将PD-1和PD-L1阻断抗体与其他靶向T细胞活化机制的抗体(如糖皮质激素诱导的肿瘤坏死因子受体相关蛋白[GITR]、OX40、4-1BB)以及其他免疫检查点的抗体(如淋巴细胞活化基因[LAG3]和T细胞免疫球蛋白和粘蛋白结构域-3 [TIM3])联合使用。这些策略已经在多种肿瘤类型中进入临床试验。
此外,某些免疫抑制机制与上皮性卵巢癌的不良预后密切相关,包括肿瘤浸润性调节性T细胞(Tregs)、肿瘤相关巨噬细胞(TAMs)、髓源性抑制细胞(MDSCs)以及由肿瘤或基质细胞表达的吲哚胺2,3-双加氧酶(IDO)。因此,联合使用PD-1/PD-L1阻断剂和靶向这些免疫抑制机制的疗法具有合理性。
艾卡哚司他(Epacadostat)是一种口服IDO1抑制剂,目前正在对晚期卵巢癌和三阴性乳腺癌患者进行I/II期临床研究,评估其单药治疗效果以及与免疫检查点抑制剂联合使用的疗效。
36.2.4 单克隆抗体
目前已发现几种与卵巢癌相关的抗原,这些抗原可能成为单克隆抗体(mAbs)的潜在靶点。因此,多个单克隆抗体正在作为这一疾病的新型治疗方法进行开发。其中,靶向CA-125、叶酸受体α和δ样配体4(DLL4)的单克隆抗体正在临床开发中。
36.3 乳腺癌的肿瘤免疫治疗挑战
乳腺癌是全球女性中最常见的癌症。在过去十年中,随着新药物的引入,如化疗药物埃瑞布林、抗HER2化合物(TDM-1、帕妥珠单抗)以及细胞周期抑制剂帕博西尼,乳腺癌的治疗取得了显著进展。然而,晚期和转移性乳腺癌仍然无法治愈,依然是癌症相关死亡的主要原因之一。2012年约有11,800人因乳腺癌去世,中位总生存期仅为2-3年,5年生存率仅为25%。因此,仍然存在对新疗法的迫切需求。
过去,基于乳腺癌肿瘤被认为缺乏免疫原性,研究者对乳腺癌免疫治疗的兴趣一直有限。然而,最新数据显示,乳腺癌,特别是HER2阳性和三阴性乳腺癌,实际上具有免疫原性,并且免疫反应的强度与患者预后密切相关。本文将讨论乳腺癌中免疫治疗药物的最新临床试验结果,包括疫苗、免疫检查点抑制剂以及肿瘤微环境(TME)靶向药物,这些药物在乳腺癌治疗中显示出良好的前景。
36.3.1 疫苗
在过去十年中,几种实验性癌症疫苗已在转移性实体瘤中进行了测试,但这种方法似乎对晚期乳腺癌的效果有限。近年来,癌症疫苗研究出现了范式转变,更常在辅助治疗或癌症早期阶段进行测试。
基于肽的疫苗是研究最广泛的一类,主要靶向过表达、扩增或突变的蛋白质,如HER2、MUC1、CEA、p53、乳腺珠蛋白A和癌-睾丸抗原。
其中,HER2衍生疫苗得到了广泛研究,尤其是E75(neelipepimut-S, NeuVax™)。这是一种由人白细胞抗原(HLA)-A2/A3限制性免疫肽组成的疫苗,源自HER2蛋白的细胞外结构域,目前已进入开发的后期阶段。在辅助治疗中,一项I/II期试验招募了195名HER2阳性患者,结果显示,接种疫苗的患者5年无病生存率为89.7%,而对照组为80.2%,且仅表现出轻微的局部和全身毒性。基于这些令人鼓舞的数据,早期乳腺癌的III期临床研究PRESENT已启动;然而,根据独立数据监测委员会在2016年6月的建议,该试验因未显示出显著疗效而被终止。
36.3.2 免疫检查点
首次免疫治疗临床试验的初步结果显示,某些乳腺癌确实对免疫检查点抑制剂治疗有反应(Table36.1)。
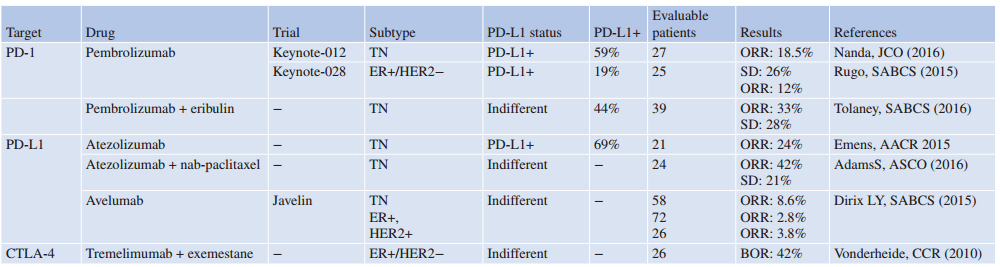
Table 36.1 免疫检查点抑制剂在乳腺癌中的主要结果
36.3.2.1 腔内型乳腺癌
在一项I期研究中,26例患者接受了曲美木单抗(tremelimumab)与依西美坦(一种芳香化酶抑制剂)的联合治疗。虽然未观察到客观反应,但有趣的是,42%的患者疾病得到了至少6周的稳定控制。
在Keynote-028这项多队列I期试验中,25例PD-L1阳性腔内乳腺癌患者接受了抗PD-1药物帕姆珠单抗的治疗。在这群重度治疗的患者中,总缓解率为12%,临床获益率为20%。在JAVELIN研究中,无论患者的PD-L1状态如何,所有患者均接受了阿维鲁单抗(avelumab,一种抗PD-L1药物)治疗。在腔内型乳腺癌队列中,总缓解率(ORR)仅为2.8%。
36.3.2.2 三阴性乳腺癌
Keynote-012是首个报道抗PD-1治疗转移性三阴性乳腺癌临床结果的试验。这项Ib期研究在27例PD-L1阳性患者中评估了帕姆单抗(Pembrolizumab)的疗效。6个月时,帕姆单抗的总体缓解率(ORR)为18.5%,无进展生存期(PFS)为23%。另一种PD-L1抑制剂阿特珠单抗(Atezolizumab)也在这一人群中进行了评估,单药治疗显示出类似的效果。在PD-L1阳性人群中,ORR为24%,6个月时的PFS为27%。在JAVELIN研究中,非选择性人群中阿维鲁单抗(Avelumab)的ORR为8.6%。
目前,检查点抑制剂与化疗的联合使用正在积极探索中。在一项I期临床试验中,联合使用阿特珠单抗与nab-紫杉醇的治疗,无论PD-L1状态如何,ORR均为38%。值得注意的是,超过80%的患者此前曾接受过紫杉烷治疗。基于这些令人鼓舞的数据,IMpassion130这项III期研究目前正在进行中,比较了nab-紫杉醇联合阿特珠单抗与nab-紫杉醇联合安慰剂的一线治疗效果。
在2016年圣安东尼奥乳腺癌研讨会(SABCS)上,Tolaney等人也报道了帕姆利珠单抗(Pembrolizumab)与埃日布林联合治疗的积极结果。在一项Ib/II期研究中,联合治疗在既往接受过治疗的患者中显示出33.3%的ORR。此外,无论PD-L1状态如何,一线治疗患者的ORR为41%。
总体来看,对于这些既往接受过大量治疗且化疗耐药的三阴性乳腺癌患者,这些缓解率可能优于预期。更值得注意的是,当患者出现反应时,这些反应通常是持久的,有时持续超过1年。这种现象在其他背景下的免疫治疗中已有报道,但在此前接受过大量治疗的患者中,化疗通常不会有如此持久的效果。
36.3.2.3 乳腺癌研究的未来方向
预计未来对乳腺癌免疫治疗的研究兴趣将继续增长,许多试验正在评估各种免疫治疗方法,包括单克隆抗体、疫苗、免疫检查点阻断剂,以及基因工程T细胞或免疫调节剂(如细胞因子或Toll样受体(TLR)激动剂)在过继T细胞治疗中的应用。
乳腺癌免疫治疗的成功可能取决于为特定的疾病类型和阶段确定合适的免疫治疗策略。例如,转移性病灶的微环境通常对免疫系统非常不利,免疫抑制性细胞因子和细胞在其中有效地抑制了抗肿瘤免疫反应。尽管研究表明乳腺肿瘤具有一定的免疫原性,但免疫反应并不总是强烈。一项研究报告指出,激素受体阳性乳腺癌中浸润TILs的间质面积中位百分比仅为10%,HER2阳性乳腺癌为15%,而三阴性乳腺癌(TNBC)为20%。由于免疫浸润的缺乏,检查点阻断剂可能无法单独发挥显著的治疗效果。
因此,刺激免疫反应的策略,如使用疫苗或Toll样受体激动剂,可能更有效。这些策略能够激发免疫反应,随后通过检查点阻断剂来增强和维持这种反应,从而为乳腺癌患者带来更好的治疗效果。
结论
近年来,免疫治疗在多种癌症类型中取得了显著进展,乳腺癌和妇科恶性肿瘤也不例外。早期数据显示,免疫检查点抑制剂在这些癌症中展现出希望,表明它们可能成为未来治疗的重要组成部分。然而,这些数据同时表明,检查点抑制剂单独使用并非在所有患者中都有效,这凸显了合理设计治疗组合的必要性。
激活最佳抗肿瘤免疫反应需要针对免疫系统不同组成部分的综合策略。由于免疫逃避机制在患者之间存在差异,治疗方案可能需要个性化设计。通过在临床试验中引入适当的生物标志物,我们可以更精准地为患者选择适合的治疗方法,并为开发和应用联合疗法提供关键信息,从而帮助克服当前的治疗局限性。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 冼金欢
图文排版 | 姚佩言 邓越华
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏