1.CD40激动剂在肿瘤微环境中将调节性T细胞转化为1型效应细胞
Katelyn T. Byrne – Brenden-Colson Center for Pancreatic Care,俄勒冈健康与科学大学,波特兰,俄勒冈州
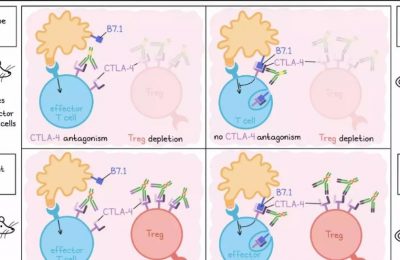
为了更好地了解为什么某些患者对免疫疗法有反应,而其他患者没有,Katelyn Byrne及其同事研究了胰腺癌小鼠模型中的免疫治疗障碍。KP胰腺肿瘤模型显示出高度的Treg浸润,即使在发育的早期阶段,Treg浸润也与PDAC肿瘤中的总Tregs相关。Byrne使用免疫治疗反应模型评估了激动剂抗CD40,该模型在与化疗和/或免疫检查点阻断剂(抗PD-1加抗CTLA-4)联合应用时可以克服抑制性的TME。在用抗PD-1加抗CTLA-4治疗的已确诊肿瘤小鼠中,接着使用激动剂抗CD40,研究人员注意到Tregs迅速减少,并重新分布到肿瘤边界,而常规CD4+ T细胞和CD8+ T细胞仍分散在整个肿瘤中。
在证实这种效应确实是由于激动剂抗CD40而不是免疫检查点阻断之后,研究人员开始研究这种现象背后的机制。由于Tregs不表达CD40,研究小组假设抗原呈递细胞可能起到了作用,并发现DCs和MHC-II是抗CD40介导的Treg减少所必需的。此外,Treg减少还需要IL-12p40、IFNγ和宿主表达的IFNγ受体。接下来,研究人员探索了Tregs是在TME中死亡还是转化。
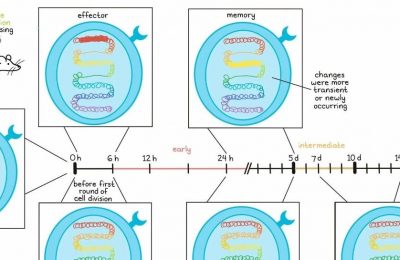
为了研究Treg的转化,研究人员在接受双重检查点阻断和激动剂抗CD40治疗的带瘤小鼠中追踪了Foxp3和Tbet,并观察到ExTregs的数量增加,这些细胞在治疗后失去了Foxp3的表达。通过追踪Foxp3和Tbet的表达,研究人员进一步发现抗CD40诱导的ExTregs获得了IFNγ效应功能,并在治疗后显示出增加的NFAT信号,这表明TCR结合增加。在患者接受激动剂CD40治疗12天后的样本中,Byrne及其同事观察到了与小鼠类似的模式,肿瘤中Tregs减少,Tbet+ Tregs增加,边界区域中的Tregs和Tbet+ Tregs增加。
总之,这些结果表明激动剂抗CD40通过诱导APCs中的变化,将胰腺肿瘤中的Treg重新编程为Th1样ExTregs,从而克服了Treg介导的免疫抵抗,这种现象在患者和小鼠中均有观察到。通过这些结果,Byrne指出了在激动剂抗CD40治疗后重新考虑TME中存在的肿瘤反应性T细胞群的重要性,以及利用Treg可塑性改善患者预后的潜力。
2.针对驱动突变的TCR基因疗法
Eric Tran – 俄勒冈州波特兰市普罗维登斯癌症研究所
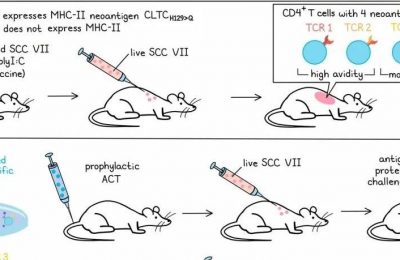
鉴于肿瘤中的驱动突变具有克隆性,并且需要许多驱动基因来维持肿瘤存活和/或生长优势,因此靶向驱动基因突变的TCR在TCR工程性T细胞疗法中可能特别有优势。Eric Tran展示了一位患有胰腺导管腺癌、肺转移的患者接受针对KRAS G12D突变的TCR工程化T细胞治疗的最新数据。患者的T细胞通过两种针对与HLA-C-0802结合的Kras突变9mer和10mer肽的TCR进行工程化,并在IL-2、IL-7、IL-21以及TGFβ存在下扩增,试图诱导组织驻留表型。T细胞产品是携带针对9mer和10mer肽特异性TCR的T细胞的1:2混合物。在输注前,患者接受了抗IL-6抗体,以减轻细胞因子释放综合症(CRS)的严重程度,进行标准淋巴细胞减少,并接受了6次计划剂量中的5次IL-2支持治疗。T细胞输注后6个月,患者肺病灶的RECIST缩小了72%,工程化T细胞约占患者所有循环T细胞的2.5%。该反应持续到1年,但随后患者逐渐恶化,肺病灶需要进一步治疗。
在第二轮工程化T细胞治疗中,患者在T细胞输注前一天开始每两周接受抗PD-1治疗,仅使用携带9mer特异性TCR的T细胞,这是基于额外的体外数据显示该TCR具有更高的亲和力。有趣的是,患者在输注后第4天开始出现2级免疫效应细胞相关神经毒性(ICANs),这在初始输注时并未观察到。ICANs在第9天消失。为了了解ICANs的原因,在第一次和第二次输注后收集的血清样本中进行细胞因子分析,发现一些细胞因子的动力学非常相似,其他细胞因子的差异较小,但与ICANs之间没有明显的关系。已知在某些模型中与神经毒性相关的IL-1β,在ICANs消失后才出现水平差异。IL-8水平在第二次输注后的前5天相对于第一次输注有所增加。IL-8(也称为CXCL8)可以促进中性粒细胞的趋化作用和脱颗粒作用。在ICANs期间,免疫刺激受体CD30的水平也特异性地升高,这可能具有重要意义。
临床上,患者的肿瘤得到稳定(一些明显缩小),根据RECIST,在6个月时维持稳定,但有一些迹象表明出现了进展。在第二次输注后,工程化T细胞的持续性较第一次输注后降低(约为6个月时的0.6%)。为了解释为什么患者在第一次输注后复发,对于进展时切除的肿瘤进行流式细胞术分析,发现工程化T细胞仍存在于肿瘤中,并表达了诸如TIGIT、TIM3、IL-7Rα和CD25等抗原遭遇的标志物。在切除的PET阳性病变中进行免疫组化检查,发现CD3+ T细胞与CD163+巨噬细胞之间存在密切关系。在另一个非PET阳性病变中,发现中性粒细胞靠近大肿瘤细胞,肿瘤细胞似乎活力减弱。需要进一步分析以确定这些中性粒细胞的作用(如果有的话)。总之,了解这位患者复发、毒性和进一步反应的原因可能为未来的TCR工程化T细胞治疗提供重要的见解。
3.剖析肿瘤干细胞逃避T细胞攻击的机制
Judith Agudo – Dana-Farber Cancer Institute,波士顿,MA
为了明确组织干细胞是否真的具有免疫特权的问题,Judith Agudo开发了针对GFP表达细胞的JEDI(just EGFP death-inducing)T细胞。通过用JEDI T细胞处理Lgr5-GFP小鼠,Agudo证明皮肤中的Lgr5+GFP+干细胞确实具有免疫特权,并通过下调MHC I类分子来逃避T细胞介导的杀伤。然而,在肠道中,Lgr5+GFP+干细胞则具有很高的免疫原性,可以轻易被JEDI T细胞清除。相反,具有DNA修复功能的结直肠癌对免疫治疗具有很高的抵抗力,这导致Agudo怀疑这些具有高度免疫原性的肠癌干细胞如何形成冷结直肠癌并规避免疫监视。
通过在受体小鼠的结肠中植入携带突变KrasG12D,p53和APC(AKP)丧失的结肠类器官,并进行数次传代,构建出肿瘤来源的AKP类器官。通过RNAseq和ATACseq发现Sox17上调。Sox17是在胚胎发育过程中参与前肠形成的转录因子,虽然在健康的结肠组织中被沉默,但对结肠癌的发展至关重要。Sox17基因敲除在免疫功能正常的小鼠中显著减少肿瘤生长,但在免疫缺陷小鼠中没有这种作用,表明Sox17在免疫逃逸中可能起作用。
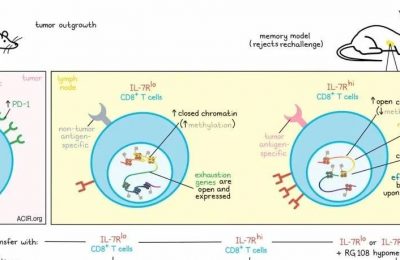
单细胞RNAseq、免疫组化和FACS分析显示,与野生型肿瘤相比,Sox17敲除型中效应类IFNγ+ CD8+ T细胞浸润增加,几乎没有耗竭的CD8+ T细胞。CD8+ T细胞耗竭恢复了Sox17敲除型肿瘤的生长。此外,Sox17丧失诱导了干扰素基因特征的富集,通过上调IFNAR1和MHC I类增加IFNγ信号传导。更多实验表明Sox17直接抑制这些类器官中的IFN受体表达,而IFNGR1的敲除恢复了Sox17敲除型肿瘤的生长。
由于结肠癌起源于腺瘤,研究者将Lgr5-CreERT-GFP小鼠与APCf/f小鼠交叉,以研究Sox17在腺瘤形成中的作用,并发现Sox17在腺瘤中高度表达,但与Lgr5互斥。Sox17的丧失以CD8+ T细胞依赖的方式阻止了腺瘤的形成。在腺瘤中,Sox17抑制Lgr5的表达,Sox17敲除后Lgr5+ MHC I类表达细胞出现扩增。总之,在肠道干细胞中触发类胚胎程序会上调Sox17,进而下调IFNAR1、IFNγ信号和MHC I类以规避免疫监视。一旦肿瘤块和免疫抑制肿瘤微环境形成,某些细胞中又重新开启Lgr5,使得它们形成转移瘤并导致肿瘤复发。
4.肿瘤相关淋巴管及T细胞在肿瘤微环境中的转移
Amanda W. Lund – 纽约大学Langone Health Perlmutter癌症中心,纽约
Amanda Lund讨论了肿瘤中淋巴管的相关性,这是肿瘤微环境中经常被忽视的一个特征。淋巴管朝着淋巴结单向流动,可以对其环境中的信号(如VEGFA、IFNγ)做出动态反应,使它们在肿瘤中发挥多种作用,从肿瘤转移到免疫介导和干细胞生态位的控制。在最近的工作中,Lund及其同事研究了淋巴管如何调节开/关信号以驱动对癌症的免疫应答。
以前的研究发现,在黑素瘤小鼠中,皮肤淋巴管的缺失改善了对免疫T细胞转移的免疫应答。在重复实验中跟踪T细胞时,发现无论淋巴管结构如何,T细胞的激活和初始浸润都相似,但在后期时间点,肿瘤特异性CD8+ T细胞在肿瘤部位的积累增加。有趣的是,这并不是由于增加的增殖,因为这些肿瘤部位的T细胞实际上增殖较少。Lund假设是由于淋巴管结构的缺乏限制了T细胞的外流,使肿瘤特异性和旁观者T细胞在肿瘤部位停留更长时间。
在具有功能性淋巴管结构的小鼠中研究T细胞外流时,Lund及其同事使用了一种光转换小鼠模型。将肿瘤和肿瘤内的内源性细胞从绿色转换为红色,使研究者能够跟踪任何新的浸润或外流细胞。这些研究发现,在光转换后24小时,大量的T细胞,包括大部分CD8+ T细胞,已经从肿瘤中外流,最终进入引流淋巴结。跟踪肿瘤特异性时,研究人员发现外流的T细胞包括许多具有进一步激活能力的功能性肿瘤特异性T细胞,表明淋巴管结构介导了对抗肿瘤的效应细胞的早期退出。
为了探究决定哪些T细胞留下或离开的因素,Lund及其团队比较了留下的和外流的细胞,并发现趋化因子受体谱受到肿瘤内T细胞状态的调节,未激活的T细胞富集在CXCR4中,更容易离开,而激活/抗原经验丰富的T细胞富集在CXCR6中,更容易停留。与此相一致,CXCR4缺陷的CD8+ T细胞的免疫转移抑制了T细胞的退出使得肿瘤更容易得到控制。这些结果支持了一种观点,即根据T细胞是否遇到了抗原,调整T细胞的迁移潜力。
再次审视淋巴管的作用,Lund发现,炎症淋巴管(如肿瘤中的淋巴管)表达CXCL12(CXCR4的配体),将非活化的CD8+ T细胞从肿瘤中吸引出来。通过敲除CXCL12证实了这一点,这导致了从肿瘤周围到肿瘤中心的CD8+ T细胞的显著重新分布,增强了CD8+ T细胞介导的肿瘤控制。Lund希望进一步研究这些机制,并希望利用它们开发出相应的免疫疗法,以增强肿瘤特异性效应T细胞在肿瘤内的保留。
5.一种用于治疗复发/难治性多发性骨髓瘤患者的具有低CD3亲和力的BCMAxCD3双特异性抗体的1/2期安全性和有效性临床试验
Attaya Suvannasankha – 印第安纳大学西蒙癌症中心和Roudebush VAMC,印第安纳波利斯,印第安纳州
为了给接受过多种治疗后必然复发的多发性骨髓瘤患者提供治疗选择,Attaya Suvannasankhha展示了一项关于一种新型双特异性T细胞结合抗体REGN5459的I期剂量递增试验结果,该抗体能结合BCMA和CD3。这种完全人源化抗体(来源于Veloci-Bi™小鼠)经过工程设计,其对CD3的亲和力低于其他典型的T细胞结合剂。在临床前模型中,REGN5459激活了T细胞并以低细胞因子释放的方式减少了浆细胞。试验中的43名患者均接受过大量治疗,没有其他可用选择。
最初的逐步升级剂量在前两到三周进行,以减轻细胞因子释放综合症(CRS),这在其他双特异性抗体中常见,接着是每周给药直到第16周,然后改为每两周给药。患者预先用地塞米松和可选择的扑热息痛和/或抗组胺药进行治疗。当完全剂量被良好忍受时,预先给药逐渐减少,然后停止。剂量递增阶段确定了第二阶段的推荐剂量(RP2D)为480毫克,用于扩展队列评估总体反应。最大耐受剂量(MTD)未达到。约63%的患者发生感染,其中约30%的患者为高级感染。
细胞因子释放综合症(CRS)是最常见的与治疗相关的不良事件,其发生频率随剂量增加,但严重程度没有增加。16%的患者因不良事件停止治疗。反应率随剂量增加而增加,在最高剂量(RP2D和一名900毫克的患者)时,91%的患者出现了反应,其中62%为完全反应。反应较早出现,中位反应时间为0.8个月。在9个月的中位随访时间内,未达到中位反应持续时间,截至数据停止收集,最长的反应持续26+个月。

加入读者交流群~
(添加请备注单位姓名)

关注本号~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏