前期精彩内容:
Cancer Cell:通过mRNA技术编码持久性IL-2在MHC I类分子缺陷癌症中可恢复针对新抗原的CD8+ T细胞反应
杂志名称:Nat Commun.
发表日期:2024.03.18
DOI:10.1038/s41467-024-46769-9.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38499573/
影响因子:16.6
内容简介
免疫检查点抑制剂(ICI)的潜力可能在免疫细胞健康受损的情况下受到限制。研究表明,由于在小鼠中和治疗诱导的细胞衰老(TIS)背景下积累的衰老细胞,癌症免疫治疗的效果受到了影响。对免疫治疗的抗性与肿瘤内CD8 T细胞的积累和激活减少相关。消除衰老细胞可以恢复肿瘤微环境(TME)内的免疫稳态,并增加小鼠对免疫治疗的生存反应。通过使用单细胞转录组分析,观察到ABT263(Navitoclax)注射可以逆转TME中髓系细胞的加剧的免疫抑制性特征。这些髓系细胞的消除也在体外恢复了CD8 T细胞的增殖,并在体内消除了对免疫治疗的抗性。总的来说,该研究表明,在ICI治疗前使用清除衰老细胞的药物可能构成一种药理学方法,以提高癌症免疫治疗的有效性。
创新性及研究意义
这篇文章的核心创新性在于揭示了细胞衰老(senescence)在诱导免疫治疗抗性中的关键作用,并通过实验证明了消除衰老细胞能够恢复肿瘤微环境(TME)中的免疫稳态,从而增强免疫治疗的效果。研究显示,在小鼠模型中,衰老细胞的积累与免疫治疗的抗性密切相关,这主要体现在肿瘤内CD8 T细胞的积累和激活减少上。
研究意义方面,这项工作为癌症免疫治疗领域提供了新的视角和干预手段。通过使用清除衰老细胞的药物ABT263(Navitoclax),能够逆转髓系细胞的免疫抑制性特征,恢复CD8 T细胞的增殖能力,并在体内有效克服对免疫治疗的抗性。这为提高癌症免疫治疗的有效性提供了一种潜在的药理学策略,即在免疫检查点抑制剂(ICI)治疗前使用清除衰老细胞的药物,从而增强治疗效果,对于癌症治疗具有重要的临床意义。
数据图
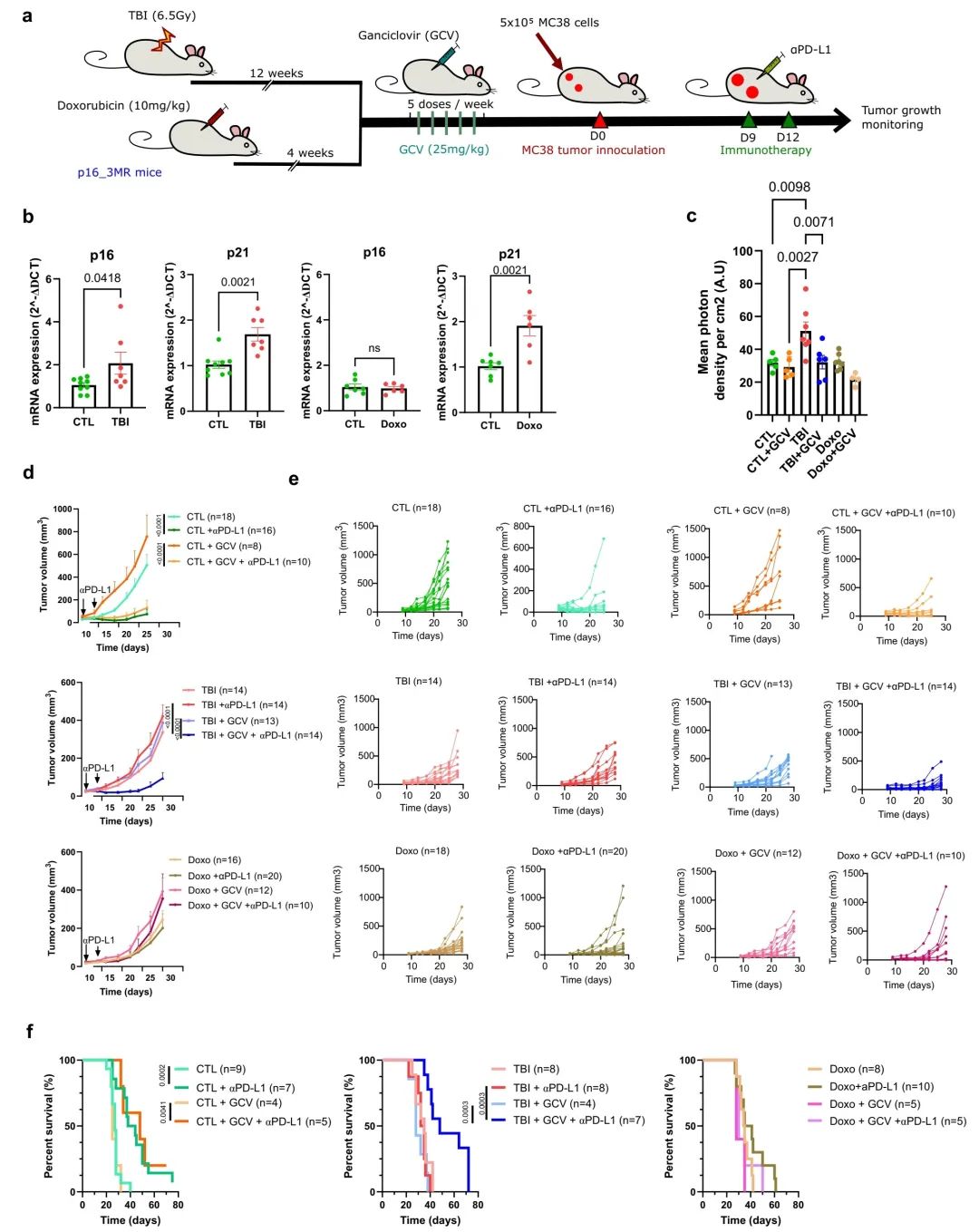
图1:衰老导致免疫疗法抗性增强
a 实验示意图。简要来说,通过给p16-3MR小鼠施加一次6.5 Gy的次致死剂量全身照射(TBI)或注射多柔比星(Doxo,10mg/kg)来诱导衰老。在TBI后12周或多柔比星注射后4周,小鼠通过腹腔注射GCV(25mg/kg)连续5天,以清除衰老细胞。在最后一次注射GCV后5天,小鼠在每侧胁部分别注射5×105个表达mPlum荧光蛋白的MC38肿瘤细胞。在第9天和第12天,对小鼠注射αPD-L1阻断抗体,并持续观察肿瘤生长直至达到限制点。
b 通过RT-qPCR定量测定了TBI或多柔比星处理后10周和4周脾脏中p16和p21的相对表达量。CTL组9个样本,TBI组6个样本;Doxo组分别为7个和6个独立动物样本。Doxo组采用双尾非配对T检验进行p16/p21的统计,而TBI组采用Mann-Whitney检验。数据以均值±SEM显示。
c 在GCV处理前后,通过生物发光测量p16-3MR小鼠脾脏中p16的表达。CTL组5个样本,CTL+GCV组5个样本,TBI组7个样本,TBI+GCV组6个样本,Doxo组7个样本,Doxo+GCV组4个独立动物样本。采用普通单向ANOVA分析并进行Tukey校正。数据以均值±SEM显示。
d 展示了CTL小鼠25天内及TBI/Doxo小鼠28天内的平均肿瘤生长量±SEM。未经TBI或Doxo处理的对照小鼠标记为CTL。括号内显示每组的肿瘤总数。采用混合效应分析或双向ANOVA分析并进行Tukey校正。
e 展示了所指时间点每个单独肿瘤的大小。括号内显示每组的肿瘤总数。
f CTL、TBI和Doxo小鼠在各指定条件下的Kaplan-Meyer生存曲线。括号内显示每组的小鼠总数。采用Log-rank (Mantel-Cox检验)。
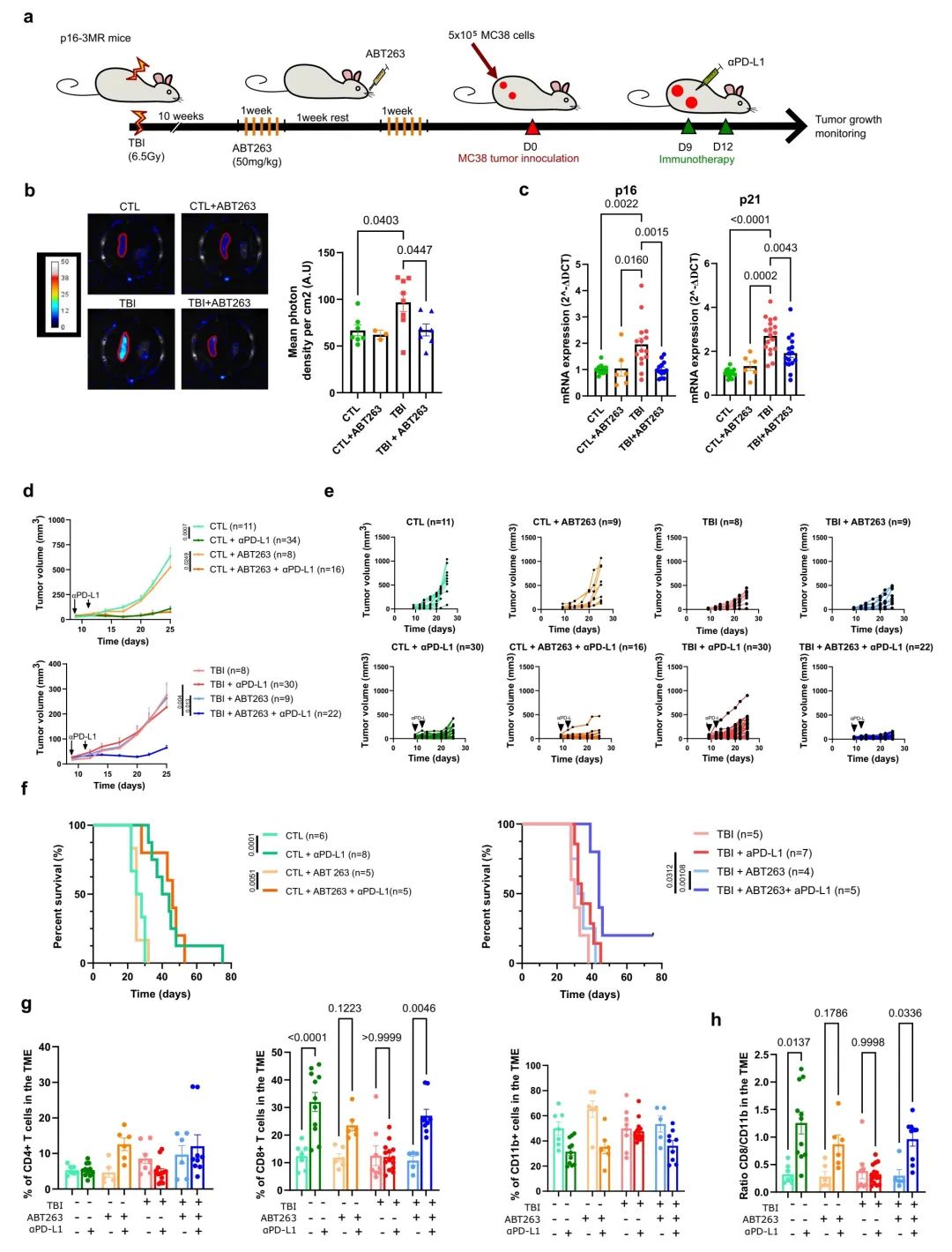
图2:使用ABT263治疗消除衰老细胞改善了受照射小鼠的αPD-L1癌症免疫疗法效果
a 实验示意图。简要来说,通过次致死剂量的TBI诱导衰老,10周后小鼠通过胃管灌注接受ABT263(50 mg/kg)治疗,分两个周期,每个周期连续5天,以清除衰老细胞。最后一次灌注后5天,小鼠要么被牺牲以外部测量脾脏中的衰老情况,要么注射MC38肿瘤细胞。
b 通过生物发光技术评估ABT263处理前后脾脏中p16表达。数据以均值 ± SEM显示。CTL组7个样本,CTL + ABT263组3个样本,TBI组8个样本,TBI + ABT263组7个独立动物样本。采用普通单向ANOVA分析并进行Tukey校正。
c 通过qPCR技术评估ABT263处理前后脾脏中p16和p21的表达。CTL组11个样本,CTL + ABT263组6个样本,TBI组15个样本,TBI + ABT263组13个独立动物样本。采用普通单向ANOVA分析并进行Tukey校正。数据以均值 ± SEM显示。
d 评估各指定小鼠组的肿瘤生长。每条线代表25天内或直至必须从研究中移除该小鼠为止的肿瘤平均生长量 ± SEM。括号内显示每组的肿瘤总数。采用混合效应分析或双向ANOVA分析并进行Tukey校正。
e 展示了所指时间点每个单独肿瘤的大小。未经TBI处理的小鼠标记为对照组(CTL)。括号内显示每组的肿瘤总数。
f 展示了对照组和TBI小鼠在各指定条件下的Kaplan–Meyer生存曲线。采用Log-rank (Mantel-Cox检验)。
g 在接种后第14天,通过流式细胞术分析肿瘤解离后的肿瘤免疫细胞浸润情况。数据显示CD45+细胞群中CD4 T细胞、CD8 T细胞和CD11b+细胞的比例。CTL组7个样本,CTL (αPD-L1)组11个样本,CTL + ABT263 (αPD-L1)组共12个样本,TBI组8个样本,TBI (αPD-L1)组14个样本,TBI + ABT263 (αPD-L1)组共14个样本。采用普通单向ANOVA分析并进行Tukey校正。数据以均值 ± SEM显示。
h 展示了肿瘤中CD8 T细胞与CD11b+细胞的比例。数据来源同g。采用Brown-Forsythe和Welch ANOVA分析并进行Games-Howell校正。数据以均值 ± SEM显示。
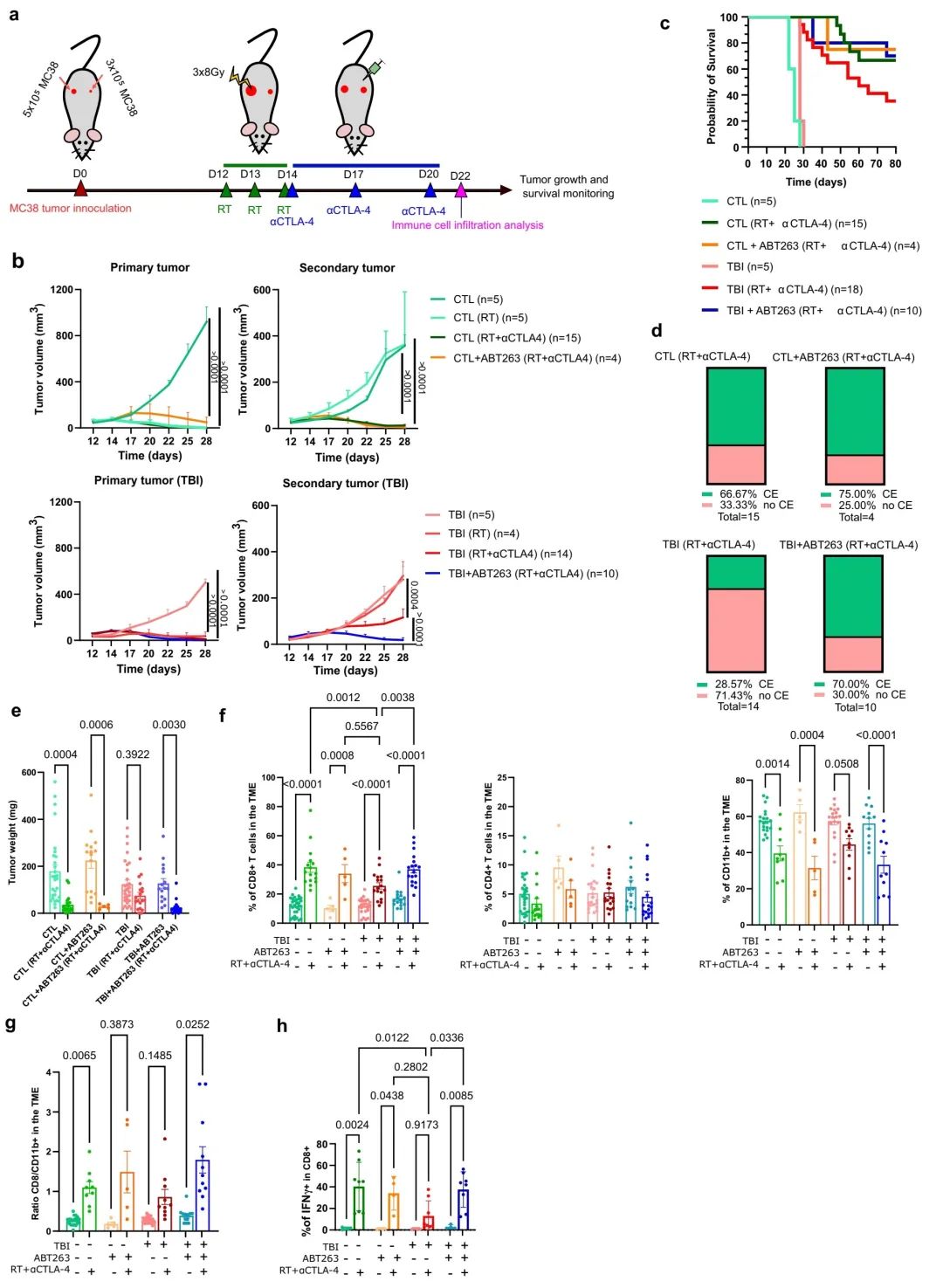
图3:ABT263恢复了之前受照射小鼠中受损的远端杀伤效应
a 实验示意图。经或未经ABT263处理的CTL或TBI小鼠在每侧胁部接种了3或5 × 105个MC38肿瘤细胞。在肿瘤接种后的第12、13和14天,对较大的原发性肿瘤进行了3轮(每轮8Gy)的放射治疗(RT)。然后在第14、17和20天给小鼠注射αCTLA-4阻断抗体,并评估肿瘤生长直至达到限制点。另外,一些小鼠在第22天被安乐死,并手术移除肿瘤以分析免疫浸润。
b 评估了各指定小鼠组的肿瘤生长。每条线代表一个单独肿瘤在28天内或直到必须将小鼠从研究中移除为止的生长情况。括号内显示每组的肿瘤总数。采用双向ANOVA分析并进行Tukey校正。数据以均值 ± SEM显示。
c 为每种指定条件绘制的Kaplan–Meyer生存曲线。
d 直方图显示了每组中实现完全的次生(远隔)肿瘤消除(CE)的小鼠比例。
e 展示了第22天在解离前的次生肿瘤重量。CTL组29个样本,CTL (RT + αCTLA4)组17个样本,CTL + ABT263组15个样本,CTL + ABT263 (RT + αCTLA4)组5个样本,TBI组29个样本,TBI (RT + αCTLA4)组19个样本,TBI + ABT263组16个样本,TBI + ABT263 (RT + αCTLA4)组19个独立动物样本。采用Brown-Forsythe和Welch ANOVA检验并进行Games-Howell校正。数据以均值 ± SEM显示。
f 在接种后第22天,通过流式细胞术从解离的肿瘤中确定肿瘤免疫细胞浸润情况。展示了CD8 T细胞、CD4 T细胞和CD11b+细胞相对于从肿瘤中收集的CD45+细胞总数的比例。对于CD8和CD4,CTL组29个样本,CTL (RT + αCTLA4)组17个样本,CTL + ABT263组及CTL + ABT263 (RT + αCTLA4)组共10个样本,TBI组24个样本,TBI (RT + αCTLA4)组17个样本,TBI + ABT263组及TBI + ABT263 (RT + αCTLA4)组共34个独立动物样本。对于CD11b,数据来源同上。采用普通单向ANOVA分析并进行Tukey校正。数据以均值 ± SEM显示。
g 展示了第22天肿瘤中CD8 T细胞与CD11b+细胞的比例。数据来源同f。采用Brown-Forsythe和Welch ANOVA分析并进行Games-Howell校正。数据以均值 ± SEM显示。
h 展示了第22天浸润CD8 T细胞中IFNγ表达的定量,通过流式细胞术测量。CTL组4个样本,CTL (RT + αCTLA4)组8个样本,CTL + ABT263组及CTL + ABT263 (RT + αCTLA4)组共8个样本,TBI组4个样本,TBI (RT + αCTLA4)组8个样本,TBI + ABT263组4个样本,TBI + ABT263 (RT + αCTLA4)组8个独立动物样本。采用普通单向ANOVA分析并进行Tukey校正。数据以均值 ± SEM显示。
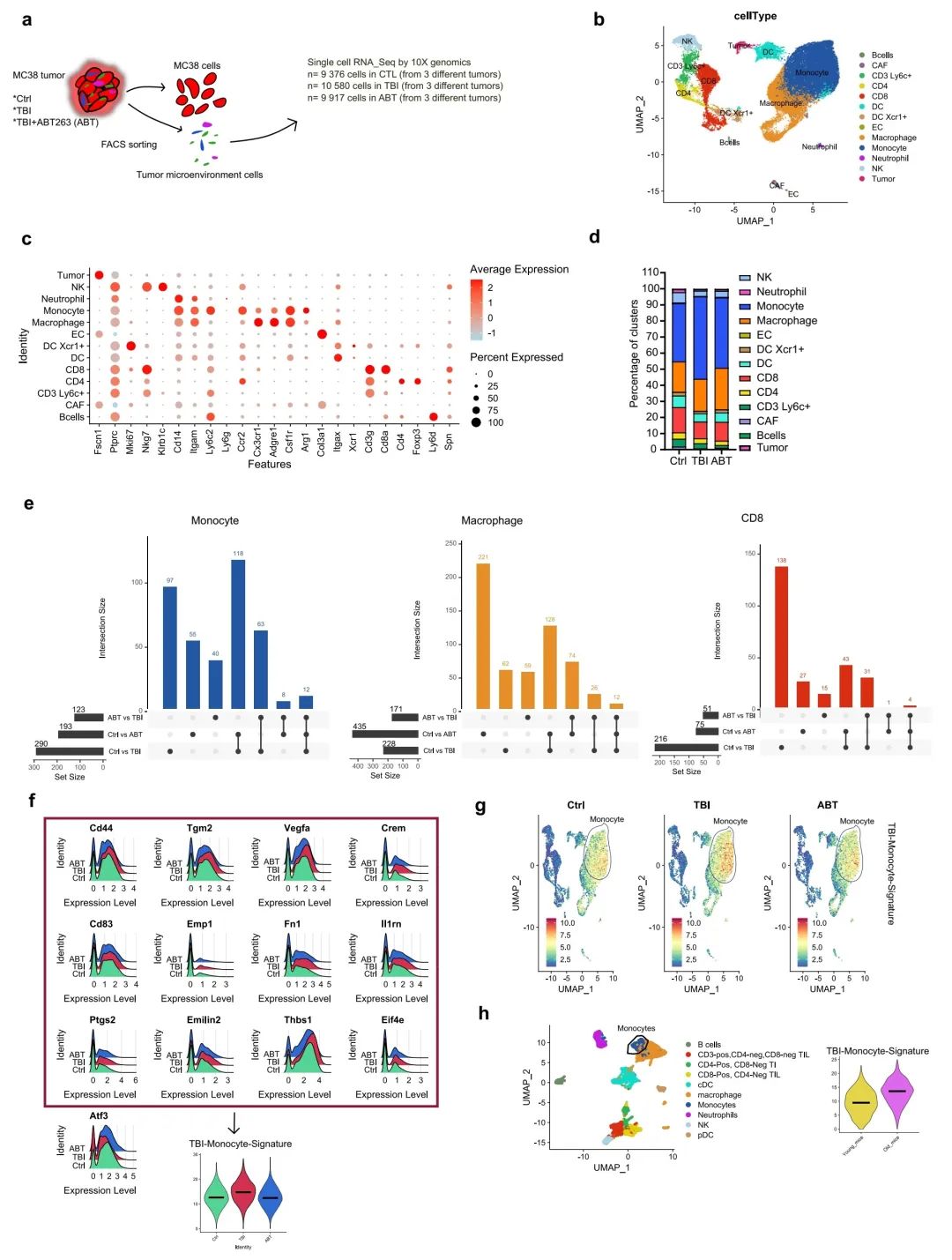
图4:ABT263治疗后,单核细胞的免疫抑制表型部分恢复
a 在接种后第22天收集指定小鼠组的肿瘤并进行解离。非肿瘤生成细胞(称为肿瘤微环境细胞)被分选并用于两个独立实验的单细胞转录组分析。每组包含来自三个肿瘤的细胞池。每组分析了大约10000个细胞。
b 通过R-studio中的Seurat包,生成了12个不同的簇,代表了肿瘤微环境(TME)中几乎所有的细胞,这些簇通过U-MAP表示定位。
c 展示了一个DotPlot,列出了用于识别b面板中生成的细胞簇的基因表达情况。
d 展示了从所有分析细胞中单个细胞群体的比例。
e UpsetPlot显示了在单核细胞、巨噬细胞和CD8 T细胞样本比较后的交互作用大小(差异表达基因的数量)。
f 在ABT处理的小鼠中恢复表达的单核细胞簇中的63个基因中,根据它们与免疫抑制/免疫疗法抗性的关联选择了13个。它们的个体表达情况通过RidgePlot展示,以演示这些单核细胞的整体免疫抑制表型。过表达基因的全局表达(不包括Atf3)构成了TBI-单核细胞-特征,并通过ViolinPlot表示。
g 在f面板中识别的TBI-单核细胞-特征在整个细胞中通过FeaturePlot进行量化,以突出在b面板中定义的单核细胞簇内的表达。
h 使用Zhang等人在老龄(20-22个月大)和年轻(6-8周大)小鼠中收集的B16F10肿瘤中生成的单细胞数据集,通过小提琴图分析TBI-单核细胞-特征在单核细胞中的表达情况。
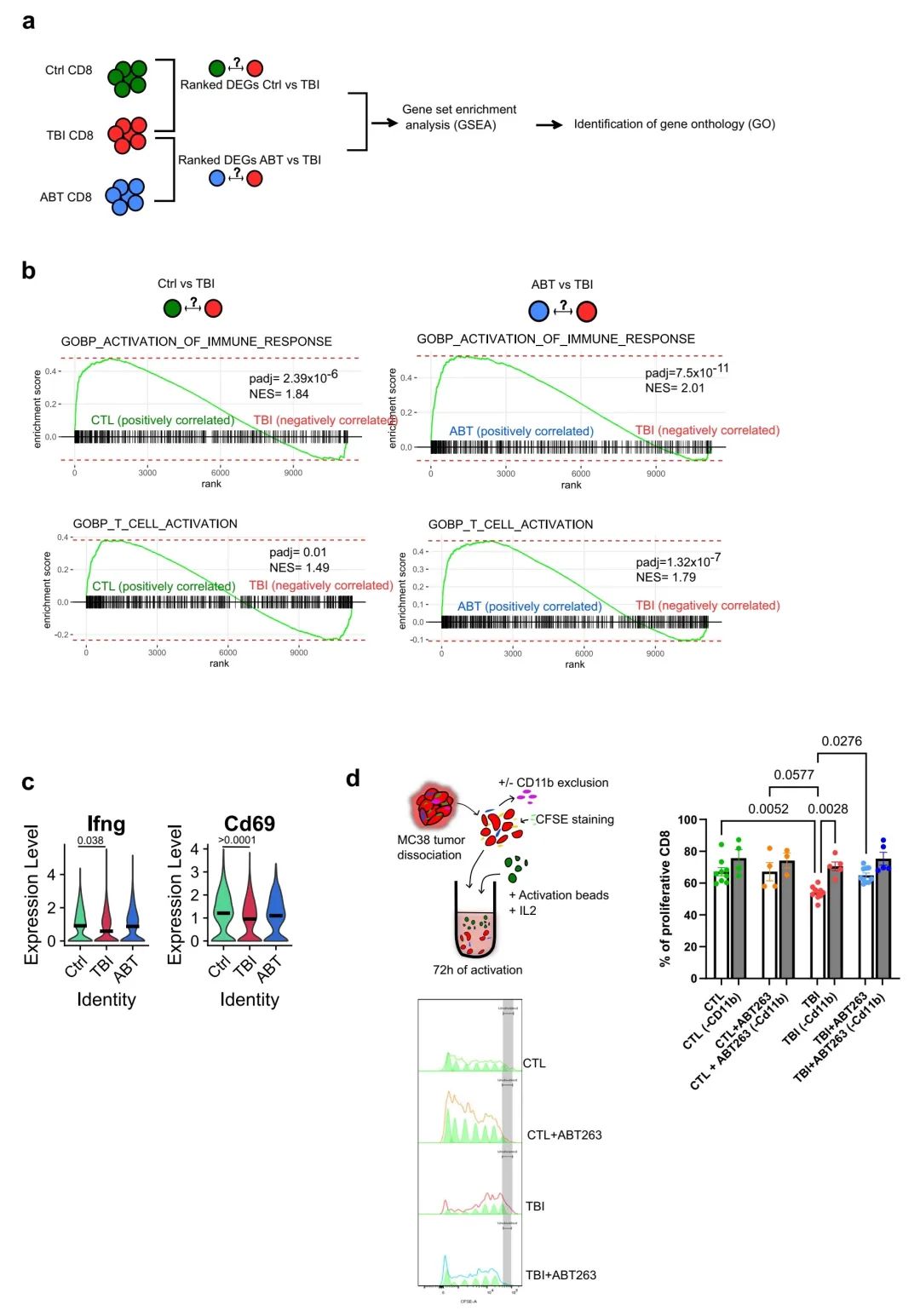
图5:ABT263可部分恢复单核细胞介导的CD8 T细胞激活和增殖受损
a 利用fgsea包对我们的CD8 T细胞RNA转录组数据进行基因集富集分析(GSEA),以识别富集的基因本体(GO)。CTL组中有1421个CD8 T细胞(来自三个不同肿瘤),TBI组中有1073个CD8 T细胞(来自3个不同肿瘤),ABT组中有1072个CD8 T细胞(来自三个不同肿瘤)。
b 展示了CD8 T细胞GSEA的富集图及统计信息(调整后的p值或padj,以及标准化富集得分或NES),针对选定的特定GO:T细胞激活和免疫应答激活。
c 小提琴图展示了CD8 T细胞中Ifnγ和Cd69效应器标志物的转录组表达。使用FindMarkers函数和Wilcoxon秩和检验。CTL组中有1421个CD8 T细胞(来自三个不同肿瘤),TBI组中有1073个CD8 T细胞(来自3个不同肿瘤),ABT组中有1072个CD8 T细胞(来自三个不同肿瘤)。
d 示意图表示在激活珠刺激下,来源于指定组的肿瘤微环境中,有或没有髓系细胞(CD11b+)的CFSE染色CD8 T细胞的体外增殖能力。使用FlowJo软件和增殖工具评估增殖性CD8 T细胞的百分比。CTL组9个样本,CTL (-CD11b)组4个样本,CTL + ABT263组4个样本,CTL + ABT263 (-CD11b)组4个样本,TBI组11个样本,TBI (-CD11b)组5个样本,TBI + ABT263组10个样本,TBI + ABT263 (-CD11b)组5个样本。采用普通单向ANOVA分析并进行Tukey校正。数据以均值 ± SEM显示。
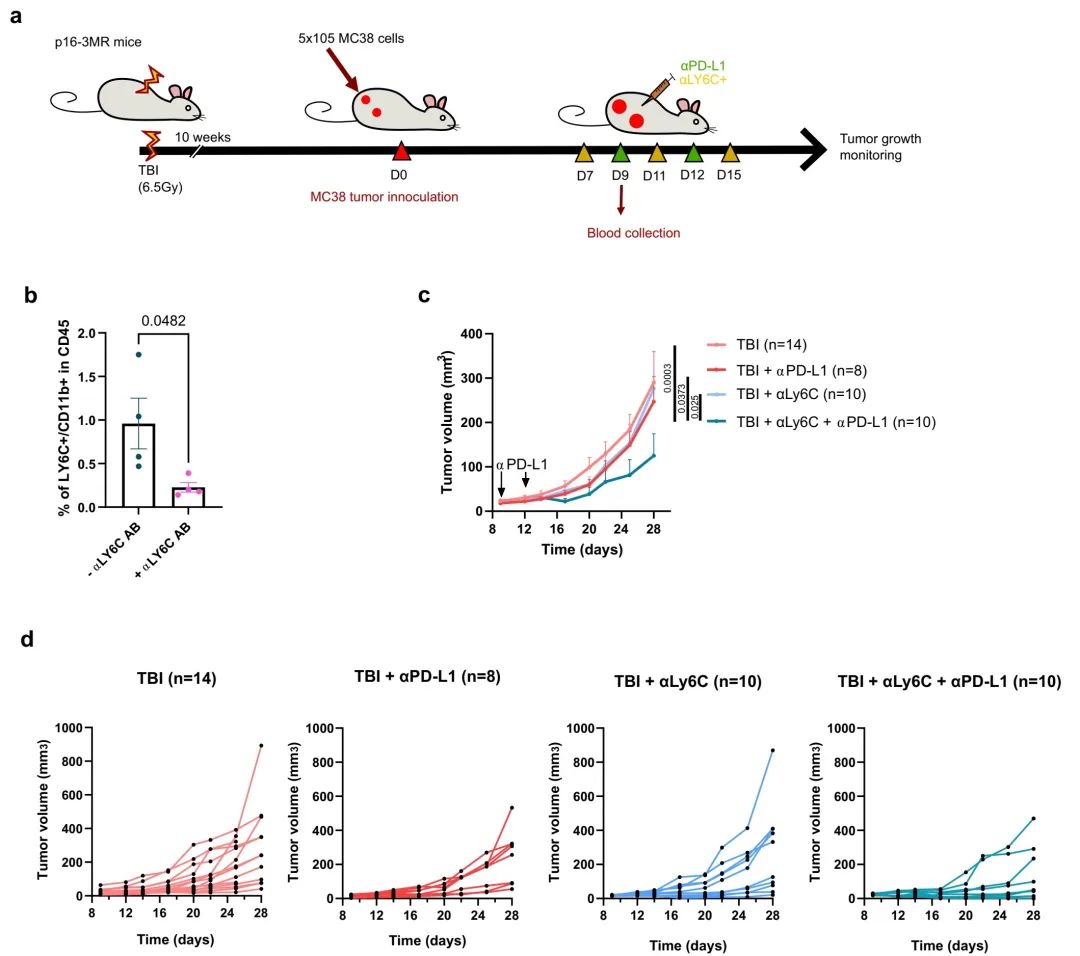
图6:清除Ly6c+髓系细胞部分克服了对αPD-L1的抵抗
a 实验示意图。简要来说,p16-3MR小鼠在每侧胁部注射了5 × 10^5个表达mPlum荧光蛋白的MC38肿瘤细胞。小鼠在第7、11和15天通过腹腔注射接受αLy6c阻断抗体,并在第9和12天接受αPD-L1阻断抗体。
b 展示了αLy6c抗体第一次注射后两天(肿瘤接种后第9天)通过流式细胞术测量的CD45+细胞群中CD11b+/Ly6c+细胞的比例。n = 4个独立动物。采用两个非配对的T检验。数据以均值 ± SEM显示。
c 评估了各指定小鼠组的肿瘤生长。每条线代表28天内或直到必须将小鼠从研究中移除为止的平均肿瘤生长。括号内显示每组的肿瘤总数。采用2way ANOVA或混合效应分析并进行Tukey校正。数据以均值 ± SEM显示。TBI组与图1d中的相同,此处再次显示以便比较。
d 展示了所指时间点每个单独肿瘤的大小。括号内显示每组的肿瘤总数。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏