35.3 肿瘤疫苗
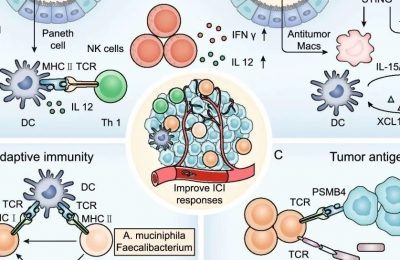
免疫检查点阻断通过降低抑制性免疫信号来增强现有的肿瘤免疫应答,而疫苗的作用机制则有所不同,其目的是激发并诱导新的抗肿瘤免疫反应。疫苗的主要作用在于抗原提呈细胞(如树突状细胞,DCs)的水平。DCs摄取并处理抗原,然后将其与增强CD8 T细胞应答的共刺激分子一起提呈给细胞毒性CD8 T细胞。这些T细胞识别MHC分子背景下呈递的小肽片段,通过其T细胞受体(TCR)识别抗原,从而激活T细胞。活化后的CD8 T细胞会增殖、广泛迁移,并能够特异性地攻击表达其同源肽/MHC配体的靶细胞。
树突状细胞是最有效的抗原提呈细胞(APC),因为它们不仅能够启动初始T细胞反应,还能响应固有免疫信号,协调整体免疫反应。因此,癌症疫苗通常包含一种佐剂和一种肿瘤特异性肽或蛋白,佐剂的作用是激活树突状细胞,使其能够有效地向T细胞呈递抗原并提供必要的共刺激信号。
前列腺癌由于表达多种特异性肿瘤抗原,如前列腺酸性磷酸酶(PAP)、前列腺特异性膜抗原(PSMA)和前列腺特异性抗原(PSA),成为疫苗开发的理想候选对象。这些抗原主要在前列腺中高表达,因此通过疫苗强有力地激活T细胞,可以在理论上降低误伤其他组织的风险。此外,患有转移性前列腺癌的男性通常已接受了放疗或手术的初步治疗,因此在这些患者中,前列腺抗原的唯一来源可能就是肿瘤本身,使得疫苗的靶向性更为明确。
美国FDA批准的唯一用于治疗实体瘤的疫苗是Sipuleucel-T,这是一种由患者自身细胞制备的树突状细胞疫苗。其制备过程包括分离患者的单核细胞,并将这些细胞与由前列腺酸性磷酸酶(PAP)和粒细胞-巨噬细胞集落刺激因子(GM-CSF)组成的融合蛋白共培养,从而诱导单核细胞成熟为树突状细胞,并激活这些细胞,将PAP作为靶抗原。当这些被激活的树突状细胞回输到患者体内后,抗原被呈递到MHC I和II分子上,从而潜在地诱导细胞毒性T细胞反应,并促进体液免疫效应的产生。
在前列腺腺癌免疫治疗研究(IMPACT)中,数据显示接受Sipuleucel-T治疗的患者的平均总体生存期(OS)延长了4.1个月,Sipuleucel-T组的OS为25.8个月,而安慰剂组为21.7个月。然而,接受治疗的患者中,仅有2.6%的人PSA水平下降超过50%。此外,这些患者不仅血清中针对PAP的抗体显著增加,还对其他抗原如LGALS3和ECE1(已知在原发肿瘤中表达的抗原)的抗体也显著增加。这种现象被称为“抗原扩散”,可能是由于免疫介导的癌细胞攻击导致在促免疫原性环境中释放额外抗原所引发的。
尽管Sipuleucel-T在III期试验中表现出疗效,但另一种用于前列腺癌的疫苗在III期试验中的结果却不尽如人意。GVAX前列腺疫苗是一种全细胞疫苗,由两个肿瘤细胞系(PC3和LNCaP)组成,这些细胞系经重组病毒载体转导后能够分泌GM-CSF。2006年,一项在mCRPC患者中比较GVAX前列腺疫苗与化疗的随机III期试验招募了约600名患者。需要注意的是,与Sipuleucel-T试验或正在进行的Prostvac-VF III期试验(见下文)不同,这项试验使用了多西他赛化疗作为活性对照,而多西他赛化疗在mCRPC中具有明确的临床益处。然而,由于无效性分析(futility analysis)显示达到试验主要终点的概率低于30%,该试验提前终止。
尽管如此,目前仍在进行GVAX与其他治疗联合应用的研究,包括在II期试验中将其与新辅助激素治疗相结合的研究 (Table 35.2)。
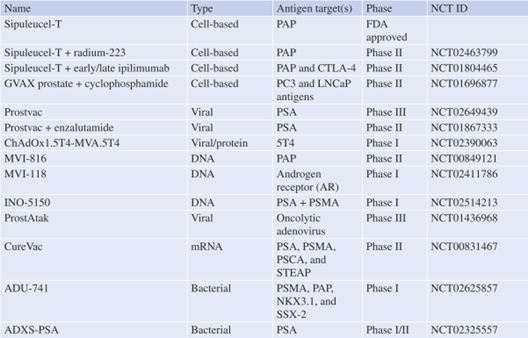
Table 35.2 入选临床试验的前列腺癌疫苗名称
另一种正在研发的前列腺癌疫苗是Prostvac-VF(由Bavarian Nordic公司开发,位于北卡罗来纳州Morrisville),这是一种两部分组成的病毒疫苗,包括初次接种(Prostvac-V)和加强接种(Prostvac-F),其主要靶向抗原是前列腺特异性抗原(PSA)(Table 35.2)。此外,Prostvac-VF还包含TRICOM™,这是一种共刺激分子组合(B7.1、ICAM-1和LFA-3),旨在增强抗原提呈细胞(APC)的抗原呈递能力。
Prostvac-VF在Ⅱ期试验中未能达到预设的无进展生存期(PFS)终点,但事后分析显示,在3年随访时,该疫苗似乎将总体生存期延长了8.5个月,从16.6个月延长至25.1个月。目前,Prostvac联合GM-CSF治疗mCRPC患者的Ⅲ期试验正在进行中(Table 35.2)。这项生存期试验将1,200名未接受化疗的mCRPC男性患者随机分为三组,分别接受安慰剂、Prostvac-VF联合皮内GM-CSF或Prostvac-VF联合安慰剂(NCT01322490)。该试验排除了内脏转移的患者。虽然患者的招募已经完成,但最终结果尚未公布。此外,Prostvac与抗CTLA-4以及其他药物的联合试验也在进行中,初步结果显示,30名患者中有14名的PSA水平有所下降。
DNA疫苗是另一项用于前列腺癌的技术,正在进行I期和II期临床试验。通常,这些疫苗由编码靶向抗原的细菌质粒构成;当通过肌肉注射给患者后,编码的蛋白质通过宿主细胞的转录机制表达。这些抗原随后被树突状细胞处理和呈递,可能导致淋巴细胞的动员和激活。此外,细菌质粒上的低甲基化CpG基序能够激活多种免疫细胞的病原体识别受体,如TLR9和cGAS,包括树突状细胞、B细胞和自然杀伤(NK)细胞。这些受体下游的信号传导级联反应引发促炎效应,包括GM-CSF的产生以促进单核细胞的成熟,以及I型干扰素的产生以增强B细胞和T细胞的活化。
如前所述,前列腺癌细胞表达一组共同的肿瘤抗原,因此它们是DNA疫苗的理想候选。针对前列腺癌,已有多种DNA疫苗开发完成并处于不同的临床试验阶段。最具进展的是MVI-816(由麦迪逊疫苗公司开发,位于威斯康星州麦迪逊),这是一种编码PAP的DNA疫苗,目前正在进行Ⅱ期试验。在这项试验中,非转移性前列腺癌患者被随机分组,分别接受MVI-816联合GM-CSF治疗或单独接受GM-CSF治疗,主要终点是无转移生存期(NCT01341652)。
由于晚期癌症患者的肿瘤特异性T细胞亚群可能表达高水平的PD-1,因此仅靠DNA疫苗可能不足以有效激活这些耗竭的T细胞。因此,在一项针对mCRPC患者的I期试验中,MVI-816正在与PD-1抑制剂帕博利珠单抗联合使用,主要终点包括客观缓解率、无进展生存期、不良事件发生率、影像学进展时间和PSA缓解率 (Table.35.1)。
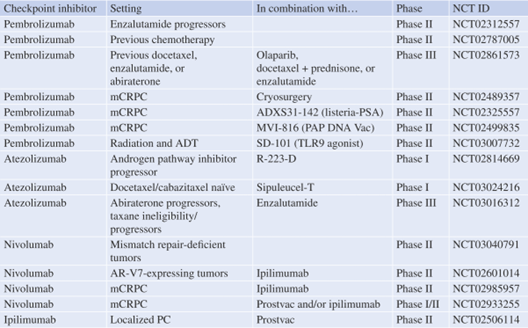
Table 35.1 前列腺癌的免疫检查点阻断试验
另一种引人注目的DNA疫苗策略靶向前列腺特异性膜抗原(PSMA)和前列腺特异性抗原(PSA)。这种疫苗的独特之处在于,它并不编码天然蛋白质,而是编码经过轻微修改的版本,这些版本与天然抗原相比在自然界中更具异种性,从而增强对天然抗原的免疫反应。这款DNA疫苗名为INO-5150(由Inovio公司开发,位于宾夕法尼亚州Plymouth Meeting),目前正在进行Ⅰ期临床试验,单独使用或与其细胞因子佐剂IL-12质粒INO-9012联合使用。试验的主要目标是评估疫苗的安全性和抗原特异性应答 (Table 35.2)。该试验的目标患者是早期前列腺癌患者,即在初次手术或放疗后PSA升高的患者。目前,患者招募工作已经完成,免疫监测数据尚待公布。
另一种更直接的疫苗接种方法是通过肿瘤内注射免疫原性物质,以增强原位肿瘤的免疫原性。其中一种疫苗ProstAtak(由Advagene公司开发,位于马萨诸塞州奥本代尔)目前正在前列腺癌的Ⅲ期开发阶段 (Table 35.2)。这款疫苗由一种减毒的腺病毒组成,将疱疹病毒衍生的胸苷激酶(tk)基因注射到肿瘤内,导致肿瘤细胞表达该基因。这使得这些细胞对标准抗病毒药物伐昔洛韦(由葛兰素史克公司开发,位于英国米德尔塞克斯)非常敏感。药物给药会导致感染的肿瘤细胞死亡,同时释放肿瘤抗原。虽然FDA已批准一种用于治疗黑色素瘤的瘤内疫苗,但在前列腺癌中进行反复的瘤内注射增加了操作复杂性。
另一种疫苗策略是利用高静水压力(HHP)使肿瘤细胞失活,从而保留其抗原性。在小鼠模型中,当树突状细胞暴露于这些HHP失活的肿瘤细胞时,IL-12的产生和成熟标志物的表达增加,效果优于暴露于辐射灭活肿瘤细胞的树突状细胞。此外,当这种疫苗与多西他赛联合用于免疫原性较低的小鼠TRAMP-C2肿瘤时,结果显示肿瘤生长减缓且生存率提高。
基于mRNA的疫苗CV9104(由CureVac公司开发,位于德国图宾根)将免疫刺激性鱼精蛋白与编码PSA、PSMA、PSCA和STEAP的mRNA结合 (Table 35.2)。mRNA疫苗具有减少构建体整合入宿主基因组的风险,这在使用DNA疫苗时可能是一个问题。尽管Ⅰ期和Ⅱa期试验的初步结果令人鼓舞,但在Ⅱb期试验中,与安慰剂相比,该疫苗未能显著改善总体生存期和无进展生存期。
使用灭活细菌进行疫苗接种是最古老的疫苗接种形式之一,并且在抗肿瘤免疫中也有应用。其中一种特别引人注目的疫苗载体是阳性细菌单核细胞增生李斯特菌(Lm)。Lm可以直接感染抗原提呈细胞,促使其表达抗原并通过I类MHC分子进行呈递。因此,基于Lm的疫苗能够诱导强烈的先天性和适应性免疫反应。通过基因工程技术,Lm的重组株可以表达外源抗原,包括肿瘤抗原。虽然未经修饰的Lm具有毒性,但临床使用的疫苗采用了多种方法来降低其致病性。例如,通过基因敲除ActA和InlB基因,这两种基因分别与细胞间扩散和肝脏归巢有关。敲除这些基因的菌株致死性降低了约四个对数单位,从而可以在增加剂量的同时增强抗原性。
这种方法已经应用于前列腺癌的Ⅰ期试验中,使用的是一种减毒活双删除(LADD)疫苗株ADU-741(由Aduro Biotech公司开发,位于加利福尼亚州伯克利)(Table 35.2)。该疫苗株的独特之处在于,它同时编码四种与前列腺相关的抗原:PSMA、PAP、癌抗原SSX2和前列腺相关转录因子NKX3.1。
另一种减毒方法是通过敲除李斯特菌裂解素O(LLO)基因,从而阻止李斯特菌进入宿主细胞的细胞质。这种方法由Advaxis公司(位于新泽西州普林斯顿)开发,并已进入临床试验阶段,正在进行与抗PD-1抗体帕博利珠单抗联合使用的I/II期临床试验。
基于Lm的疫苗已被证明能够减少肿瘤环境中调节性T细胞的数量,这些调节性T细胞通过分泌免疫抑制性细胞因子和抑制抗原提呈细胞(APC)的功能,削弱T细胞的免疫应答。此外,髓系来源的抑制性细胞(MDSCs)也通过产生类似的抗炎细胞因子,促成肿瘤环境中的高度抑制性状态。在基于Lm的抗肿瘤疫苗模型中,MDSCs的数量和抑制能力也显著降低。
李斯特菌天然的免疫刺激特性以及其易于基因操作的特性,使其成为开发用于晚期肿瘤(如mCRPC)疫苗的有力工具,尤其是在针对具有特定微环境的肿瘤时展现出很大潜力。
35.4 过继细胞疗法
广泛的抗肿瘤治疗并不总是对每位患者都有效,因此,研究人员正在努力开发针对个体肿瘤的个性化治疗方法。过继性细胞治疗(ACT)是一种从患者体内分离出细胞(通常是淋巴细胞)并进行基因操作,然后再回输到患者体内的技术。这种基因操作包括转导肿瘤抗原特异性T细胞受体基因或引入嵌合抗原受体(CAR)。CAR T细胞表达与下游激活复合物(如CD3-ζ)连接的抗体重链和轻链,使其在不依赖主要组织相容性复合物(MHC)背景的情况下被激活,同时保持抗原特异性。
目前,一项正在进行的Ⅰ期临床试验正在研究PSMA特异性CAR T细胞在mCRPC患者中的疗效,主要评估其安全性和耐受性(NCT01140373)。在最近的一项相关Ⅰ/Ⅱ期试验中,多发性骨髓瘤患者接受了NY-ESO-1特异性TCR工程化T细胞治疗,其中70%的患者达到了接近完全缓解或完全缓解的效果。这一发现尤为重要,因为NY-ESO-1是一种常见的睾丸癌抗原,在多种肿瘤类型中都有表达,包括前列腺癌。
35.5 抗肿瘤抗体
过继性细胞疗法的一个潜在缺点是所提供的细胞可能具有较长的寿命,这在长期毒性方面带来了一定的挑战。相比之下,基于抗体的疗法可以对肿瘤抗原展现相同的特异性,同时具有较短半衰期的优势。在前列腺癌治疗中,最为成熟的抗肿瘤抗体是J591,这是一种靶向PSMA的抗体。作为一种人源IgG1抗体,J591裸抗体(未修饰的抗体)有望诱导抗体依赖性细胞毒性(ADCC),即通过抗体的Fc部分与细胞表面表达的Fc受体相互作用,激活细胞毒性细胞(如巨噬细胞和NK细胞)。在人类中,这通常是通过IgG1亚型的抗体与NK细胞表面的Fcγ受体Ⅲ(FcγRIII)相互作用实现的。
在复发性前列腺癌患者中进行的一项Ⅱ期单臂试验中,J591与IL-2联合使用,显示出良好的耐受性,并且试验队列的生存期超过了Halabi模型的预期,提示可能存在长期生存获益。此外,J591还被结合放射性同位素,用于将放疗靶向前列腺肿瘤细胞。在一项使用放射性同位素$^{177}$Lu标记的J591的Ⅱ期试验中,8名患者的病情稳定,1名患者显示出影像学部分缓解。研究还发现,较高剂量的治疗与更长的生存期相关。除了作为治疗手段外,J591结合放射性同位素的能力还为肿瘤成像提供了高灵敏度和特异性。
前列腺癌的另一种抗肿瘤抗体是靶向B7-H3的抗体,B7-H3在原发肿瘤中高度表达,并且与较差的术后预后显著相关。一种靶向B7-H3的裸抗体(MGA271,由MacroGenics公司开发,位于马里兰州Gaithersburg)目前正处于Ⅰ期开发阶段,可以单独使用,也可以与帕博利珠单抗或伊匹单抗联合使用。临床前研究显示了令人鼓舞的反应结果,激发了人们对这些试验的兴趣。
一种有趣的免疫治疗方法是使用经过工程改造的抗体将T细胞引导至肿瘤部位。这类制剂通常包含两个部分:一个肿瘤特异性抗体部分(Fab)和一个对T细胞具有特异性的第二部分(通常是抗CD3的Fab)。其机制是在肿瘤结合部分与肿瘤靶点结合的同时,抗CD3部分非特异性地捕获路过的T细胞,并将其定向至肿瘤 (Fig.35.4)。抗体与T细胞表面的CD3分子结合后,可激活T细胞,进而导致肿瘤细胞的死亡。
针对前列腺癌,正在研发的一种双特异性抗体是DART™抗体(MGD009,由MacroGenics公司开发,位于马里兰州Rockville)。该药物靶向B7-H3和CD3,使其能够定位至表达B7-H3的肿瘤细胞,并将T细胞募集到该部位并激活它们,而不考虑抗原特异性 (Fig.35.4)。类似的研究还包括使用抗PSMA和CD3的双特异性T细胞结合抗体(BiTE™,BAY2010112,由拜耳公司开发,位于德国勒沃库森),目前正处于Ⅰ期临床试验中(NCT01723475),主要研究目标是确定最大耐受剂量和不良事件的数量。
此外,针对其他免疫细胞群体的抗体也在研发中,例如AAT-007(由AskAt公司开发,位于日本名古屋),这是一种用于治疗实体瘤的Ⅱ期EP4拮抗剂(NCT02538432)。阻断EP4可以消除髓系来源的抑制性细胞(MDSCs)的多种抑制功能,这些功能通常会削弱抗肿瘤反应。
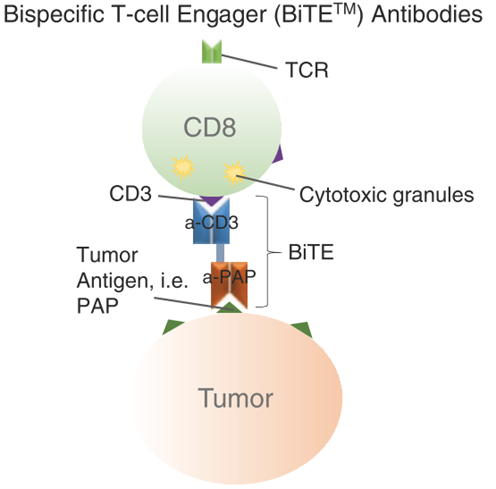
Fig 35.4 通过BiTE™抗体激活T细胞。BiTE™或DART™抗体通过结合T细胞表面的CD3分子,使T细胞被激活并对表达特定抗原(如PAP)的肿瘤细胞产生细胞毒性反应,而无需考虑T细胞的TCR特异性。BiTE™抗体由一个多肽链连接体组成,而DART™抗体则由两条多肽链和一个链间二硫键组成。
35.6 总结
mCRPC是一种免疫细胞浸润较少的致命性疾病,免疫治疗的效果往往不理想。虽然在其他实体瘤中有效的疗法(如免疫检查点抑制剂抗CTLA-4和抗PD-1)作为单药治疗时对晚期前列腺癌的疗效有限,但这种效果的缺乏可能与前列腺肿瘤中检查点配体的低表达有关。此外,肿瘤的内在特征(如低突变负荷)也可能是影响因素之一。
尽管如此,前列腺癌具有表达限于器官本身的几种关键肿瘤抗原(如PSMA和PSA),这使得前列腺癌成为疫苗治疗的理想靶点。疫苗有可能将“冷”肿瘤转变为“热”肿瘤,使其更容易受到免疫检查点阻断疗法的攻击。
mCRPC的抑制性肿瘤微环境对免疫治疗提出了重大挑战。可能需要联合治疗策略,不仅要解除免疫检查点的抑制,还要改善抗原的处理和呈递。尤其是通过疫苗来激活免疫系统,增强炎症反应,可能有助于增强适应性免疫的激活和功能。此外,抗体可以阻断维持抗炎肿瘤环境所需的关键相互作用,例如抑制MDSCs和TAMs的功能和生存。
综上所述,这些联合疗法有望广泛激活并动员免疫系统以对抗前列腺癌。总体而言,越来越多的证据表明,可能需要联合治疗方案来诱导足够的免疫活性,使其在前列腺癌的治疗中产生临床意义。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 章震
图文排版 | 林子畅 郑家怡
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏