前期精彩内容:
Nat Commun:衰老通过诱导免疫抑制性肿瘤微环境导致免疫治疗抗性
Cancer Cell:通过mRNA技术编码持久性IL-2在MHC I类分子缺陷癌症中可恢复针对新抗原的CD8+ T细胞反应
杂志名称:Cancer Cell
发表日期:2024.02.27
DOI:10.1016/j.ccell.2024.02.004.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38428412/
影响因子:50.3
内容简介
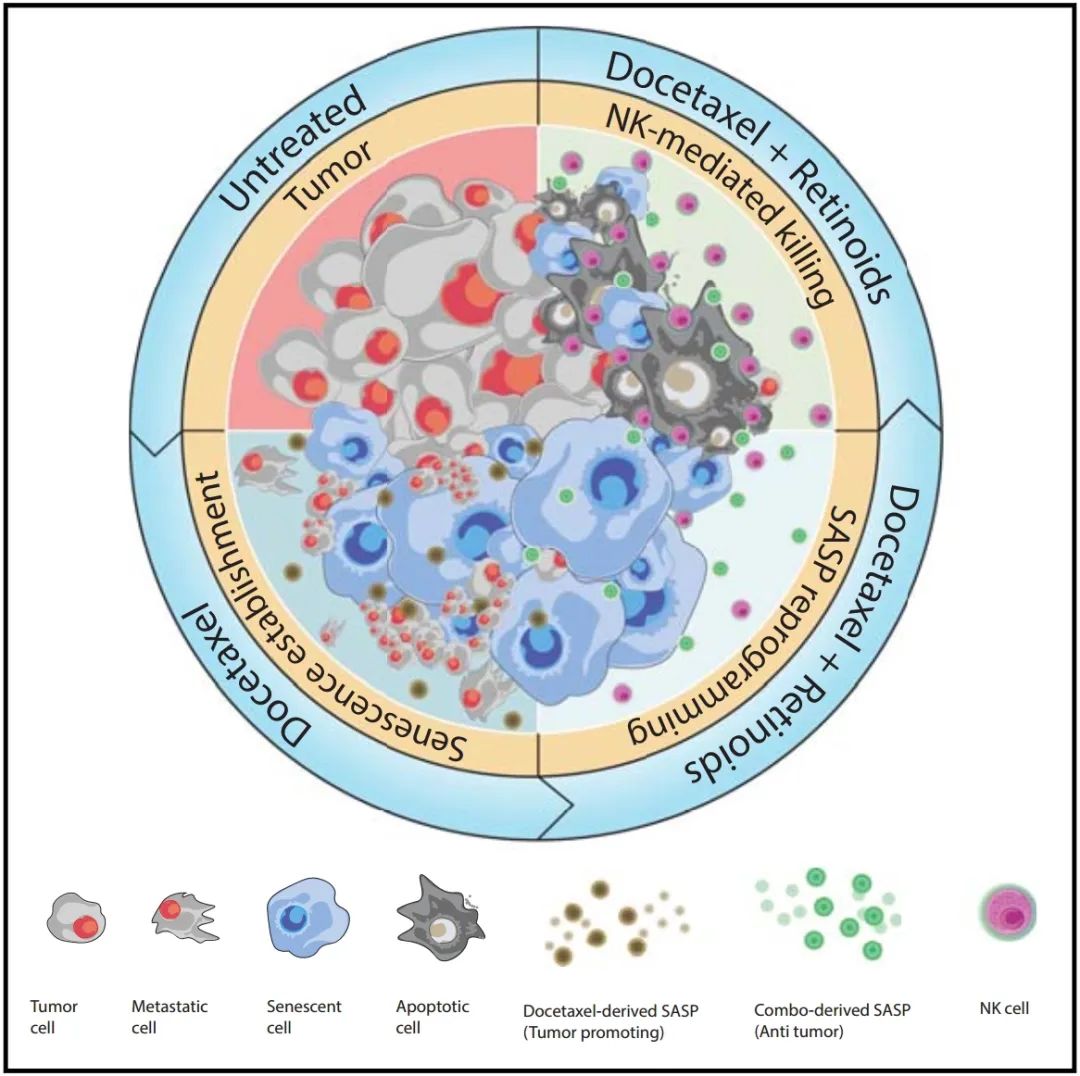
细胞衰老在肿瘤中可以产生双重效应,既可以抑制也可以促进肿瘤进展。由衰老细胞释放的衰老相关分泌表型(SASP)在这一二分性中发挥关键作用。因此,临床上的挑战在于开发安全增强癌症中衰老,并且偏好促进抑瘤的SASP因子而非促进肿瘤的因子的治疗方法。在这里,我们确定了维甲酸受体(RAR)激动剂阿达帕林作为前列腺癌(PCa)中有效的促衰老化合物。RAR的重新激活触发了强烈的衰老反应和抑瘤SASP。在前列腺癌的临床前小鼠模型中,阿达帕林与多西他赛的联合使用促进了抑瘤SASP,比单独使用任一药物都能更有效地增强自然杀伤(NK)细胞介导的肿瘤清除。这种方法增强了人类NK细胞对注射人类前列腺癌细胞的小鼠同种异体肿瘤的疗效,提示了一种在“免疫荒漠”肿瘤中刺激抗肿瘤免疫反应的替代治疗策略。
创新性及研究意义
这篇文章的核心创新性在于发现维甲酸受体(RAR)激动剂阿达帕林在前列腺癌中作为有效的促进衰老化合物。研究表明,通过重新激活RAR,可以触发强烈的细胞衰老反应和具有抑制肿瘤特性的衰老相关分泌型表型(SASP)。在前列腺癌的临床前小鼠模型中,阿达帕林与多西他赛的组合能够促进一种抑制肿瘤的SASP,这种组合比任一单独药物更有效地增强了自然杀伤(NK)细胞介导的肿瘤清除。
这项研究的意义在于提供了一种潜在的治疗策略,即通过激活RAR来促进肿瘤内的衰老反应和抗肿瘤免疫反应,尤其是在那些“免疫学上冷漠”的肿瘤中。通过这种方式,可以增强人体NK细胞在小鼠体内对人类前列腺癌细胞的杀伤效果,为开发新的抗肿瘤疗法提供了重要的实验依据。这不仅为肿瘤治疗提供了新的视角,也为理解肿瘤微环境中的细胞衰老机制和免疫反应提供了更深入的洞察。
数据图
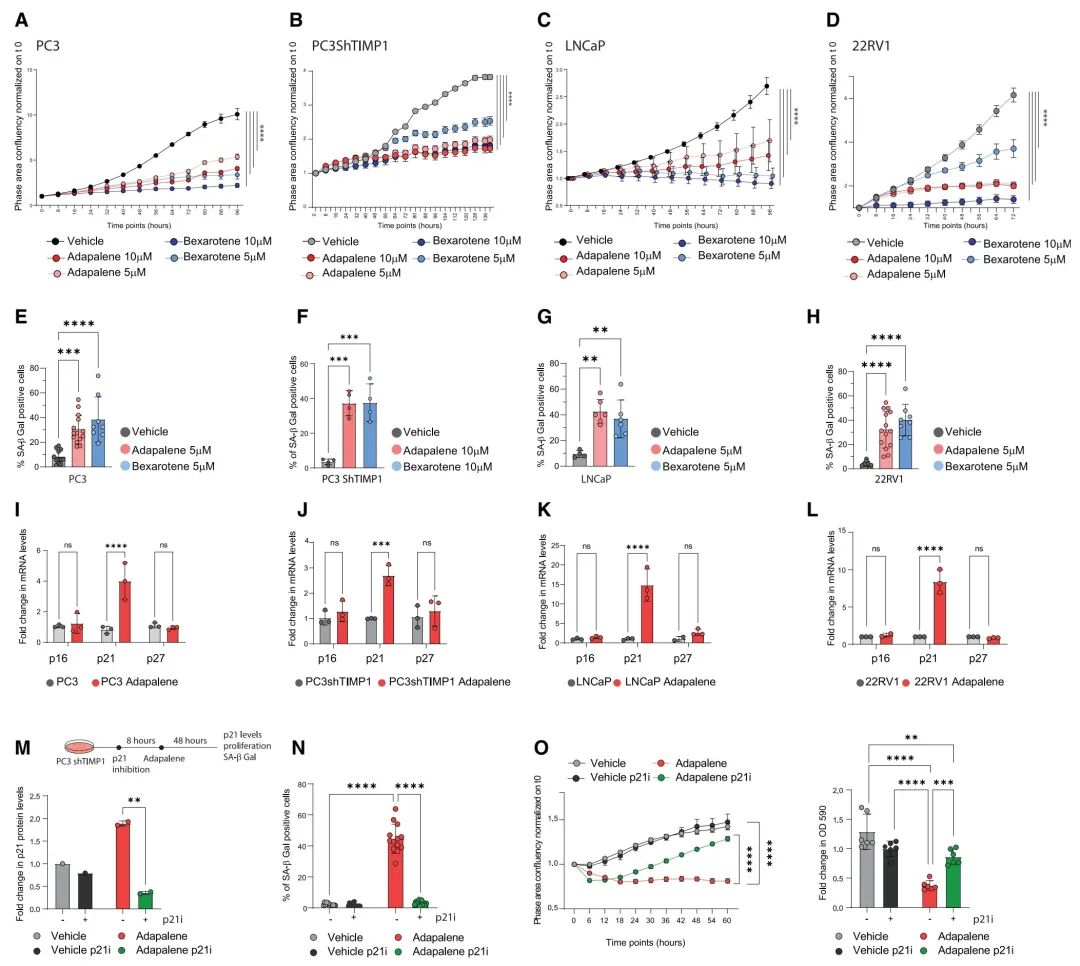
图 1. 发现RAR激动剂为促进衰老的化合物
(A) 特定化合物处理后PC3细胞增殖倍数的变化,以时间0为基准进行标准化。
(B) 特定化合物处理后PC3shTIMP1细胞增殖倍数的变化,以时间0为基准进行标准化。
(C) 特定化合物处理后LNCaP细胞增殖倍数的变化,以时间0为基准进行标准化。
(D) 特定化合物处理后22RV1细胞增殖倍数的变化,以时间0为基准进行标准化。
(E) 经过处理的PC3细胞中SA-β Gal的定量。
(F) 经过处理的PC3shTIMP1细胞中SA-β Gal的定量。
(G) 经过处理的LNCaP细胞中SA-β Gal的定量。
(H) 经过处理的22RV1细胞中SA-β Gal的定量。
(I) PC3细胞中衰老标志物的RT-qPCR分析。
(J) PC3shTIMP1细胞中衰老标志物的RT-qPCR分析。
(K) LNCaP细胞中衰老标志物的RT-qPCR分析。
(L) 22RV1细胞中衰老标志物的RT-qPCR分析。
(M) 实验设计(上图)及经处理的PC3shTIMP1细胞的免疫印迹定量(下图),参见图S1J。
(N) 经p21抑制剂(p21i)UC2288和adapalene处理的PC3shTIMP1细胞中SA-β Gal的定量。
(O) 经p21抑制剂(p21i)UC2288和adapalene处理后PC3shTIMP1细胞增殖倍数的变化,以时间0为基准进行标准化(左图),以及结晶紫染色定量(右图)。
数据(E–N)和(O右图)表示为均值 ± 标准差;数据(A–D)和(O左图)表示为均值 ± 标准误差。数据代表三到五次独立实验。数据(M)代表一次实验。数据(E–H)的统计测试使用单向方差分析后接Tukey’s测试 *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据(A–D)和(I–O)的统计测试使用双向方差分析 *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S1。
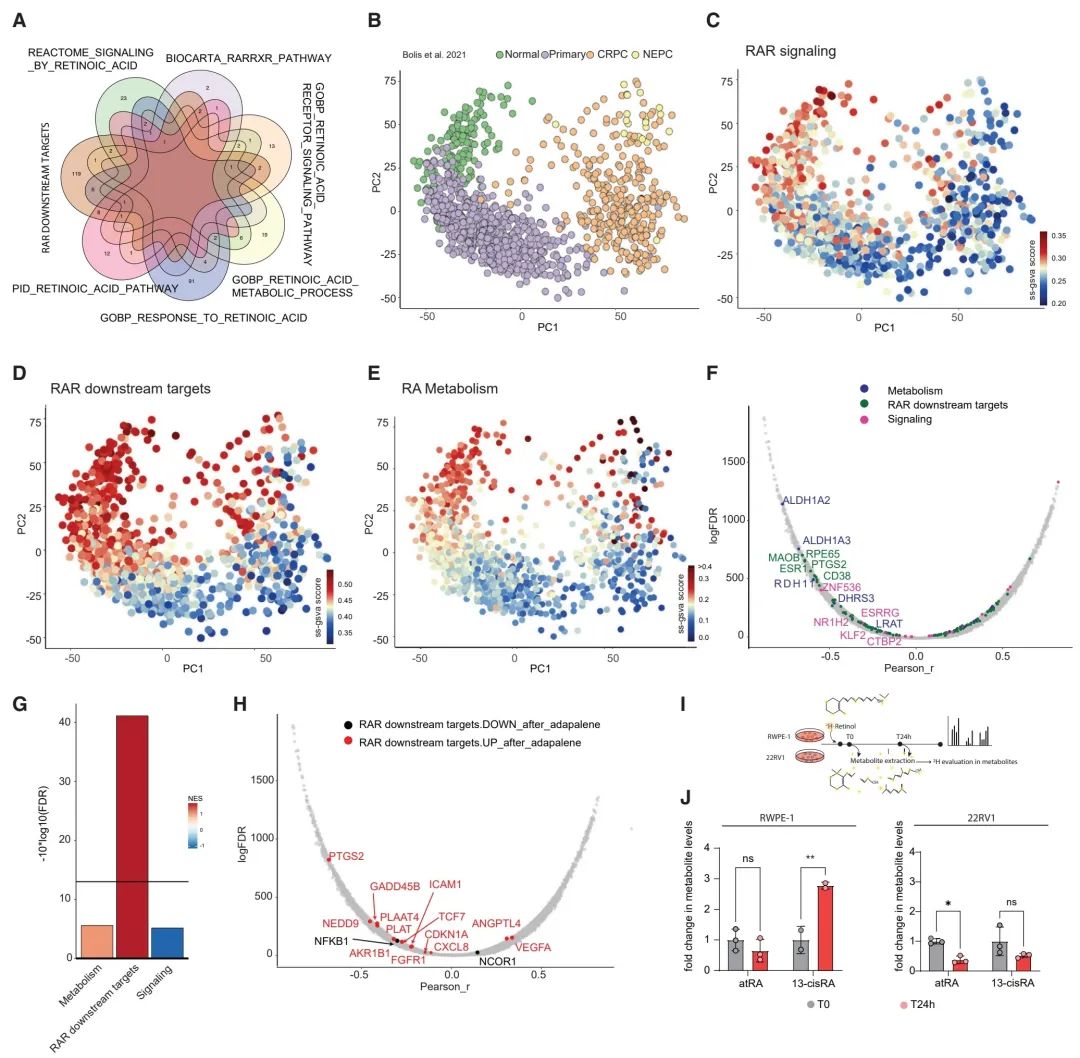
图 2. 维甲酸代谢和通路在前列腺癌发展过程中受损
(A) 维恩图展示了每个与RA相关的特征中差异表达基因的数量。
(B) 利用指定研究获得的全前列腺癌转录组进行主成分分析(PCA),比较正常前列腺(绿色)、原发性前列腺癌(紫色)、去势抵抗性前列腺癌(CRPC,橙色)和神经内分泌前列腺癌(NEPC,黄色)。
(C) PCA展示了PCa疾病进展过程中RAR信号通路的激活情况。
(D) PCA展示了PCa疾病进展过程中RAR下游目标的表达情况。
(E) PCA展示了PCa疾病进展过程中RA代谢相关基因的表达情况。
(F) 图表展示了患者RNA-seq数据中RA相关基因的皮尔森相关性。灰色点代表与RAR通路无关的基因,蓝色点代表与RA代谢相关的基因,绿色点代表RAR目标基因,粉色点代表与RAR信号相关的基因。
(G) 条形图展示了PC3shTIMP1细胞在adapalene处理与未处理情况下,从RNA-seq得到的RAR下游目标、RA相关代谢和RAR信号的标准化表达分数(NES)。
(H) 图表展示了患者和经adapalene处理的PC3shTIMP1细胞RNA-seq数据中RA相关基因的皮尔森相关性。灰色点代表与RAR通路无关的基因,黑色点代表adapalene处理后下调的基因,红色点代表上调的基因。
(I) (J)的实验设计。
(J) 在非转化前列腺细胞系RWPE-1和癌细胞系22RV1中,经2H-ROH处理后ROH转化产物(atRA和13-cisRA)的倍数变化。
数据(J)展示为表示一次实验的均值 ± 标准差。统计测试(J)使用的是单向ANOVA后接Tukey’s测试 *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。另见图S2。
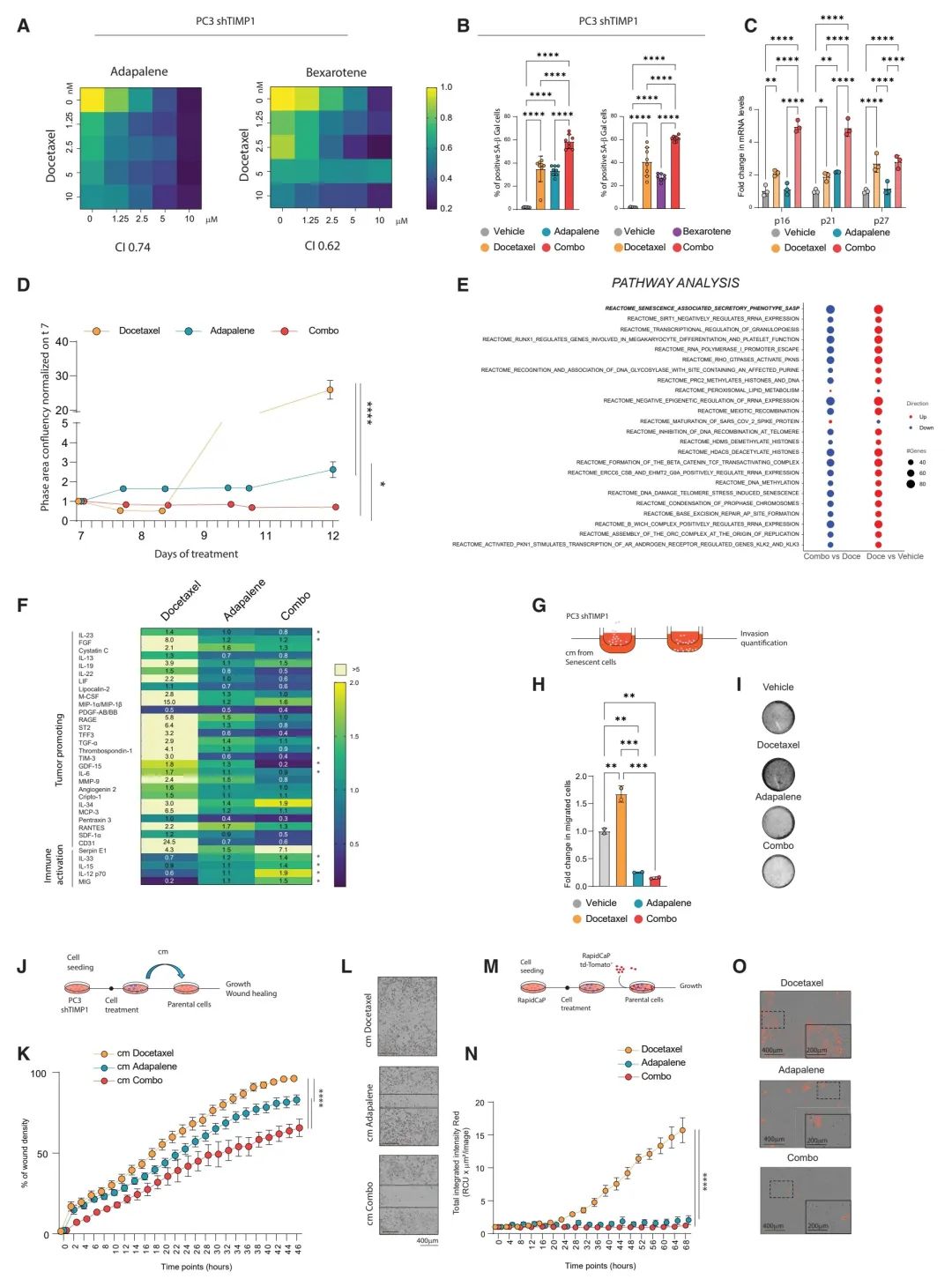
图 3. RARs激活通过重新编程SASP增强化疗效果
(A) 热图展示了对PC3shTIMP1细胞进行的协同增殖实验结果,这些细胞接受了docetaxel和adapalene或docetaxel和bexarotene组合治疗(治疗48小时)。
(B) 对用docetaxel、adapalene及其组合(左侧)和docetaxel、bexarotene及其组合(右侧)治疗两天后的PC3shTIMP1细胞进行的SA-β Gal实验的定量。
(C) 对用docetaxel、adapalene和组合药物治疗的PC3shTIMP1细胞进行衰老标志物的RT-qPCR分析。
(D) 在连续12天的治疗中,PC3shTIMP1细胞增殖的倍数变化,以第7天为基准进行标准化(每三天更换一次培养基)。
(E) 对PC3shTIMP1细胞的RNA-seq进行的通路分析,展示了组合药物与docetaxel及docetaxel与对照组比较时上调和下调的通路。报道的通路FDR <0.05。
(F) 对用指定药物治疗的PC3ShTIMP1细胞进行的细胞因子阵列,以对照组细胞为基准进行标准化。
(G) (H和I)的实验设计。
(H) 对PC3shTIMP1细胞进行的Boyden室迁移实验的定量,这些细胞暴露于docetaxel、adapalene或组合药物的条件培养基中,以OD590的倍数变化表示。
(I) 用结晶紫染色的Boyden室的代表性图像。
(J) (K和L)的实验设计。
(K) 用docetaxel、adapalene或组合药物处理的PC3shTIMP1细胞的条件培养基处理的PC3shTIMP1亲本细胞的创伤密度百分比。
(L) K的代表性图片(刻度尺:400毫米)。
(M) (N和O)的实验设计。
(N) 在与衰老的未标记RapidCaP细胞共培养的情况下,TdTomato+ RapidCaP细胞的增殖,以总积分强度(RCU x mm²/图像)的倍数变化量化。
(O) N中增殖实验的代表性图像(刻度尺:400毫米,插图200毫米)。
数据(B)、(C)和(H)以均值 ± 标准差显示。数据(H)使用的统计测试:单向ANOVA后接Tukey’s测试 *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据(D)、(K)和(N)以均值 ± 标准误差显示。数据(B–D)、(K)和(N)使用的统计测试:双向ANOVA *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据(F)代表一次实验。图版(A–D)、(H)、(K)和(N)的数据代表三次独立实验。另见图S3。
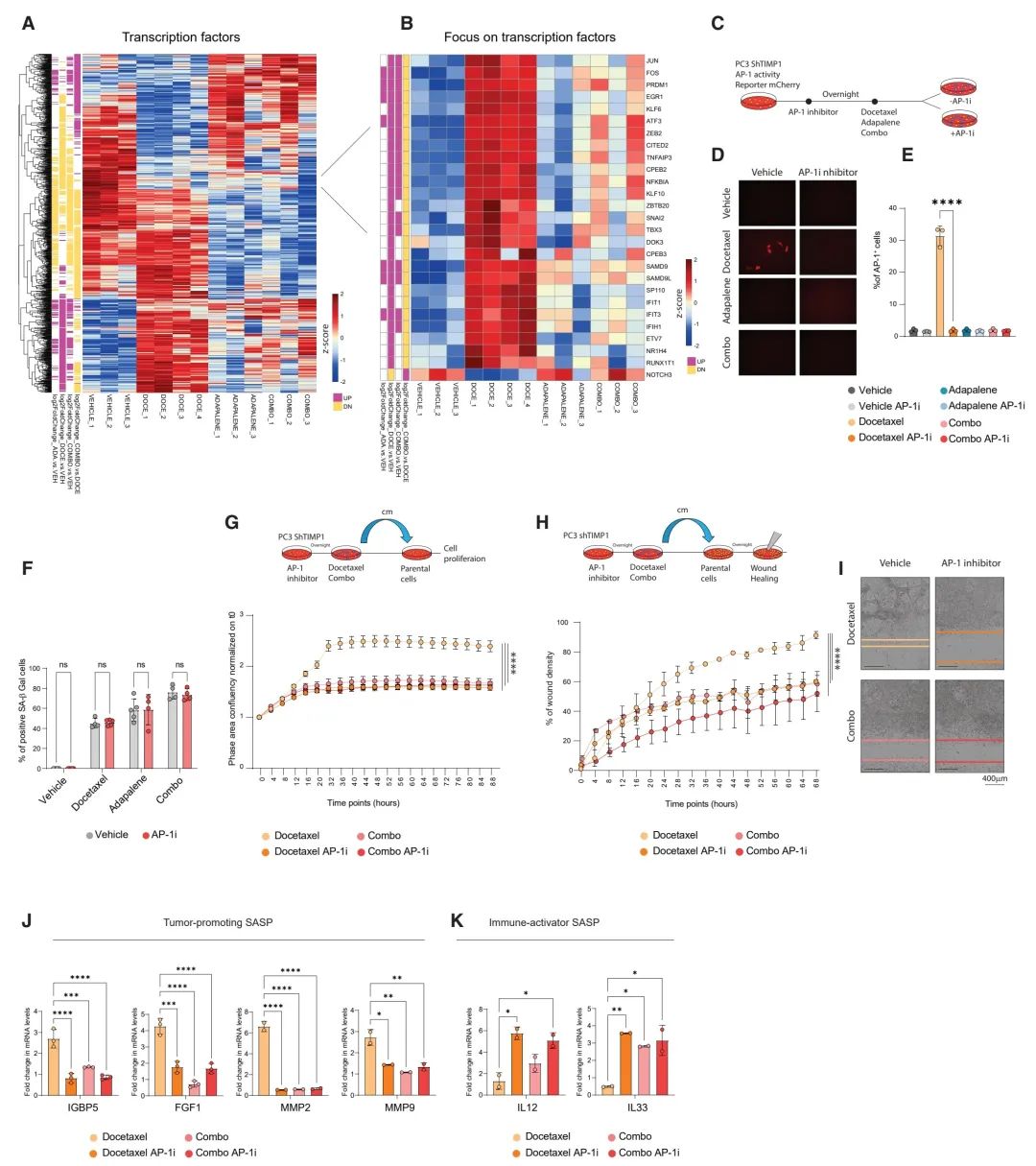
图 4. 阿达帕林通过AP-1重新编程由多西他赛引发的有害SASP
(A) 热图展示了用多西他赛、阿达帕林和组合药物处理的PC3shTIMP1细胞中差异表达的转录因子。至少在一次与对照药物比较中报告的基因FDR <0.05。
(B) 热图的焦点展示了在PC3shTIMP1细胞中差异表达的转录因子,这些因子在用多西他赛与对照药物处理的细胞以及组合药物与多西他赛处理的细胞中有相反的表达模式。
(C) (D和E)的示意图。
(D) 代表性图片展示了以mCherry荧光表示的AP-1介导的转录激活。
(E) 在有或无AP-1抑制剂(AP-1i)T-5224的情况下,用多西他赛、阿达帕林或组合药物处理的PC3shTIMP1细胞中mCherry阳性细胞的定量。
(F) 在有或无AP-1抑制剂的情况下,用多西他赛、阿达帕林或组合药物处理的PC3shTIMP1细胞的SA-β Gal染色定量。
(G) 实验设计的表示(上图)和在有或无AP-1抑制剂的情况下,用前列腺肿瘤细胞的条件培养基(经多西他赛或组合药物处理)处理的PC3shTIMP1细胞的增殖倍数变化,以t0为基准(下图)。
(H) 实验设计(上图)和用经多西他赛和组合药物处理的细胞的条件培养基处理的PC3shTIMP1细胞的创伤并合百分比(下图)。
(I) (H)中创伤愈合实验的代表性图片(刻度尺:400毫米)。
(J) 所示肿瘤促进分泌因子mRNA水平的倍数变化。
(K) 不同抗肿瘤免疫反应激活因子mRNA水平的倍数变化。
数据(G)和(H)以均值 ± 标准误差显示。使用的统计测试:双向ANOVA,****p < 0.0001。数据代表三次独立实验。数据(E)、(F)、(J)和(K)以均值 ± 标准差显示。数据(E)使用的统计测试:单向ANOVA后接Tukey’s测试 *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据(F–H)、(J)和(K):双向ANOVA *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据代表两次独立实验。另见图S4。
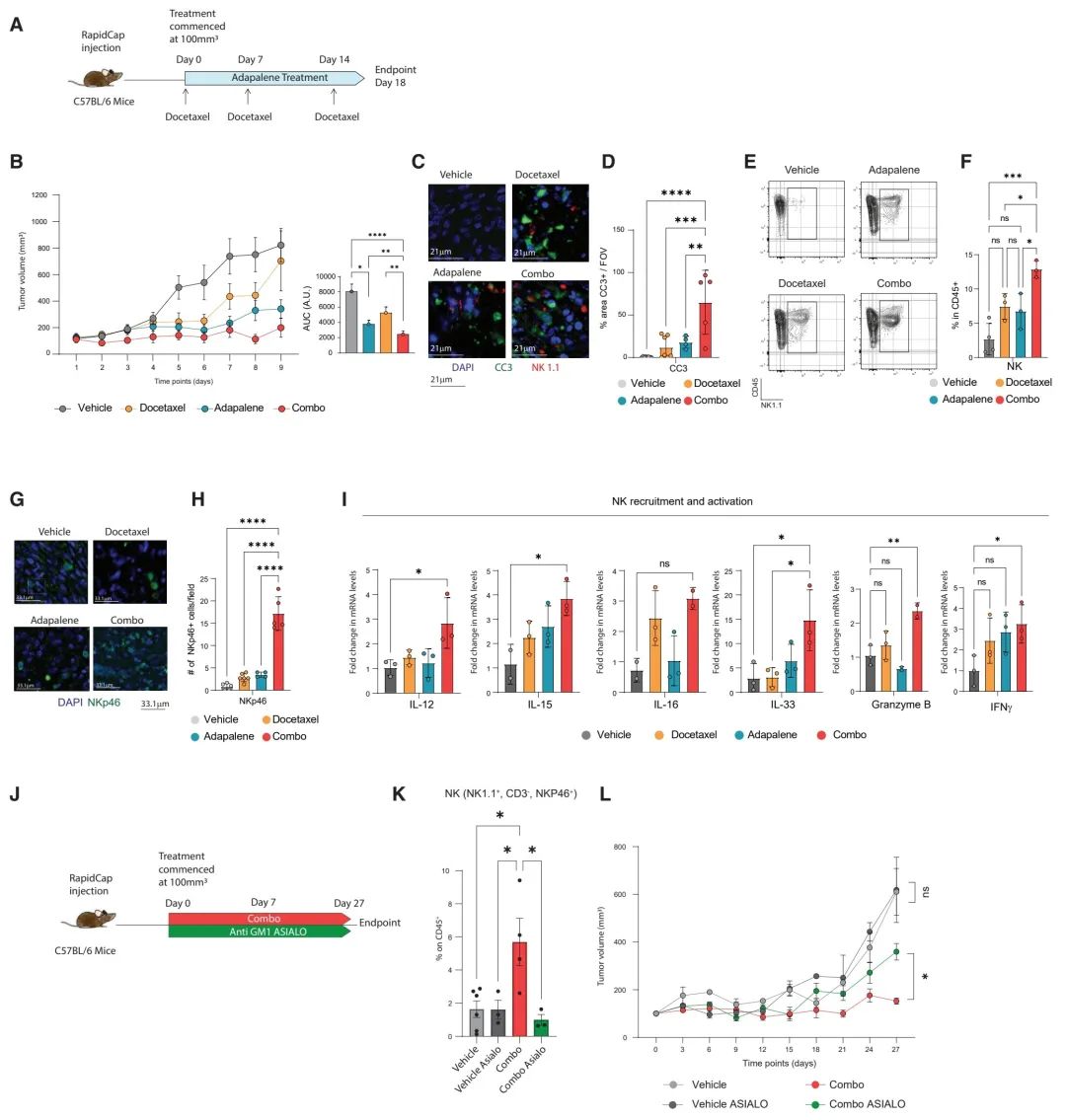
图 5. 阿达帕林联合多西他赛增强细胞衰老并激活抗肿瘤免疫反应
(A) 实验设计。
(B) 给予指定药物治疗的小鼠的肿瘤体积(单位:mm³,每组n = 5)(左图),以及基于肿瘤体积计算的曲线下面积(右图)。
(C) 肿瘤切片中NK细胞(使用抗NK1.1抗体,红色)和裂解型caspase 3(CC3,绿色)的免疫荧光染色(刻度尺:21 mm)。
(D) 来自(C)中肿瘤切片每个视野中CC3阳性细胞的定量。
(E) 用指定药物治疗的肿瘤中NK1.1和CD45+细胞的FACS图,筛选活细胞。
(F) 用指定药物治疗的肿瘤中NK1.1+细胞的百分比。
(G) 肿瘤切片中NK细胞(使用抗NKp46抗体,绿色)的免疫荧光染色(刻度尺:33.1 mm)。
(H) 来自(G)的肿瘤切片每个视野中NK细胞的定量。
(I) 用指定药物治疗的肿瘤中招募NK细胞及其产生的颗粒酶B和IFNγ的mRNA水平的倍数变化。
(J) (K和L)的实验设计示意图。
(K) 未经治疗或用联合药物和抗GM1 Asialo治疗的小鼠肿瘤中浸润的NK细胞(NK1.1+,CD3–,NKp46+)在CD45+细胞中的百分比。
(L) 在有或无NK细胞耗竭抗体存在下,用指定药物治疗的小鼠的肿瘤体积(单位:mm³,Vehicle, Iso n = 4, Vehicle, Asialo n = 4, Combo, Iso n = 3, Combo, Asialo n = 4)。
数据(B)和(L)以均值 ± 标准误差显示。使用的统计测试:双向ANOVA *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据(B)代表两次独立实验。数据(L)代表一次实验。数据(D)、(F)、(H)、(I)和(K)以均值 ± 标准差显示。使用的统计测试:单向ANOVA后接Tukey’s测试 *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据代表一次实验。另见图S5。
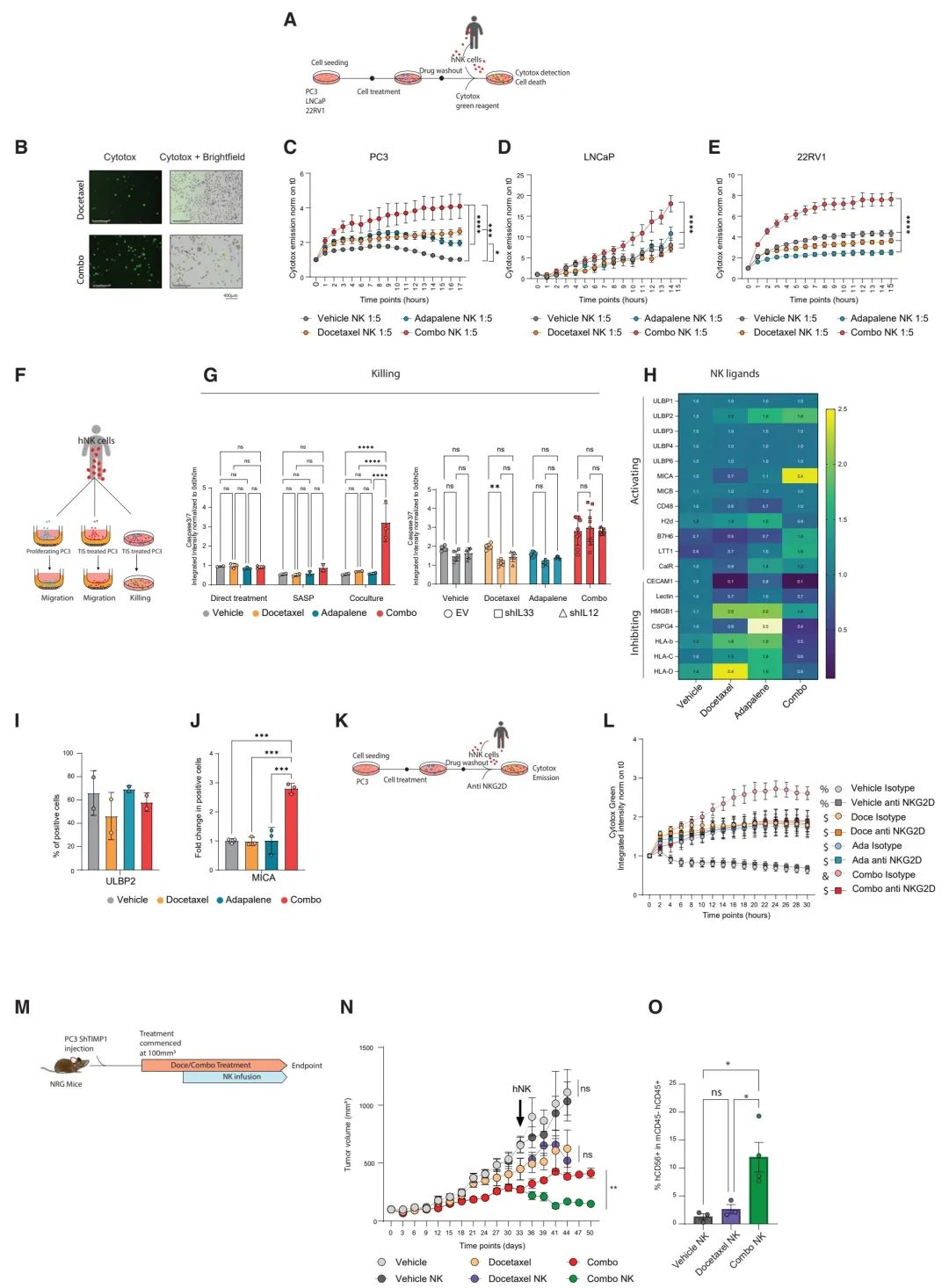
图 6. RAR激动剂联合多西他赛增强了源自人体的NK细胞的抗肿瘤活性
(A) 实验设计。
(B) 代表性图像显示与人NK细胞共培养的、预先用多西他赛和组合药物处理过的PC3细胞的细胞毒性发射(绿色)(刻度尺:400mm)。
(C) PC3细胞在预处理指定化合物后与人NK细胞共培养(目标:效应比1:5)时,细胞毒性发射的定量,以总积分强度(GCU x mm²/图像)的倍数变化表示。
(D) LNCaP细胞在预处理指定化合物后与人NK细胞共培养(目标:效应比1:5)时,细胞毒性发射的定量,以总积分强度(GCU x mm²/图像)的倍数变化表示。
(E) 22RV1细胞在预处理指定化合物后与人NK细胞共培养(目标:效应比1:5)时,细胞毒性发射的定量,以总积分强度(GCU x mm²/图像)的倍数变化表示。
(F) (G)的实验布局示意图。
(G) PC3细胞经指定化合物处理后的caspase 3/7累积荧光强度,以时间0(t0)为基准进行标准化,左图为不同化合物处理,右图为不同shRNAs工程化处理:EV(圆圈)、shIL-33(方块)、ShIL-12(三角)。
(H) PC3细胞的RT-qPCR分析,显示癌细胞上NK配体的表达。
(I) FACS分析显示表达ULBP2的PC3细胞的阳性百分比。
(J) FACS分析显示表达MICA的PC3细胞的阳性百分比。
(K) (L)的实验设计示意图。
(L) 在有或无中和NKG2D抗体存在的情况下,用指定化合物处理的PC3细胞的Cytotox绿色发射积分强度,以时间0(t0)为基准进行标准化。
(M) (N和O)的实验设计表示。
(N) 经不同处理的小鼠的肿瘤体积(mm³),分组情况:对照(n = 15),对照+NK(n = 16),多西他赛(n = 7),多西他赛+NK(n = 7),组合(n = 15),组合+NK(n = 16)。由于肿瘤溃疡,对照组、对照NK组、多西他赛组和多西他赛NK组的小鼠在第44天较早时间点被安乐死。
(O) FACS分析显示门控在hCD45+、mCD45-中的hCD56+细胞的百分比。
数据(G)、(I)、(J)和(O)以均值 ± 标准差显示。数据(C–E)、(L)和(N)以均值 ± 标准误差显示。数据(C–E)、(G)和(N)使用的统计测试:双向ANOVA *p < 0.05, **p < 0.01, ***p < 0.001, ****p < 0.0001。数据(I)和(J)使用的统计测试:单向ANOVA后接Tukey’s测试 ***p < 0.001。数据(C–E)、(G–J)、(L)和(N)代表两次独立实验。数据(O)代表一次实验。数据(L)使用的统计测试:双向ANOVA。带有不同符号的线表示彼此间统计学上存在显著差异。另见图S6。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏