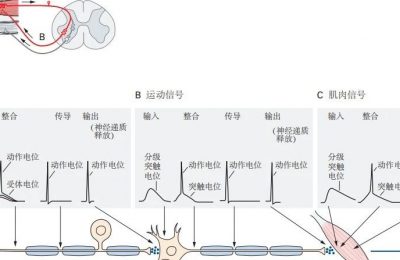
上期内容:神经科学原理-第2章 基因和行为(上)
2.6 通过研究人类遗传综合症初步揭示社会行为的基础
2.6.1 人类脑部疾病是基因与环境相互作用的结果
人类神经系统疾病的研究首次清晰地展示了基因与环境在决定认知和行为表型时的相互作用。1934年,挪威科学家阿斯比约恩·佛林描述了苯丙酮尿症,这种疾病大约影响每15,000名儿童中的一名,导致严重的认知功能障碍。
苯丙酮尿症患者携带两个异常的苯丙酮尿症基因拷贝,这些基因编码苯丙氨酸羟化酶,一种将氨基酸苯丙氨酸转化为酪氨酸的关键酶。由于这种突变是隐性的,杂合子携带者没有症状。缺乏正常功能的两个基因副本的儿童会从饮食中的蛋白质中积累大量苯丙氨酸,进而产生干扰神经元功能的有毒代谢物。尽管苯丙氨酸如何具体影响大脑的生化过程尚未完全理解,但其结果是明显的。
苯丙酮尿症的表现(智力障碍)是基因型(苯丙酮尿症基因的纯合突变)与环境(饮食)相互作用的结果。因此,苯丙酮尿症的治疗方法既简单又有效:通过低蛋白饮食可以预防发育迟缓。对苯丙酮尿症基因的分子和遗传分析显著改善了受影响个体的生活质量。自20世纪60年代初以来,美国实施了新生儿苯丙酮尿症的强制性筛查。通过在症状出现前识别患有该遗传病的儿童并调整他们的饮食,许多疾病发展相关的问题得到了预防。
本书后面的章节将描述许多单基因特征的例子,如苯丙酮尿症,这些例子加深了我们对大脑功能和功能障碍的理解。这些研究揭示了一些共同主题。例如,一些罕见的神经退行性疾病,如亨廷顿病和脊髓小脑性共济失调,是由蛋白质中谷氨酸残基的异常扩展引起的。这些多谷氨酸重复疾病的发现突显了错误折叠和聚集的蛋白质对大脑的潜在危害。此外,发现癫痫发作可以由离子通道的多种突变引起,这使我们认识到这些疾病主要是由神经元兴奋性失调导致的。
2.6.2 罕见的神经发育综合症为社会行为、知觉和认知的生物学提供了见解
儿童时期出现的神经和发育障碍突显了遗传学在人类大脑功能中的重要性和复杂性。早期对基因如何影响特定认知和行为回路的证据来自对一种罕见的遗传病——威廉斯综合症的研究。患有这种疾病的个体通常语言能力正常,且极具社交性;他们在幼年时不具备常见的对陌生人的羞怯。然而,这些个体在空间处理能力方面严重受损,整体智力存在缺陷,并且焦虑程度较高(尽管很少表现为社交焦虑)。与自闭症谱系障碍等其他疾病相比,威廉斯综合症的特征表明,语言和社交技能可以与大脑的其他功能区分开来。
在自闭症儿童中,语言相关的大脑区域受损,而这些区域在威廉斯综合症患者中却表现活跃或过度活跃。相比之下,威廉斯综合症患者的一般智力和空间智力受损程度远高于大多数自闭症谱系障碍儿童。
威廉斯综合症是由于第7号染色体1区1带2亚带3次亚带的一个染色体区域的杂合缺失引起的,这通常涉及大约1.5Mb的DNA和27个基因。对这一缺失最简单的解释是,这些基因的表达水平降低,因为每个基因只有一个拷贝而非两个。尽管影响社交沟通和空间处理的确切基因尚未明确,但这些基因非常引人关注,因为它们可能为理解人类行为的遗传调控提供重要线索。
自闭症谱系障碍的最新研究进一步强调了遗传变异与社会和智力功能之间的复杂关系,这一关系最初通过对威廉斯综合症的研究得到了揭示。过去十年中,基因组技术的进步使得研究人员能够使用高通量方法筛查基因组中的染色体结构变异,并且其分辨率远高于传统光学显微镜(见Box 2.1)。2007年和2008年的开创性研究表明,患有自闭症谱系障碍的个体比未受影响的个体更频繁地携带新的(从头)拷贝数变异。这些发现首次将特定基因组区域与常见形式的自闭症谱系障碍(即没有综合症特征的自闭症谱系障碍,也称为特发性或非综合症性自闭症谱系障碍)联系了起来。
2011年,两项大规模研究同时对一个明确定义的队列进行了去新拷贝数变异的分析,发现威廉综合症中缺失的同一区域在某些个体中显著增加了自闭症谱系障碍的风险。然而,在这些案例中,导致风险增加的并非缺失,而是该区域的额外副本(重复)。这些发现表明,相同一组基因的丢失和增加可能会导致截然不同的社会行为表型,尽管两者通常都与智力障碍有关。这进一步支持了认知和行为功能领域可以分离,但可能共享重要的分子机制。
脆性X综合症是另一种提供认知功能遗传学深入见解的儿童神经发育障碍。与威廉综合症不同,脆性X综合症已被定位到X染色体上的单个基因。脆性X综合症的表现各不相同,受影响的儿童可能表现出智力障碍、社交认知困难、高度社交焦虑和重复行为;大约30%的脆性X综合症男孩符合自闭症谱系障碍的诊断标准。此外,脆性X综合症还与一些身体特征有关,例如长脸和突出的耳朵。
脆性X综合症的原因已被确认为是编码脆性X智力迟钝蛋白的基因表达减少所致。由于该基因位于X染色体上,当男性携带唯一的该基因拷贝发生突变时,他们将失去该基因的所有表达。脆性X智力迟钝蛋白在神经元中调控信使RNA的翻译,而这一过程本身受到神经元活动的调节。神经元中调控的翻译是突触可塑性的重要组成部分,这对于学习至关重要。因此,脆性X综合症在翻译水平上的缺陷会影响神经元功能、学习能力及更高层次的认知过程。有趣的是,许多与自闭症谱系障碍和精神分裂症风险增加相关的基因也受到脆性X智力迟钝蛋白的调控。
另一种广为人知的孟德尔遗传疾病是雷特综合症(在第62章中详细讨论)。雷特综合症是一种X连锁的进行性神经发育障碍,是女性智力障碍的主要原因之一。这种疾病几乎只影响女性,因为典型的雷特综合症突变在发育中的男性胚胎中通常是致命的,男性只有一条X染色体。受影响的女孩通常在6至18个月大时,发育出现停滞,语言能力未能正常获得,智力功能开始退化,并且表现出强迫性、不受控制的手部扭动,而非有目的的手部动作。此外,患有雷特综合症的女孩通常会经历一段时间的社交互动明显受损,这可能与自闭症谱系障碍难以区分,尽管社交功能在后期生活中通常会有所改善。胡达·佐格比和她的团队发现,这种综合症的主要原因是甲基CpG结合蛋白2(MeCP2)基因的突变。特定CpG序列的DNA甲基化会改变邻近基因的表达,而MeCP2的作用之一是结合甲基化DNA,调控信使RNA的转录过程。
罕见综合症还为我们提供了一些关于精神分裂症遗传基础的初步见解(见第60章)。例如,1978年,罗伯托·什普林茨恩及其同事首次描述了22q11染色体缺失,发现这种缺失会导致广泛的身体和行为症状,包括精神病。现在,这种情况通常被称为腭心面综合症、迪格奥尔格综合症或22q11缺失综合症。由于与相同缺失相关的表型差异非常大,最初这种描述受到了质疑。然而,现在已普遍接受,22q11缺失是与精神分裂症和儿童期发病的精神分裂症相关的最常见染色体异常之一。此外,研究发现,同一区域的染色体缺失也与自闭症风险增加有关。虽然目前尚未确定该区域内具体导致精神病表型的基因,但来自自闭症研究的最新证据表明,这一区域内多个基因的组合——每个基因都具有相对较小的效应——可能共同导致了社会障碍的表型。
2.7 精神疾病涉及多基因特征
如前所述,与神经退行性疾病和精神疾病的整体负担相比,单基因综合症相对罕见。因此,有人可能会质疑,既然罕见疾病只占疾病总负担的一小部分,研究它们的意义何在。实际上,研究这些罕见疾病可以为我们提供对更常见、更复杂疾病所涉及的生物学过程的深刻见解。例如,人类遗传学的一个重要成就是发现了导致早发性阿尔茨海默病或帕金森病的罕见遗传变异。尽管携带这些严重罕见变异的个体在所有患有这些疾病的人群中只占很小一部分,但对这些罕见变异的研究揭示了在更广泛患者群体中也被干扰的细胞过程,从而为普遍的治疗策略指明了方向。同样,对雷特综合症、脆性X综合症以及其他神经发育障碍的病理生理机制的研究,已经促成了一些针对精神综合症的合理药物开发初步尝试。
在本章的余下部分,我们将深入探讨两种复杂神经发育和精神疾病的遗传学:自闭症谱系障碍和精神分裂症。与前面讨论的罕见孟德尔遗传病相比,这些常见疾病的遗传学更加复杂、多样且异质,涉及许多不同个体中的众多基因,以及多个共同作用提供易感性的风险基因。此外,尽管有大量证据表明这些疾病有显著的遗传成分,但环境因素的影响同样不可忽视。
对这些疾病的理解得益于基因组技术和统计方法的快速发展、开放数据共享的文化,以及大规模患者队列的整合,这些因素使得研究人员能够检测到非常罕见的高渗透性等位基因和携带小风险增量的常见遗传变异。更为重要的是,最近在理解这两种综合症方面取得的进展,为深入探究这些遗传风险因素在分子、细胞和神经回路层面引发的病理生理学奠定了坚实的基础。
2.7.1 孤独症谱系障碍遗传学的进展揭示了罕见和从头突变在神经发育障碍中的关键作用
孤独症谱系障碍(ASD)是一类具有不同程度严重性的发育综合症,影响大约2%至3%的人口,其特征是社交沟通障碍、刻板兴趣以及重复行为。ASD在男性中更为常见,受影响的男孩人数平均是女孩的三倍。ASD的临床症状通常在生命的前3年内显现,尽管在生命的最初几个月内,受影响的儿童与未受影响的儿童之间已经能够观察到显著的差异。
ASD患者之间存在显著的表型变异性,这导致了该障碍的广泛诊断分类。此外,ASD患者比一般人群更频繁地出现癫痫发作和认知问题,并且在适应功能方面往往面临严重的挑战。然而,许多ASD患者并未受到如此严重的影响,能够过上非常成功的生活。
ASD具有很强的遗传基础(见图2.1.1A),这可能是它成为首批通过现代基因发现工具和方法得到深入研究的复杂神经精神综合症之一的原因。ASD的研究不仅对理解这种特定障碍具有意义,还为理解典型的人类行为(如语言、复杂智力和人际互动)提供了重要见解。值得注意的是,ASD中观察到的社交沟通缺陷可以与正常智力和其他认知功能共存,这表明大脑在某种程度上是模块化的,不同的认知功能可以独立变化。
虽然ASD的综合征形式只占所有病例的一小部分,但首次研究发现,在更常见的“特发性”或“非综合征”形式的ASD中,罕见突变也发挥了重要作用,并具有显著的生物学效应。例如,2003年对少数具有孤独症特征的女性进行基因测序,发现X染色体上的神经连接蛋白4X基因(NLGN4X)存在罕见的功能丧失突变,该基因编码一种在兴奋性神经元中起作用的突触粘附分子。在这些女性中,几位受影响的男性家族成员也携带了这一突变。不久之后,对一个大型家族的连锁分析显示,患有智力障碍和ASD的家族成员同样携带NLGN4X的功能丧失突变。
染色体结构中的从头亚显微缺失和重复可能显著增加个体患孤独症谱系障碍(ASD)的风险。这些拷贝数变异(CNV)往往集中在基因组的特定区域,从而确定了特定的风险区段。早期的研究表明,尽管染色体16p11.2的新生CNV仅出现在大约0.5%至1%的ASD患者中,但它能将患ASD的风险增加10倍以上。随后,研究确定了十多个类似的高风险CNV,包括16号染色体1区1带2亚带、1号染色体2区1带、15号染色体1区1带1亚带3次亚带、3号染色体2区9带、22号染色体1区1带和1区3带(SHANK3基因缺失)、2号染色体1区6带(NXRN1基因缺失)以及7号染色体1区1带2亚带3次亚带(威廉综合症区域)的从头重复。
有趣的是,虽然这些CNVs显著增加了ASD的风险,但研究还发现它们同样与精神分裂症和双相情感障碍等其他精神疾病的风险增加有关。此外,通过基因型确定的个体研究表明,这些CNV与多种行为表型相关,从特定语言障碍到智力障碍,再到精神分裂症不等。这种“一对多”现象对深入理解精神疾病的特定病理生理机制以及从基因发现到治疗的转化提出了重大挑战。
罕见的从头CNV会增加ASD及其他发育障碍的风险,这一广泛且可复制的发现引发了一个关键问题:是否单个基因中的罕见从头突变也可能带来类似的风险。事实上,随着低成本、高通量DNA测序技术的发展,研究人员最初集中在基因组的编码部分,鉴定出了大量可能破坏基因功能的从头突变(可能的基因破坏突变)。这些突变在无关个体中反复出现,现在被用来识别ASD的特定风险基因。
大规模研究现已确定了100多个与ASD相关的基因,其中约45个达到了统计学上的最高置信度。这些基因涵盖了广泛的已知功能,但分析表明,参与突触形成和功能以及转录调控的基因在ASD中显著过量。此外,编码脆性X智力低下蛋白的基因以及在早期大脑发育中活跃的基因也显著超过了预期。这些发现为理解ASD的生物学基础提供了重要线索。
2.7.2 精神分裂症基因的鉴定揭示了罕见和常见风险变异的相互作用
精神分裂症影响了约1%的年轻人,表现为思维障碍和情感退缩,严重损害了生活质量。这种疾病具有很强的遗传性(见图2.1.1B),同时也受到与胎儿期压力相关的强大环境因素的影响。二战后荷兰饥荒期间出生的儿童,在多年后患精神分裂症的风险显著增加;同样,在1960年代风疹病毒大流行期间,孕期感染风疹病毒的母亲所生的儿童,也面临更高的患病风险。
精神分裂症的发病受基因和环境的共同影响。与孤独症类似,基因组测序、全基因组基因分型和拷贝数变异(CNV)检测技术的进步,加上大规模患者队列的整合,推动了精神分裂症遗传学研究的重大突破。
首先,到2000年代初期,罕见的新发CNV开始与精神分裂症的风险相关联。这些染色体异常往往与自闭症谱系障碍相关的位点高度重叠,但在风险表现上有所不同。例如,16号染色体1区1带2亚带区域的重复和缺失都与ASD和精神分裂症有关,但该区域的重复更可能导致精神分裂症,而缺失则更常见于ASD和智力障碍。
过去十五年中,精神分裂症研究的最重要进展之一是全基因组关联研究(GWAS)的出现。与早期基于假设的候选基因研究不同,GWAS通过同时检测基因组中每个基因的多态性来识别风险基因。这种无假设的方法,结合大规模队列,并适当校正多重比较,已成为一种高度可靠和可重复的策略,用于识别常见疾病中的常见风险等位基因。
一项涉及近4万个病例和113,000个对照的GWAS研究确定了108个与精神分裂症相关的风险位点。虽然这些位点中的任何一个变异对疾病风险的影响都相对较小,通常只增加不到25%的风险,但其意义重大。此外,许多GWAS中检测到的遗传多态性位于基因组的非编码区域。因此,尽管已确定了108个风险基因座,但尚未完全明确哪些基因与这些风险变异相关。在某些情况下,变异与特定基因的距离足够近,可以合理推测它们之间的关系;在其他情况下,这些关系仍有待进一步研究确定。
与精神分裂症风险相关的基因为理解该疾病的生物学基础提供了重要起点。例如,自20世纪90年代后期以来,研究表明一个名为主要组织相容性复合体(MHC)的区域与精神分裂症风险密切相关。在精神分裂症患者中,MHC区域显示出人类基因组中最强的全基因组关联研究(GWAS)信号。由于队列样本量大,研究人员能够深入分析这一强大的风险关联,将MHC区域的信号解析为三个不同的基因座(可能是三个不同的基因)。其中,一个编码补体C4因子的基因对疾病风险具有显著且明确的影响。史蒂文·麦卡罗和他的团队发现,C4基因座是一个自然的拷贝数变异案例,健康个体在C4基因拷贝数上存在显著差异,而C4A等位基因的表达水平与精神分裂症风险的增加相关。后续研究表明,C4基因敲除的小鼠在发育过程中存在突触修剪缺陷,这支持了一个假设:人类中C4A过度表达可能导致突触修剪过度,这一过程长期以来被认为与精神分裂症有关。
这一发现是将基因组学与疾病风险的潜在生物机制联系起来的一个重要例证。然而,即使携带最高风险C4单倍型且没有精神分裂症家族史的个体,其因该等位基因而罹患精神分裂症的概率也仅从1%增加到约1.3%。相比之下,有一级亲属患有精神分裂症的个体,其风险增加约10倍。这一发现显示了精神分裂症遗传研究的希望,同时也揭示了其局限性:从常见变异的成功鉴定到深入解析导致人类病理的具体机制之间仍然存在挑战。
除了确定多个特定的风险位点外,GWAS研究还发现,精神分裂症的风险是由许多常见等位基因的累加效应推动的。这些结果为探索基因型与表型关系提供了新的强大路径。研究表明,个体携带的风险等位基因数量会显著影响其患病风险。例如,在所谓的多基因风险评分中处于最高十分位数的人,其精神分裂症风险比普通人群高出8到20倍。虽然累积效应的生物学机制尚不清楚,但这一发现为研究与疾病进程和治疗反应相关的问题奠定了基础,并可能重新激发结合神经影像学与基因组学的研究兴趣。早期的常见变异研究曾因专注于生物学上合理的候选基因而存在局限性,导致结果的可靠性问题,而新的方法有望改善这一点。
此外,类似于孤独症谱系障碍研究中采用的高通量测序方法,精神分裂症研究中也开始应用这些技术并取得了初步成果。具体来说,外显子组测序在寻找罕见和新发风险等位基因方面取得了一些成功。然而,与孤独症谱系障碍相比,精神分裂症研究需要更大的队列来确定可能的基因破坏突变的统计学显著性,这表明这些变异在精神分裂症中的整体影响可能较小。迄今为止,这些研究已经鉴定出一些与精神分裂症相关的风险基因,并涉及关键的神经生物学途径。特别是,最近的外显子组研究揭示了活性调节的细胞骨架复合体中的分子,以及与精神分裂症发病机制相关的组蛋白H3赖氨酸4特异性甲基转移酶相关的基因组结构域的重要性。
2.8 神经精神疾病遗传基础的见解
基因在行为的许多方面都起着重要作用。即使是分开抚养的双胞胎,也在性格特质和精神疾病方面表现出显著的相似性。家畜和实验室动物可以通过培育展现出特定的、稳定的行为特征;此外,我们对神经发育和精神疾病的广泛遗传变异的贡献也在不断加深理解。
一系列平行的发展为我们提供了一个前所未有的机会去理解基因、大脑和行为之间的关系。用于操作和研究模型系统的技术已经发生了革命性的变化;与此同时,在确定人类神经精神疾病的遗传风险因素方面也取得了显著进展。尽管这个领域仍处于发展的早期阶段,但已经有了多个成功的基因发现案例,并通过这些发现进一步深化了对相关生物学的理解。
最近神经发育和精神疾病遗传学研究中的一个引人注目的发现是,不同诊断范畴之间的遗传风险存在重叠。尽管生物学不完全遵循传统的分类诊断标准这一点并不令人意外,但如何追踪这些重叠效应并提出新的治疗策略,仍然是一个巨大的挑战。
此外,对于许多尚未取得显著进展的精神疾病,解决方案似乎也很简单:更大的投资和更大的样本量将带来更深入的洞察力。例如,最近对图雷特综合症和强迫症新发突变的研究表明,限制高置信度风险基因鉴定的关键因素是亲子三人组测序数据的可用性。同样,重度抑郁症的全基因组关联研究,直到最近样本量才达到足以确认统计学显著相关变异的水平。这些研究包括了数十万人,并且不出所料地发现了对疾病风险仅有微小影响的等位基因。
这一点突出了一个重要观点,即在行为、发育和精神疾病的基因组学研究中,没有一种方法能适用于所有情况。从模型系统的研究到罕见孟德尔疾病的解析,再到常见和罕见变异对常见疾病的贡献,当今可用的工具和研究机会是前所未有的。未来几年应该能够大幅加深我们对精神疾病和神经发育障碍的生物学理解,并有望带来可以帮助患者及其家庭的治疗方法。
2.9 本章要点回顾
1. 脆性X综合症、雷特综合症和威廉综合症等罕见遗传综合症为我们揭示了复杂人类行为的分子机制,提供了宝贵的见解。尽管相关研究仍有大量工作要完成,但这些研究已经挑战了认知和行为缺陷不可改变的观念,并证明了广泛应用模型系统在阐明保守生物学机制方面的效用。
2. 随着人类基因组测序、高通量基因组检测的发展,以及计算和方法学的进步,我们对人类行为和精神疾病遗传学的理解发生了深刻变革。精神分裂症和自闭症等几种典型疾病的研究取得了显著进展,已鉴定出数十个明确的遗传风险基因和染色体区域。
3. 过去十年里,精神病学遗传学和基因组学领域的发展揭示了传统候选基因研究的局限性。这类研究现已被全基因组扫描取代,涵盖了常见和罕见等位基因。通过结合严格的统计框架和共识统计阈值,这些研究正在产生高度可靠且可重复的结果。
4. 目前的研究表明,复杂行为综合症的遗传基础涵盖了多种类型的变异,包括常见和罕见、遗传和新发、生殖细胞和体细胞,以及序列和染色体结构变异。然而,这些不同类型的遗传变异对特定疾病的影响程度各不相同。
5. 人类行为遗传学的最新发现中一个引人注目的现象是,具有不同症状和病程的综合症之间存在遗传风险的重叠。理解相同突变如何在不同个体中导致多样化的表型结果,将是未来研究中的一大挑战。
6. 常见精神疾病的研究表明,遗传异质性非常高。这一现象,加上已确定的风险基因的生物学多效性,以及人类大脑发育的动态性和复杂性,预示着在从理解风险基因到理解行为之间存在重大挑战。同样,目前的研究表明,揭示风险基因的生物学功能与阐明行为综合症的病理生理学之间还存在重要的区别。
本文翻译整理自Principles of Neural Science, Sixth Edition,翻译初稿来自于GitHub/OpenHUTB,本公众号进行进一步校对排版后发布,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Principles of Neural Science, Sixth Edition
图文排版 | 李芋岭
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏