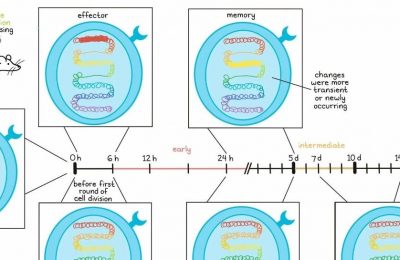
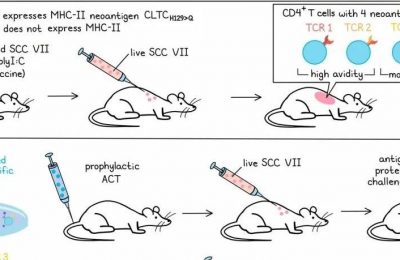
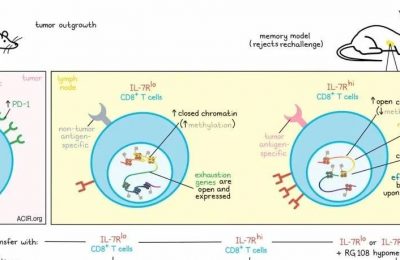
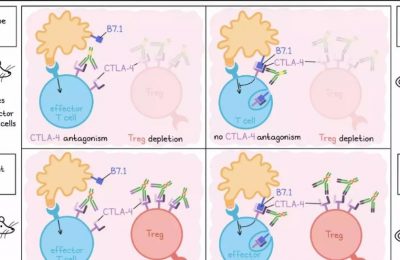
PD-1轴阻断已经被证明是一种成功的免疫治疗方法,适用于多种癌症类型,它被认为是通过扭转或预防T细胞耗竭来发挥…
PD-1轴阻断已经被证明是一种成功的免疫治疗方法,适用于多种癌症类型,它被认为是通过扭转或预防T细胞耗竭来发挥作用。然而,这种癌症免疫治疗的确切作用方式尚未完全阐明,最近的研究表明,PD-1轴阻断背后的机制可能比以前认为的更加复杂。Oh等人基于肿瘤内髓样细胞在其表面表达PD-L1这一点,开始探索不同髓样细胞群体在调节T细胞免疫和PD-1/PD-L1阻断中的作用。这些结果最近发表在《自然·癌症》上。
由于知道PD-L1和B7-1(CD28配体)在髓样细胞表面发生顺式相互作用,Oh等人开始探索破坏这种相互作用将如何影响内源性抗肿瘤反应。为了研究这个模型系统,研究人员生成了具有嵌合受体的Jurkat细胞,包括一个细胞外PD-1结构域、一个细胞内人类CD3ζ信号链和一个荧光素酶报告基因。表达PD-L1、B7-1或两者的K562细胞被用作人工抗原呈递细胞。在确认PD-L1和B7-1的顺式结合减少了PD-1信号,但不影响CD28信号后,研究人员创建了选择性抑制PD-L1和PD-1、PD-L1和B7-1,或两者之间相互作用的抗PD-L1抗体。正如预期的那样,选择性破坏PD-L1/B7-1相互作用使更多的PD-L1可用,并且在这个实验中信号增加,而阻断PD-L1/PD-1相互作用则产生相反的效应。
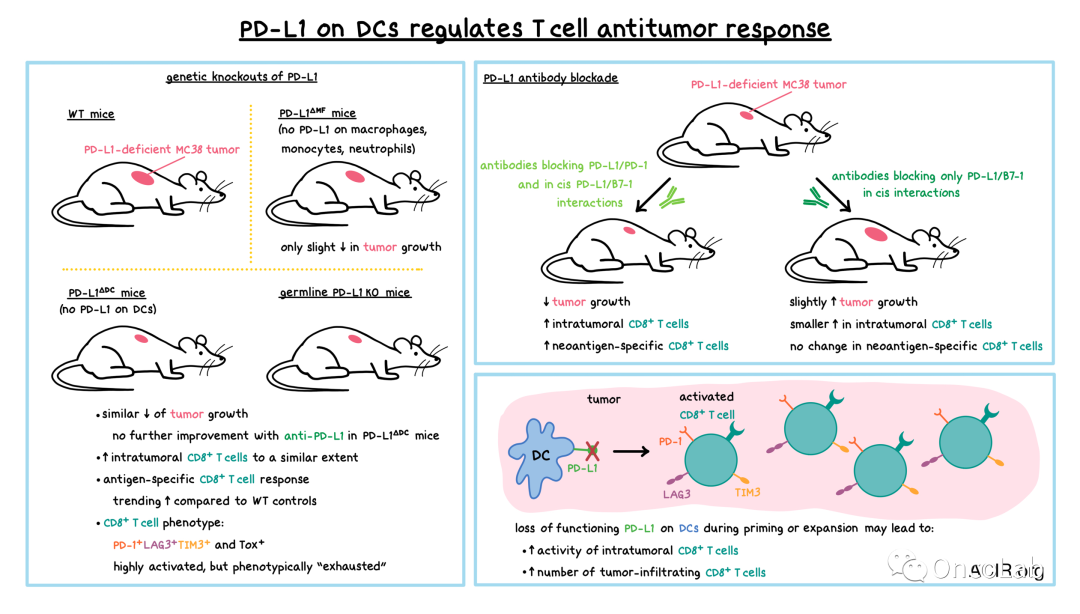
与体外观察一致,在PD-L1缺乏的MC38结直肠肿瘤小鼠中,PD-L1仅来自宿主细胞,抗体阻断PD-1/PD-L1和PD-L1/B7-1相互作用减少了肿瘤生长,而仅阻断PD-L1/B7-1相互作用略微加速了肿瘤生长,因为PD-L1的可用性增加了。阻断这两种相互作用增加了浸润肿瘤的CD8+ T细胞数量,包括特异性于肿瘤新抗原M86的CD8+ T细胞。相反,仅阻断PD-L1/B7-1相互作用导致CD8+ T细胞数量增加较小,并且M86特异性CD8+ T细胞没有增加。这些实验表明,抗原呈递细胞(APCs)上的PD-L1通过PD-1相互作用在抗肿瘤T细胞反应中发挥了作用。
在肿瘤接种后的第3、7和14天对肿瘤浸润性髓样细胞的分析显示,大多数髓样细胞是巨噬细胞,远远超过了负责交叉呈递的树突状细胞(DCs)。大多数肿瘤内或肿瘤引流淋巴结内的髓样细胞表达PD-L1,而不共表达B7-1(但仍然表达B7-2,后者不与PD-L1发生顺式相互作用),因此留下了大量的PD-L1可以与T细胞上的PD-1相互作用。大多数肿瘤内PD-L1+髓样细胞是巨噬细胞(约75%),而交叉呈递DC仅占该髓样细胞亚群的不到2%,直到肿瘤接种后的第14天。人类非小细胞肺癌(NSCLC)肿瘤的RNASeq数据中观察到了类似的PD-L1表达分布。然而,有趣的是,在NSCLC肿瘤中,成熟的DC的PD-L1(和B7-1)的基础表达水平最高,属于肿瘤内髓样细胞群体中最高水平。
为了确定哪些表达PD-L1的髓样细胞是抗肿瘤免疫的主要调节因子,Oh等人创建了具有DC特异性PD-L1缺陷(PD-L1ΔDC小鼠)的小鼠。PD-L1丢失最多的是CD11b-F4/80-DC亚群。研究人员还创建了PD-L1ΔMF小鼠,其中在巨噬细胞,单核细胞和中性粒细胞中删除了PD-L1,而DC基本上没有受到影响。在PD-L1缺陷的动物中,与野生型(WT)小鼠相比,完全PD-L1敲除(KO)的小鼠更好地控制了PD-L1缺陷的MC38肿瘤的生长,如先前观察到的那样。PD-L1ΔDC小鼠像PD-L1 KO小鼠一样有效地控制肿瘤,而PD-L1ΔMF小鼠则不太有效,与WT对照组相比仅略微减少了肿瘤生长。在携带PD-L1充足的荷瘤小鼠中也观察到了类似的结果。用阻止PD-L1 / B7-1相互作用或同时阻止PD-L1 / B7-1相互作用和PD-L1 / PD-1相互作用的抗-PD-L1抗体治疗携带肿瘤的PD-L1ΔDC小鼠并没有进一步增强肿瘤控制。这些结果表明,尽管它们出现频率较低,但与更丰富的巨噬细胞相比,在PD-L1 / PD-1调节抗肿瘤反应中,DCs扮演着更重要和关键的角色作为PD-L1来源。此外,在DC上而不是在巨噬细胞上的PD-L1 / B7-1的顺式相互作用起到了限制PD-1信号和激活T细胞的作用。
在接种后的第10天分析T细胞反应,发现PD-L1 KO和PD-L1ΔDC小鼠的PD-L1缺陷MC38肿瘤中CD8 + T细胞的频率和数量增加,与WT对照组相比。两种类型的小鼠中肿瘤内CD8 + T细胞的水平都有所增加。特异性抗原CD8 + T细胞反应是可变的,但在PD-L1 KO和PD-L1ΔDC小鼠中也呈上升趋势(通过测量疫苗诱导的SIINFEKL反应单独确认的趋势),进一步凸显了DC PD-L1在调节免疫反应中的重要作用。在所有三种类型的小鼠中,CD8 + T细胞表现出PD-1 + LAG3 + TIM3 +表型,通常与衰竭一致。
在接种后的第23天,PD-L1缺陷(PD-L1 KO和PD-L1ΔDC)小鼠的肿瘤比WT对照组小得多。在那个时间点,所有三种类型的小鼠中都观察到了新抗原特异性的肿瘤浸润CD8 + T细胞,以及高度活化的PD-1+LAG3+TIM3+ CD8+ T细胞(后者与对照组相比在PD-L1 KO和PD-L1ΔDC小鼠中增加)。PD-1+ Tox+ CD8+ T细胞在PD-L1 KO和PD-L1ΔDC小鼠中也有所增加。这些结果表明,在PD-L1 KO和PD-L1ΔDC小鼠与对照组相比,肿瘤内CD8 + T细胞高度活化。令人惊讶的是,尽管肿瘤控制得到改善,但CD8 + T细胞更有可能出现“衰竭”状态,这挑战了衰竭表型状态必然会降低抗肿瘤活性的观念。研究人员假设,在激活或扩增过程中DC上的PD-L1丢失可能会导致衰竭的肿瘤内CD8 + T细胞的活性增强,或者可能会增加浸润肿瘤的CD8 + T细胞数量,或者两者都可能起作用。此外,这些实验澄清了PD-L1不是诱导肿瘤内T细胞出现衰竭表型所必需的。
总的来说,Oh等人证明,在肿瘤内髓系细胞群中,表达PD-L1的DC通过PD-L1/B7-1在DC上的顺式相互作用和DC与T细胞之间的PD-L1/PD-1相互作用最终在调节抗肿瘤T细胞反应方面发挥关键作用。这些结果表明,PD-1/PD-L1阻断可能以比以前认为的更复杂的方式起作用:除了逆转或预防T细胞衰竭外,这也出乎意料地取决于DC/T细胞相互作用,PD-1轴阻断可能在T细胞激活和扩增期间发挥作用。需要更全面地了解这些机制,以优化抗PD-1/抗PD-L1癌症免疫治疗。
本周,第一作者Soyoung Oh回答了我们的问题。
是什么促使您研究这个问题?
长期以来,PD-1或PD-L1的阻断被认为是通过恢复耗竭型的肿瘤浸润CD8 + T细胞的功能来发挥作用。这种范式将PD-1/PD-L1阻断的机制集中在肿瘤中,尽管PD-L1可以由肿瘤细胞和免疫细胞表达,但普遍的观点是阻断肿瘤细胞上表达的PD-L1推动了这些治疗的功效。但是,我们对几个观察结果感到困惑,这些结果表明PD-L1在抗PD-L1治疗中的作用比肿瘤细胞上的PD-L1更为复杂。小鼠的研究表明,肿瘤和非肿瘤(例如免疫细胞)来源的PD-L1在调节抗肿瘤免疫方面发挥着不可替代的作用。在人类癌症中,PD-L1主要由浸润肿瘤免疫细胞表达,这也是对治疗反应的预测因子。我们想确定特定(非肿瘤性)细胞来源的PD-L1是否可能对调节抗肿瘤T细胞反应具有主导作用。尽管多种类型的免疫细胞都可以表达PD-L1,但我们最感兴趣的是髓系细胞的贡献,特别是树突状细胞上PD-L1的作用。值得注意的是,髓系细胞(而不是肿瘤细胞)也可以表达B7-1,这是我们最近发现受到PD-1信号抑制的CD28共刺激途径的配体。
对您来说,这项研究最令人惊讶的发现是什么?
虽然我怀疑树突状细胞将是PD-L1的重要来源,但令人惊讶的是,具有树突状细胞特异性PD-L1缺失的小鼠与全身PD-L1缺陷小鼠一样有效地控制肿瘤。更加引人注目地是,具有巨噬细胞特异性PD-L1缺失的小鼠在控制肿瘤方面不如DC特异性或全身PD-L1敲除动物有效。
最近工作之外,您学到的最酷的事情是什么?
我的五岁儿子痴迷于关于动物的事实书。由于和他一起阅读,我最近了解到了“不死水母”Turritopsis dohrnii。在某些条件下,这种物种可以从其成熟的成年状态(水母)转变为不成熟的、分化程度较低的状态(多肉)。令人难以置信的是,Turritopsis dohrnii似乎没有限制地进行这种转分化过程的次数。
来源 | ACIR.ORG & Nat Cancer
▉ 强烈推荐
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号: OncoLab




 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏