OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

1. 表观遗传相关肿瘤抗原
Sebastian Amigorena – 巴黎法国皮屈里研究所
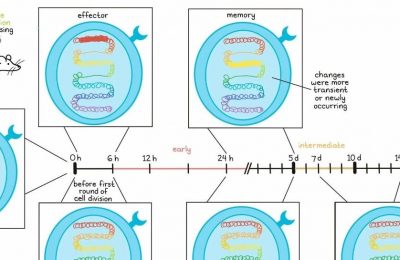
为了丰富有潜力对抗肿瘤的抗原库,Sebastian Amigorena及其研究团队对“暗基因组”(非常规转录的基因组片段)进行了深入研究。暗基因组虽然在正常情况下不被转录,但在肿瘤细胞中,由于调控机制失常,这些基因会异常地被表达出来。
Amigorena的研究特别关注的是肿瘤驱动的表观遗传学失调,这种失调导致了原本被抑制的转座元件(TEs)的激活,以及肿瘤细胞中剪接机制的广泛改变,从而产生新的抗原。这些转座元件广泛分布在基因组中的典型蛋白编码基因附近和内部。TEs的解压和新的剪接事件可能产生异常剪接的融合产物(被称为“JETs”;Junctions of Exons with Transposable elements),这些融合产物包含新的融合抗原。
在Amigorena先前的研究中,他描述了一个生物信息学流程,该流程用于在小鼠肿瘤细胞系中搜索这种新的转录本,并成功预测出了一系列具有肿瘤和组织特异性的候选抗原。通过基于质谱的免疫肽组学,他们检测出了与预测抗原相匹配的肽段,其中一些肽段在肿瘤携带的动物中被发现,并且许多抗原在接种预防性疫苗后能够控制肿瘤的生长。通过敲除表观遗传调控因子Setbp1,他们确认了JETs的表观遗传学起源,并在B16-OVA模型中延缓了肿瘤的生长。
抗PD-L1疗法显著提高了这种抗肿瘤效果,并诱导了针对JETs的特异性T细胞反应。在他们最近的研究中,他们应用了类似的流程于人类肿瘤样本,并确定了具有组织和肿瘤特异性的JETs表达。在分析了600个肺癌样本后,他们确定了一些普遍存在、肿瘤特异性和肿瘤相关的JETs,这些JETs在肿瘤邻近样本或正常组织GTEX数据库中的表达较低。
他们对17个新鲜肺癌标本进行了深入的质谱免疫肽组学分析,发现了多个HLA-I类分子呈递的肽段。对应的肿瘤浸润淋巴细胞(TILs)分析显示,他们在体外直接检测到了多个CD8+ T细胞反应(对于32个测试的肽段中的5个),并在体外刺激扩增后检测到了更多的CD8+ T细胞(对于32个肽段中的19个)。
在研究总结中,Amigorena描述了他与MNEMO Therapeutics的合作,他们的目标是发现针对与HLA分子呈递的人类JETs肽段的单链抗体,从而开发出具有T细胞双特异性和CAR T细胞的新型药物。激动人心的数据表明,他们已经在自然表达的细胞系中,以及体外和体内的实验中,实现了超高分辨率的免疫荧光检测,展现出了这种策略的可行性和有效性。
2. 靶向肿瘤微环境中无所不在的癌胎糖胺聚糖
Ali Salanti – 哥本哈根大学,丹麦哥本哈根
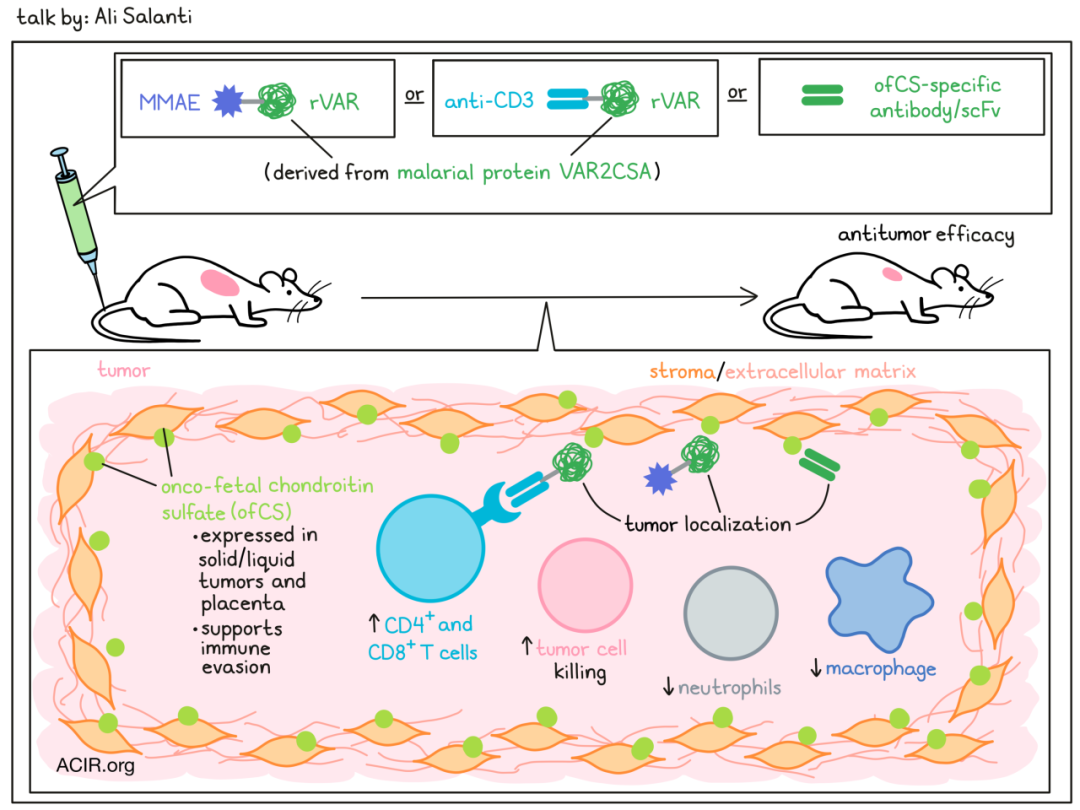
阿里·萨兰蒂(Ali Salanti)是一位疟疾研究者,他在研究过程中做出了一项引人入胜的发现。他发现,恶性疟原虫能够在感染的红细胞中表达一种名为VAR2CSA的特有疟疾编码细胞表面蛋白。这种蛋白质可以与在胎儿发育期间仅在胎盘中表达的特定类型软骨硫酸酯(CS)结合,为寄生虫提供了一个新的生存空间,使其能够避免在脾脏中被清除。胎盘中的这种独特CS模式可以形成细胞因子的储存库,促使快速侵害性生长,并使滋养层免受免疫系统攻击。
令人惊讶的是,这种特殊的CS特征也出现在恶性肿瘤细胞中。已经证明,重组的VAR2CSA(rVAR2)可以与几乎所有类型的肿瘤细胞结合,但与正常细胞(除胎盘外)的结合几乎没有,这将复杂的继发性CS修饰标识为一个胎儿型肿瘤抗原(ofCS)。在小鼠中,通过静脉注射的rVAR2能定位到肿瘤,并当与微管抑制剂MMAE结合时,能够杀死肿瘤细胞。
为了降低疟疾蛋白的免疫原性并延长此类治疗的半衰期,萨兰蒂致力于开发针对ofCS的特异性抗体。尽管在许多物种中寻找这种抗体显得极具挑战性,但萨兰蒂和他的团队最终成功筛选出大量的噬菌体展示文库,并鉴定出两种单克隆抗体,它们能够与人类和小鼠的ofCS具有高亲和性和特异性结合。
更加精准的实验结果确认,ofCS scFv可以与恶性组织中的细胞基质和细胞外基质结合,但在含有高量CS的正常组织中并未出现结合。此外,血液系统肿瘤也被发现表达ofCS,萨兰蒂展示了抗ofCS与人类急性髓系白血病(AML)的结合,而不是与正常骨髓的结合。在患有胰腺癌的基因工程KpC小鼠中,ofCS scFvs能够标记早期肿瘤起始细胞。
为了阐明ofCS在肿瘤发展中的作用,萨兰蒂和他的团队敲除了一种用于生成ofCS所需的酶。敲除这种酶的肿瘤发现CD3+细胞的浸润更严重,子群分析显示从浸润中的中性粒细胞和巨噬细胞向CD4+和CD8+ T细胞的显著转变,并且肿瘤生长减少,这表明ofCS在肿瘤免疫逃逸中发挥了关键角色。
当将抗ofCS scFvs与微管抑制剂MMAE或抗CD3 scFv(生成一种具有双特异性的T细胞结合抗体)结合后,在体内显示出肿瘤定位和抗肿瘤活性,包括产生免疫记忆。在这些实验过程中,没有观察到体重减轻的现象。
目前,已经计划进行0期研究,以确定药物的剂量和药代动力学,为之后的1期试验提供必要的信息。总的来说,萨兰蒂的这项研究为我们理解肿瘤的发展与免疫逃逸机制,以及开发新的抗肿瘤治疗策略提供了新的视角。
3. 针对成人弥漫性中线胶质瘤患者克隆驱动突变H3K27M的长肽疫苗
Niklas Grassl – 德国癌症研究中心DKFZ,德国海德堡
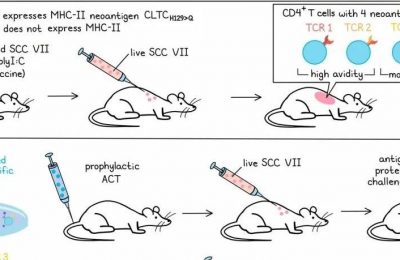
广泛中线胶质瘤(Diffuse Midline Glioma,DMG)主要发生在儿童和年轻成人中,总体生存期大约只有9个月。其中一种常见的突变是组蛋白H3 K27M,这是一种在DMG中反复出现的驱动性突变。研究表明,针对长H3K27M肽的疫苗可以抑制H3K27M阳性肿瘤在MHC人源化小鼠体内皮下移植后的生长。
尼克拉斯·格拉斯尔(Niklas Grassl)在一个首次人体试验中,针对8名患有进行性DMG的年轻成人进行了H3K27M长肽疫苗的实验,其中4名患者同时接受了抗PD-1治疗。这种治疗被良好地耐受,而唯一与疫苗相关的副作用是注射部位的反应。接种后,8名患者中有5名产生了针对H3 K27M的特异性免疫反应,表现出对突变肽的特异性。并未观察到与HLA类型的明显关联。
这个小组的总体生存期达到了令人鼓舞的12.8个月。在5名表现出疫苗诱导的T细胞反应的患者中,有4名出现了肿瘤的快速暂时性缩小,其中一名患者在接种后的30个月后仍存活,并且出现了早期的肿瘤伪进展。
通过近距离连接试验和肽激活试验中的抗MHC-II阻断,研究人员发现,识别HLA-DR的CD4+ T细胞在疫苗反应中起了关键作用。通过从长期生存患者的外周血中扩增的突变肽扩增T细胞,研究者鉴定出多个具有抗原反应性的T细胞受体(TCR)克隆。接种后,这些扩增的克隆在患者的外周血和脑脊液中的CD4+ T细胞中的频率显著增加。
最后,格拉斯尔指出,他们正在进行一项多中心试验,该试验将H3 K27M肽疫苗、放射治疗和抗PD-L1抗体结合用于新诊断的H3突变胶质瘤患者的治疗。
4. 针对检查点耐药非小细胞肺癌的替代共享新抗原(TEIPP)的I/II期临床试验
Marij Welters – 莱顿大学医学中心,荷兰莱顿
在寻找新的共享抗原来源以应对非小细胞肺癌(NSCLC)的免疫治疗耐药性时,Marij Welters描绘了一种弱化免疫逃逸机制的策略。肿瘤借助多种方式躲避免疫系统的打击,但肿瘤的遗传不稳定性和免疫系统对其强烈压力常常导致抗原呈递降低。这通常涉及到抗原呈递相关的转运蛋白(TAP)的下调,阻断了主要组织相容性复合体(MHC)对典型表位的呈递。然而,缺乏典型的TAP依赖路径允许其他在内质网中存在的肽段进入竞争,与MHC成功结合。这些肽段被称为与肽处理受损相关的T细胞表位(TEIPP)。
TEIPP来源于非突变的蛋白质组,但它们已成功避开了中枢耐受,因此可能是高免疫原性的共享“新抗原”,可用于对抗一些已经逃逸的肿瘤。Welters的团队为NSCLC样本建立了一个流程,预测N末端信号和C末端尾肽(已知是TEIPP肽的富集源)与MHC的结合能力,分析TAP缺乏的肿瘤细胞和正常健康组织的免疫肽谱,并鉴定出反应性T细胞和T细胞受体(TCR)。
在此类研究中,他们已成功鉴定出一种来自LRPAP1的肽段,作为合成长肽(SLP)疫苗,通过进行异构性锚定残基(S>V)的改变,在体外对多个供体具有高免疫原性。Welters接着描述了近期一项临床疫苗接种研究的结果,该研究针对在免疫检查点阻断治疗后复发的非小细胞肺癌患者。
患者在3周间隔的3次接种中使用Montanide佐剂接种SLP。在前两个剂量水平上,已经证明了其安全性。在接种的12名患者中,有7名患者表现出了令人鼓舞的临床反应,并且通过使用dextramer染色和外周血细胞内细胞因子染色,检测到了针对LRPAP1的特异性多功能CD8+和CD4+ T细胞。
在一个NSCLC肿瘤细胞系中,通过敲除TAP1,可以使这些经过改造的肿瘤细胞被一名接种患者的已排序的CD8+Dextramer+ PBMCs识别,从而支持TEIPP疫苗接种作为对免疫逃逸肿瘤的潜在挽救疗法,这类肿瘤的抗原处理机制已受损。
5. cDC1在肺癌中驱动对内源性免疫原性新抗原的抗肿瘤免疫
Federica Benvenuti – 国际遗传工程与生物技术中心,意大利特里斯特
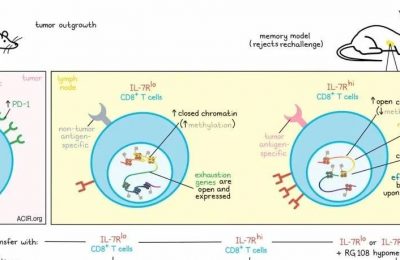
Federica Benvenuti的研究着重于类型1树突状细胞(cDC1)在选择以及产生对肿瘤新抗原的有效CD8+ T细胞反应中的角色。Benvenuti首先通过在KPcontrol(rasG12D/Trp53loss)细胞中敲除DNA修复途径的关键酶Mlh1,生成了一个新的细胞系KPneo,这个细胞系表达了非替代性的真正新抗原。
在KPneo细胞系中,研究人员鉴定出了26个新的抗原表位。将KPneo细胞植入到具备正常免疫功能的小鼠体内后,研究人员发现,与KP肿瘤细胞系相比,依赖于CD8+ T细胞的抗肿瘤免疫能够延缓肿瘤的生长,肿瘤内部的CD8+IFNγ+ T细胞数量大幅增加。同时,多个新抗原表位能够触发T细胞反应。
分析肿瘤内的cDC1s显示,与KPcontrol肿瘤相比,KPneo肿瘤中的cDC1数量显著增加。通过删除cDC1亚群(Batf3 KO)发现,新抗原对T细胞数量和表型的影响完全依赖于cDC1的存在。向肿瘤直接注射Flt3配体和polyI:C会增加KPneo肿瘤对抗PD-L1治疗的敏感性,然而,KPcontrol肿瘤对此并不敏感。根据在XCR1DTA小鼠中得到的结果,这种效应需要cDC1的存在。
分析人类非小细胞肺癌数据发现,相比于肿瘤突变负荷(TMB)较低的患者,TMB较高的患者中cDC1和CD8效应标志均较高,这一观察结果支持了KPneo和KPcontrol小鼠模型的研究结果。在肺部正位植入的KPneo肿瘤对抗PD-L1治疗的反应较弱,但通过使用Flt3L和激动剂CD40抗体(Flt3L/agOX40)刺激DC,肿瘤的生长显著受到抑制,对KPneo新抗原的反应显著增强。
在表达XCR1-venus的报告小鼠模型中,治疗后,KPneo肿瘤中浸润的cDC1和CD8+ T细胞同时增加。对未经处理和经过Flt3L/agOX40处理的肿瘤中的CD8+ T细胞进行单细胞分析显示,细胞亚群的频率存在差异,并且经过处理的肿瘤中,细胞的毒性及增殖能力增加。
对cDC亚群的分析显示,在治疗过程中,mregDCs大量减少,而cDC1和cDC2亚群整体上向较少耗竭/耐受原状态转变。这些结果表明,肿瘤内的DC亚群对响应的CD8+ T细胞的种类及其抗肿瘤功能的质量都有显著影响。
6. 胰腺癌 – 从临床发现到新的免疫疗法
Vinod Balachandran – 纪念斯隆凯特琳癌症中心,美国查尔斯顿
Vinod Balachandran的研究领域专注于胰腺导管腺癌(PDAC),这是一种典型的免疫”冷”瘤,其特点是突变负担较低、T细胞浸润较少且对免疫疗法具有抵抗性。然而,大约9%的PDAC肿瘤是免疫”热”瘤,患有这种肿瘤的患者具有较高的生存率。
为了确定如何最有效地激发新的免疫应答,增强已有的免疫应答,或者同时实现这两个目标,Balachandran和他的团队开发了一个评估新抗原质量的模型。这个模型通过预测MHC结合、潜在的T细胞受体(TCR)反应性以及与已知病毒抗原肽的相似性,来估计抗原的”自身性”和”非自身性”。他们发现,新抗原的质量而非数量更能有效地预测患者的生存率。他们还发现,高质量的新抗原特异性T细胞可以在一些胰腺癌的长期生存者的血液中被检测到,甚至可以持续存在长达十年之久。在这些长期生存者的复发性肿瘤中,高质量的新抗原很可能会被编辑,而自发产生的高质量新抗原可能会引发增加的新抗原特异性T细胞,从而延缓肿瘤的复发。
Balachandran和他的团队想要探索是否可以使用RNA疫苗来激发新的免疫应答。在一项合作研究中,他们开发了一种针对胰腺癌的个性化mRNA疫苗。他们进行了一项I期临床试验,其中患者在手术后的第6周接受atezolizumab治疗,然后从第9周开始连续8次接种个性化癌症疫苗,接着从第21周开始接受标准化疗,并在第46周进行最后的迟发性增强治疗。尽管COVID-19大流行对这项试验造成了干扰,但仍有16名接受atezolizumab治疗的19名患者继续接受疫苗接种,这证实了手术后生成和使用定制疫苗的可行性。
通过主要的ELISpot分析和确认性TCR测序CloneTrack测试,他们监测了疫苗诱导的T细胞应答,并发现在化疗后,强大的疫苗诱导应答仍能被保持。基于外周血中疫苗诱导的克隆轨迹进行聚类分析,研究人员发现,mRNA疫苗扩增的多克隆T细胞库包括在疫苗接种前无法检测到的克隆,与抗PD-L1扩增的克隆库明显不同。这种效应在疫苗增强剂后更为显著,进一步扩大了疫苗诱导的克隆,而非PD-L1诱导的克隆。他们还发现,一些长时间存活的患者体内存在的高质量新抗原特异性T细胞克隆在接受疫苗接种后显著增加。这些结果都表明,mRNA疫苗可以扩增新的免疫应答。
总的来说,他们的工作证明了个性化mRNA疫苗具有扩增新的免疫应答并维持已有应答的能力,这为胰腺癌的治疗提供了一种新的可能性。他们的研究也表明,新抗原质量的评估模型可以帮助预测患者的生存率,这是一个重要的临床工具。然而,这项研究还需要在更大的患者群体中进行验证,并且需要进一步研究如何最有效地利用这种治疗方法。
这项研究的一个重要意义在于,它不仅提供了一个新的方法来刺激免疫系统对胰腺癌的反应,而且还提供了一种方法来评估新抗原的质量,这可能有助于更好地理解和预测患者的生存率。
CIMT终身成就奖
CIMT终身成就奖汉斯-格奥尔格·拉门西(Hans-Georg Rammensee)是德国图宾根大学的知名教授,他在癌症免疫治疗领域的卓越贡献为他赢得了CIMT终身成就奖。拉门西教授揭示了肽段与MHC分子之间交互作用的规律,这极大地推动了我们对T细胞特异性识别、T细胞耐受性的理解,以及疫苗设计与功能发展的深入研究。
利用质谱技术和生物信息学手段,拉门西教授首次精确预测了自然呈现肽段,为抗原表位预测工具、T细胞分析的新技术开发,以及健康与疾病状态下MHC呈现肽段数据库的构建奠定了坚实的基础。
不仅如此,拉门西教授还将这些科研成果转化为实际应用,用于个性化治疗肽段和mRNA癌症疫苗的设计。他的研究亦催生了七家公司,包括Immatics Biotechnologies和CureVac等。总的来说,拉门西教授在免疫治疗领域的贡献对于科研和医疗实践都具有广泛而深远的影响。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏