6.1 介绍
用特异性单克隆抗体阻断表达在T细胞表面的免疫检查点受体而产生抗肿瘤免疫,这种方法使多种实体肿瘤和血液系统恶性肿瘤的在临床治疗中取得了极大进步。
T细胞在长时间抗原刺激后可上调免疫检查点受体的表达,这些受体的表达与T细胞功能障碍有关。针对细胞毒性T淋巴细胞相关蛋白4(CTLA-4)、程序性细胞死亡蛋白1(PD-1)或程序性死亡配体1(PD-L1)的单克隆抗体研究已成功应用于临床。
免疫肿瘤学研究延长了一些侵袭性肿瘤患者的存活期,如转移性黑色素瘤和非小细胞肺癌。然而,免疫肿瘤学虽然取得了成功,但仍有许多患者没有从抑制性受体阻断疗法中获益,这表明可能需要利用额外的免疫机制来引发有效的抗肿瘤反应。
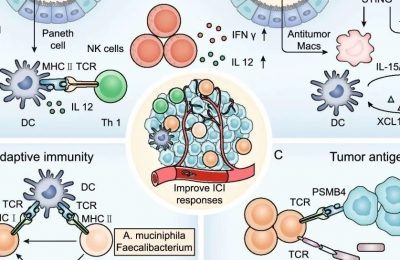
调节性T细胞(Tregs)通过限制炎症和自身免疫来维持外周免疫。然而,Tregs也在无意中限制了慢性病毒感染的清除,并导致肿瘤耐受,因为它们在限制组织损伤方面具有自我平衡的作用(Fig.6.1)。
在这一章中,我们在免疫肿瘤学的背景下讨论Tregs,首先是Tregs和Treg特异性细胞标志物的发现,接着描述Tregs的免疫抑制机制,并提出Tregs在限制抗肿瘤免疫中起作用的证据。
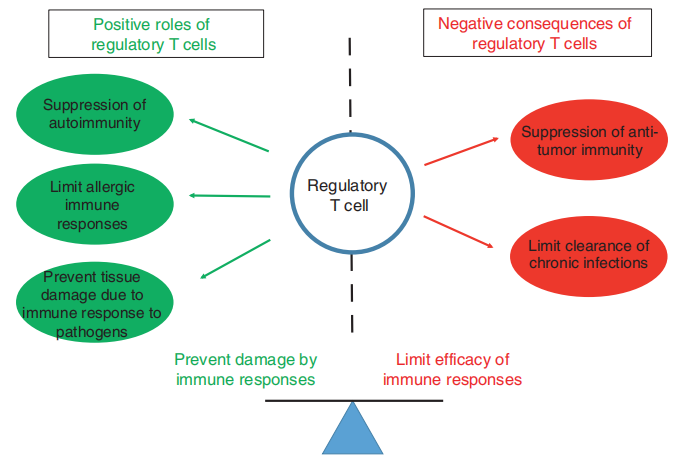
Fig.6.1 调节性T细胞(Tregs)限制自身免疫反应但同样也会抑制抗肿瘤免疫和慢性病毒感染的清除。
6.2 调节自身免疫的T细胞群的发现
Tregs首先是作为CD4+T细胞的一个亚群被发现的,负责防止自身免疫的发生。随后几十年的工作阐明了与Tregs相关的分子通路和表面受体,并使人们认识到它们在维持体内外周免疫耐受中所起的核心作用。因此,在靶向免疫治疗的背景下关于Tregs在癌症中的作用的研究持续推进。本章初步讨论了用于鉴定T细胞群体的表面标志物的发现,以及对Tregs在免疫稳态中的作用进行基本介绍。
6.2.1 CD4+T细胞对自身免疫的抑制作用
Tregs的重要性最早可以追溯到20世纪60年代中期在动物模型系统中关于自身免疫的研究中。这些早期的研究表明,切除新生小鼠的胸腺会导致许多系统出现严重的自身免疫,包括血液系统疾病、内分泌疾病、胃炎和卵巢炎/睾丸炎。这些研究表明,胸腺来源的T细胞在抑制多种组织的自身免疫反应中起着重要作用。更重要的是,早期研究还表明,需要一个T细胞亚群来防止自身免疫(Fig.6.2a)。
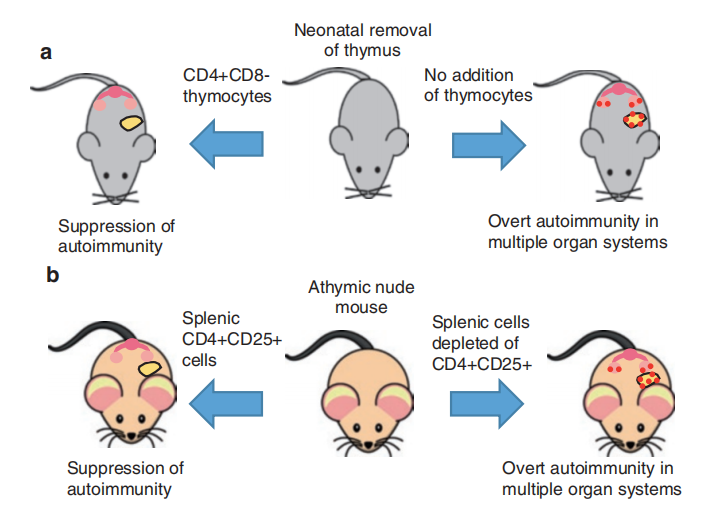
Fig.6.2 一种抑制自身免疫的T细胞亚群的发现。(a)当新生小鼠在出生后3天内切除胸腺时,卵巢和胰腺等不同器官系统会出现明显的自身免疫。然而,当CD4+ CD8− 胸腺细胞被用来重组这些小鼠时,这种自身免疫是可以被阻止的。(b)随后的研究表明,当自然裸鼠的脾细胞耗尽了CD4+CD25+T细胞后,在多个器官系统中发生了自身免疫。相反,用脾脏CD4+CD25+T细胞重组裸鼠会导致自身免疫功能受到抑制。这些实验表明,胸腺衍生的CD4+CD25+T细胞在出生后不久就会发育,对自身免疫的抑制产生效果。
6.2.2调节性T细胞的标志物
随后的研究试图确定这种抑制自身免疫的细胞的固有标记物。鉴定Tregs标记的研究首先观察到Tregs似乎是一个激活的T细胞群体。与T细胞活化和功能相关的细胞表面标志是高亲和力的IL-2受体α链(IL2Rα或CD25R)。通过比较CD4+CD25+和CD4+CD25−脾细胞的功能,发现了CD25在Treg生物学中的重要性。具有CD4+CD25+亚群的裸鼠会导致自身免疫抑制,而CD4+CD25−T细胞重组小鼠继续发生自身免疫(Fig.6.2b)。这项研究首次强调了CD25作为Tregs标记物的重要性。
这些观察表明CD25和IL-2对于Treg的发育和存活都是必不可少的。虽然IL-2通过CD25促进所有类型T细胞的存活和功能,但它对Tregs尤为重要。树突状细胞本身并不分泌IL-2,因此需要其他类型的细胞旁分泌IL-2来发挥其效应功能。在确定CD4+CD25+T细胞为抑制性细胞群之后,研究者试图进一步确定Tregs的标志物。
在小鼠身上发现了一种基因突变,导致了严重的自身免疫性疾病(称为皮屑),在人类中也发现了一种类似的疾病(称为X性连锁多内分泌腺病、肠病伴免疫失调综合征,简称IPEX),这促使研究人员考虑了该基因在Tregs中的作用。这个X连锁的基因(现在被称为Foxp3)被发现编码了一个关键的转录因子(Foxp3),该转录因子指导Tregs的形成和功能。
Foxp3通过控制与Tregs存活和发挥功能所需的关键基因的转录,在Tregs的发育和抑制功能中起关键作用。Foxp3驱动或增强与抑制相关的基因的转录,如CD25和CTLA-4,同时抑制炎症基因的转录,如IFN-γ和IL-2。Foxp3的表达本身是由Foxp3启动子的表观遗传低甲基化驱动的,这被认为是Tregs的一个标志。
虽然Foxp3是Tregs的特异性标记物,但值得注意的是,Foxp3也可以在激活的人类CD4+T细胞中瞬时表达。Foxp3在激活后的这种瞬时表达可能导致一些效应T细胞看起来像Foxp3+Treg,因此人类Treg的表型鉴定应该依赖于标记的组合(即CD25和Foxp3的共同表达或CD127的缺失,如下所述)。
此外,Foxp3不能用于从未经处理的小鼠或人类捐赠者的样本中分离Tregs,因为它是一种在细胞核中表达的转录因子。因此,小鼠研究中对Foxp3+细胞进行纯化通常是使用报告基因的方法。
最近,CD4+CD25+T细胞上IL-7受体CD127的缺失被认为是富含Foxp3+Tregs的人群的特征。记忆T细胞需要来自IL-7的信号来维持,因此表达高水平的CD127。相反,Tregs不表达CD127,Foxp3抑制了Il7r基因的转录,导致表达Foxp3的细胞上缺乏CD127。总的来说,这些标记物的发现促进了Tregs的纯化和分析。因此,鉴定出更多的标记物是有益的。
6.2.3 调节性T细胞来源:胸腺与外周
胸腺来源的Tregs(tTregs)在预防自身免疫中有重要的作用。然而,胸腺外也可以产生抑制性CD4+Foxp3+T细胞群。在体内胸腺外发育的Tregs被称为外周Tregs(pTregs)。在转化生长因子-β(TGF-β)存在的情况下,pTregs从外周适度剂量的抗原激活的初始CD4+T细胞分化而来。在此条件下,初始的CD4+T细胞被激活,导致Foxp3的诱导表达,不能分泌效应性细胞因子IFN-γ和IL-2,并在体外抑制效应T细胞的增殖。tTregs明显限制了体内的自身免疫,但pTregs在其中扮演的角色却还不太清楚。
pTregs可能的一个功能的是抑制对潜在破坏性抗原的免疫反应,例如肠道微生物区,而tTregs的自身反应性T细胞受体谱系不能识别这些抗原。或者,pTregs对于控制特定情况下的免疫反应可能很重要,例如对粘膜炎症的反应或控制胎儿-母体耐受。很明显,pTregs可以在特定情况下诱导,也可以在体内针对特定抗原诱导,但它们相对于tTregs在控制自身免疫中的作用以及最终在癌症免疫学中的作用还有待进一步研究。综上所述,tTregs对于限制体内自身免疫是必不可少的,而pTregs很可能在需要外源性抗原特异性Tregs的特定情况下起控制免疫激活的作用。
已经有很多人致力于对于预防自身免疫至关重要的CD4+T细胞群体的鉴别的研究。经过几十年的发展,人们对Tregs在抑制自身免疫中的作用、Tregs的起源和发展以及Foxp3在推动Treg的发展和功能中扮演的重要角色有了实质性的认识。Tregs细胞表面标记的鉴定也加速了它们在体外和体内的分析过程。
6.3 调节性T细胞抑制机制
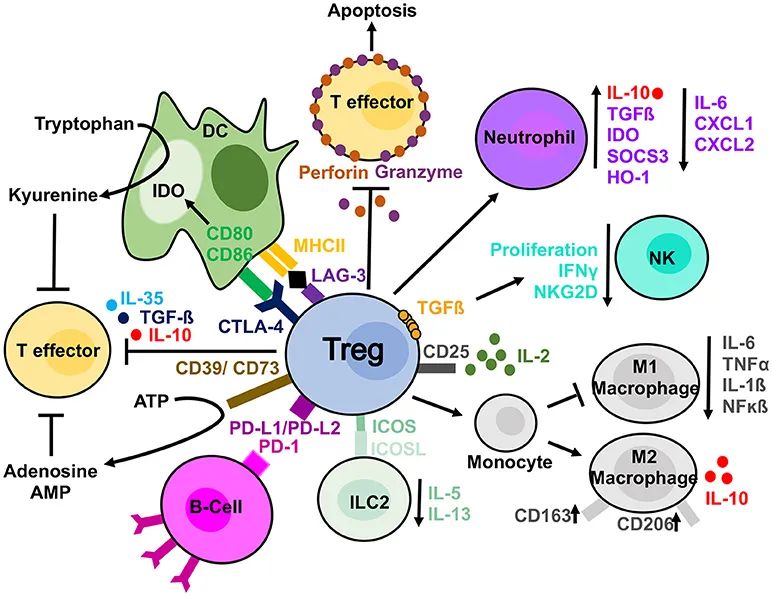
人们一直致力于了解Treg抑制免疫反应的机制。广义地说这个机制可以分为两类:依赖接触的机制和由可溶性因子介导的机制(Fig.6.3)。接触依赖性机制依赖于Tregs与被抑制的细胞的直接相互作用。可溶性的抑制机制取决于Treg细胞因子的分泌或Treg对效应细胞的代谢抑制。这两种类型的抑制机制也可以被局部微环境和细胞外途径调节和增强,如下所述。
6.3.1 依赖接触对免疫反应产生抑制
早期的研究表明,Tregs需要直接接触效应T细胞或抗原呈递细胞来介导抑制。Tregs通过与常规的CD4+CD25–T细胞或抗原提呈细胞的物理相互作用,限制效应T细胞产生IL-2,并阻止抗原提呈细胞对效应T细胞的共刺激。加入IL-2或抗CD28后,Treg介导的抑制消失,强调了Treg的抑制依赖于IL-2的剥夺和共刺激。这些初步的研究为更深入地分析Tregs抑制免疫反应所使用的接触依赖机制奠定了基础。
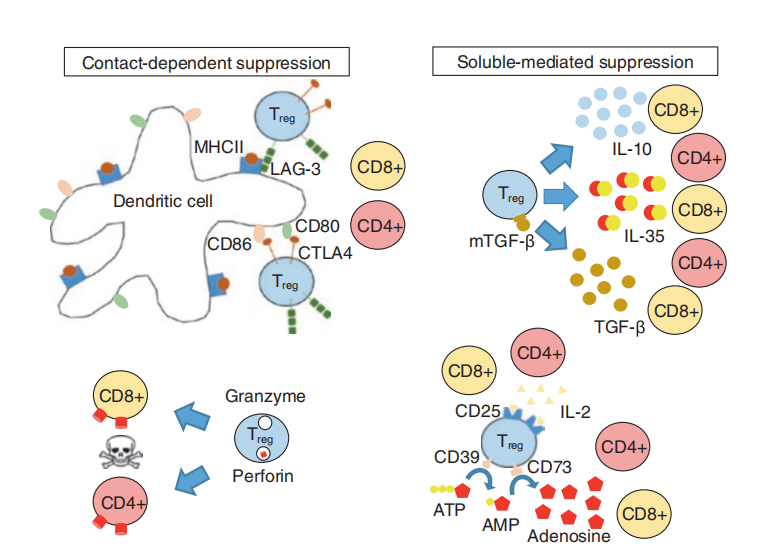
Fig.6.3 Tregs的免疫抑制机制。Treg通过接触依赖机制或可溶性介质抑制免疫反应。Tregs上的CTLA-4与树突状细胞上的CD80/CD86相互作用,或Tregs上的LAG-3与树突状细胞上的主要组织相容性复合体II相互作用,从而实现接触依赖性抑制。
Tregs表达的一个介导接触性抑制的表面分子是细胞毒性T淋巴细胞相关蛋白4(CTLA-4)。CTLA-4是防止全身性自身免疫所必需的,敲除小鼠该基因会导致自身免疫介导的多个组织的破坏,导致小鼠死亡。CTLA-4与CD28竞争结合树突状细胞表达的共刺激分子CD80和CD86。与CD28相比,CTLA-4以更高的亲和力与CD80/CD86结合,有效地消除了常规T细胞的共刺激作用。CTLA-4是由Tregs组成性表达的,并介导一种形式的接触依赖性抑制。Tregs还可以通过内吞作用和从抗原呈递细胞降解CD80/CD86来进一步剥夺效应T细胞的共刺激作用。在头颈部癌症患者中,靶向化疗导致肿瘤内CTLA-4+Tregs增加,这与不良的临床结果相关。CTLA-4+Tregs的接触依赖性免疫抑制是维持免疫稳态所必需的,CTLA-4+Tregs可能在抑制抗肿瘤免疫中发挥作用。
在Tregs上表达的另一种有助于接触性抑制的分子是淋巴细胞激活基因3(LAG-3)。在常规T细胞活化后,除了在Tregs上有表达外,LAG-3在T细胞表面也有上调。LAG-3与T细胞表面的T细胞受体(TCR)相关,并与MHC-II分子结合。LAG-3和MHC-II之间的这种相互作用导致抑制TCR/CD3介导的T细胞活化。LAG-3还可以通过与MHC-II相互作用直接调节树突状细胞的功能,并通过抑制树突状细胞在常规的CD4+T细胞中的激活信号来阻止树突状细胞成熟。根据LAG-3在Tregs接触依赖性抑制中的作用,在体外或体内阻断LAG-3可以减少Tregs的抑制。此外,小鼠LAG3基因缺失也导致抑制活性降低。在黑色素瘤和结直肠癌患者中,与健康捐赠者相比,LAG-3+Tregs在外周血中扩增,并且在有肿瘤转移的淋巴结中出现的频率比正常淋巴结高。体外实验还发现FOXP3+LAG-3+细胞能够分泌IL-10和TGF-β,并以接触依赖的方式抑制细胞增殖。
Tregs发挥效应功能的一种单独的接触依赖机制是通过释放含有颗粒酶和穿孔素的溶细胞颗粒。虽然这个特征通常仅限于CD8+T细胞,但Treg也可以表达颗粒酶和穿孔素,并可以通过穿孔素依赖的途径消除自体细胞。因此,表达颗粒酶和穿孔素的Tregs能够通过直接清除效应T细胞来抑制免疫反应。最后,一项研究证明了颗粒酶和穿孔素在抑制小鼠肿瘤模型抗肿瘤免疫中的重要性,强调了接触依赖性机制在促进肿瘤生长方面的重要性。
6.3.2 通过可溶性因子抑制免疫反应
Tregs发挥抑制功能的第二个机制是通过分泌、摄取或产生可溶性分子。如上所述,Tregs的特征是IL-2受体CD25的组成性表达,CD25的高表达导致Tregs优先结合IL-2。在炎症部位剥夺效应T细胞的IL-2会导致其效应功能的丧失和细胞凋亡。
Tregs用来抑制免疫反应的第二种可溶性机制是分泌细胞因子,如白细胞介素-10(IL-10)。特别是Tregs产生的IL-10在控制粘膜部位的炎症方面发挥了重要作用,而Tregs中缺乏IL10基因的小鼠会发生自发性结肠炎以及皮肤和肺部的炎症。IL-10可通过与异源四聚体IL-10受体复合物相互作用直接抑制效应T细胞,导致STAT3的激活和抗炎基因的转录。除了直接抑制效应T细胞外,IL-10还可以通过限制巨噬细胞产生炎性细胞因子的能力来抑制免疫反应。同样,IL-10也能阻止树突状细胞的成熟,并抑制其共刺激分子的表达。Tregs以其分泌IL-10的能力而闻名,但其他类型的细胞如某些条件下的巨噬细胞也会分泌IL-10。尽管IL-10是一种高度多效性的细胞因子,但它在Tregs介导的免疫抑制反应方面的作用尤为明显。
另一种由Tregs产生的重要细胞因子已被证明在免疫系统中发挥广泛而重要的作用,那就是TGF-β。与其他细胞因子不同,TGF-β最初被翻译为一种需要蛋白水解才能激活的非活性蛋白。失活的TGF-β通过与Tregs表面的GARP结合,与潜伏期相关肽(LAP)非共价结合。这种结合在膜上的TGF-β随后通过几种可能的蛋白水解途径被激活,从而使激活形式的TGF-β发挥其免疫抑制功能。TGF-β和Tregs之间的联系最早是在小鼠的实验性自身免疫性脑炎(EAE)模型中发现,口服耐受是通过喂食小鼠髓鞘碱性蛋白来诱导的。对渗入神经系统以促进耐受的CD4+T细胞的分析表明,这些细胞产生TGF-β,从而预防EAE。与其他Treg分子一样,敲除小鼠树突状细胞中的TGF-β会导致自身免疫性疾病的发生,这突显了TGF-β在免疫稳态中的重要性。TGF-β通过几种方式抑制效应T细胞反应,包括抑制IL-2的产生和CD8+T细胞中干扰素-γ和穿孔素的产生。在头颈部癌症患者中,Tregs分泌的TGF-β的重要作用已被证实。综上所述,Tregs分泌的TGF-β在维持免疫动态平衡和抑制抗肿瘤免疫方面起着重要作用。
Tregs产生的另一种重要的细胞因子是白细胞介素-35(IL-35),用于促进小鼠模型的免疫抑制。IL-35是IL-12异源二聚体细胞因子家族的成员,由一个IL-12α亚基和一个IL-27β/EBI3(EB病毒诱导基因3)亚基组成。这些细胞因子基因在小鼠Tregs亚群中组成性表达,但不在常规T细胞中表达,并在Treg激活后上调。IL-35对幼稚的CD4+T细胞具有抑制活性,并直接抑制常规细胞的分裂。像其他抑制性细胞因子一样,IL-35也可以驱动一种被称为iTr35的诱导性Treg亚群的发展,这种群体可以通过IL-35抑制效应T细胞。IL-35通过独特的IL12rβ2:gp130受体异二聚体和stat1:stat4异二聚体介导信号传导。在小鼠癌症模型中,IL-35最近被证明通过促进肿瘤微环境中T细胞的耗尽而在促进肿瘤生长中发挥重要作用。与高度激活的Tregs产生的IL-35增加一致,一只IL-35报告基因小鼠上发现IL-35+Tregs在肿瘤微环境中富集,中和IL-35或Treg特异性的Ebi3基因缺失导致抗肿瘤免疫增强,这是通过增强细胞增殖和效应功能以及改善效应T细胞的记忆细胞生成而介导的。Ebi3的限制性缺失还导致抑制性受体PD-1、LAG-3和TIM-3的表达减少,这表明IL-35可能通过上调多个抑制性受体来促进耗竭。
最后,Tregs还可以通过产生腺苷来调节免疫抑制,腺苷是一种不稳定的、高度抑制的分子。细胞外腺苷在体内的缺血和炎症部位聚集。在细胞外空间,腺苷是由Tregs通过分解ATP而产生的。Tregs上的胞外酶CD39和CD73,或者是与Tregs紧密相连的细胞,催化ATP分解为腺嘌呤。CD73在活化的T细胞和其他类型的细胞上广泛表达,而CD39的表达在很大程度上仅限于Tregs。炎症部位腺苷水平的升高通过与效应T细胞上的腺苷A2A受体或抗原提呈细胞上的腺苷A2B受体相互作用来抑制免疫反应。细胞外腺苷与任一受体的相互作用导致细胞内cAMP水平升高,并限制效应T细胞和抗原提呈细胞释放炎性细胞因子。因此,Tregs可以通过胞外酶将ATP分解成腺苷,从而限制局部炎性细胞运动的产生。
如本节所述,Tregs使用多种接触依赖和可溶性机制来抑制效应T细胞反应和抗原提呈细胞的发育和功能。鉴于自身免疫和过度免疫反应的有害影响,以及它们需要控制的细胞群体和效应机制的多样性,Tregs可能已经进化出多种免疫抑制机制,以在不同的环境中充分控制自身免疫和炎症。一个重要的问题是,某些机制是否在肿瘤中更主要或更优先地被Tregs利用,而不会实质上影响Tregs维持免疫稳态和外周耐受的能力,这更可能成为治疗的靶点。
6.3.3 增强抑制力和生存力
Tregs在不同的环境中发挥作用,并抑制各种类型的细胞。因此,它们的功能和生存很可能受到各种环境因素的调节或影响,其中许多我们可能还知之甚少或尚未定义。早期的研究表明Treg的表达是接触依赖性的。然而,这一观点与越来越多的人认识到细胞因子在调节Treg抑制中的重要性是不一致的。当最近的一项研究表明,Tregs本身的抑制并不完全依赖于接触,而是它们的抑制活性的增强依赖于接触时,这个难题就解决了。这项研究发现,Tregs与常规CD4+T细胞或抗原呈递细胞共培养,可以提高Tregs利用IL-10和IL-35抑制效应T细胞跨膜的能力。
Tregs表面的Nrp1(Nrp1)通过与Sema4a相互作用而增强Treg的功能和生存能力。Nrp1参与正常的神经和血管发育,也在肿瘤血管生成中发挥作用。在体外,通过Nrp1/Sema4a相互作用的信号对于Treg通过可溶性细胞因子介导的免疫抑制是必要的。Tregs上的Nrp1通过磷酸酶和张力蛋白同源物(PTEN)限制Akt(蛋白激酶B[PKB])的活性,从而稳定Treg的表型,提高其生存和功能。与Nrp1介导Treg增强相一致,小鼠Treg中Nrp1基因的消融导致体内抗肿瘤免疫显著增强,但不会导致明显的自身免疫或外周炎症。这些观察结果强调了Nrp1在稳定和增强Tregs在肿瘤微环境中的存活和抑制功能方面的独特作用。然而,Nrp1通路是否仅在肿瘤微环境中被利用,如果是,是否存在其他调节Treg存活和功能的机制仍有待确定。
— THE END —
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(下)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(上)
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA-I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡-OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频-中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程-中西医结合基础研究中心
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图-OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
中医中药系列
中成药传统方剂交叉检索数据库使用说明(免费开放使用)

关注本号~

加入读者交流群~

本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏