为了更好地理解为什么小鼠对肺部肿瘤产生的免疫应答弱于侧面肿瘤产生的免疫应答,Zagorulya等比较了它们各自…
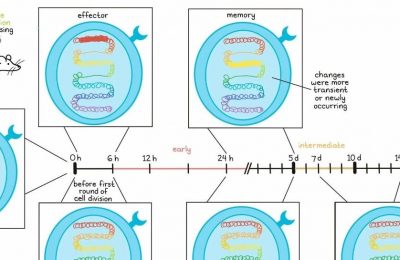
为了更好地理解为什么小鼠对肺部肿瘤产生的免疫应答弱于侧面肿瘤产生的免疫应答,Zagorulya等比较了它们各自的肿瘤引流淋巴结(纵隔淋巴结(mLN)和腹股沟淋巴结(iLN))中的免疫启动。随着他们揭示了这些位置特异性差异背后的机制,该团队发现在细胞毒性T细胞应答开始之前就发生的针对抗肿瘤免疫的挑战。
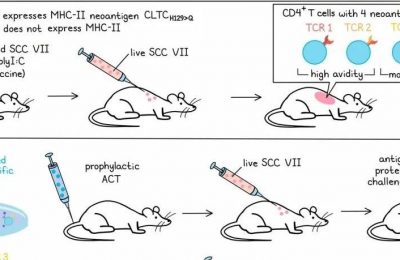
研究人员首先将KrasG12DTrp53-/- (KP)肺腺癌肿瘤原位移植到肺内,或者将其皮下移植到小鼠侧翼,并比较T细胞应答。KrasG12DTrp53-/- (KP)肺腺癌经过工程改造,表达与ZsGreen融合的SIINFEKL (ZsG)。虽然SIINFEKL特异性CD8+ T细胞在各层LN中聚集情况相似,但与iLN相比,mLN中的CD8+ T细胞活化程度较低,表达CD25、颗粒酶B和TIM3的细胞较少。
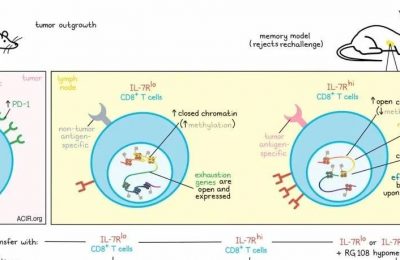
在确定这种差异效应不太可能是由TCR信号强度引起后,研究者将注意力转向抗原阳性(ZsG+)交叉呈递细胞DC1s,这是在两种肿瘤引流淋巴结(tdln)中启动T细胞所必需的。而DC1丰度、成熟程度(MHC-II、CCR7)和信号1(抗原提呈)在tdLNs之间相似,信号2(共刺激; CD80, CD86)和信号3(细胞因子; IL-12)表达受损。这一差异在初始小鼠中不明显,在体外启动研究中也不明显,提示这一效应并非DC1或mLN固有的,而是与肿瘤环境相关的。
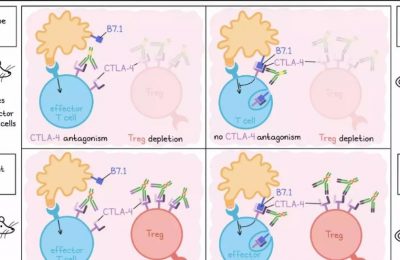
Zagorulya等发现,小鼠中去除Tregs可恢复两种tdLN中肿瘤反应性T细胞的CD25和颗粒酶B表达,但这一效应在mLN中启动的细胞中更明显。短暂清除Treg细胞还增加了ZsG+ DC1细胞CD80和CD86的表达,但不增加IL-12的产生。这些结果表明,Tregs可能通过抑制DC1s来抑制CD8+ T细胞的启动,这一假设在体外共培养的初始OT-I T细胞、ZsG+ DC1s和从引流肿瘤的mLN分离的Tregs中得到了证实。单细胞RNAseq进一步揭示,共培养中Tregs的存在降低了与效应功能相关的转录本的表达,并增加了与抑制效应T细胞分化和T细胞命运决定相关的转录本的表达。
比较来自mLN和iLN的Tregs的抑制能力,研究人员发现,来自mLN的Tregs更有效地抑制了在启动的CD8+ T细胞上表达的CD25和颗粒酶B,以及DC1s上的CD80、CD86和(较低程度)IL-12的表达(无论DC来源如何),提示treg的抑制能力存在组织特异性差异。当以抗CD28(激动剂)和IL-12的形式补充信号2和信号3时,可有效恢复对CD8+ T细胞的启动。这种效应在体内也得到了验证,在启动期间给予抗CD28和IL-12增加了肿瘤反应性CD8+ T细胞上的CD25和颗粒酶B。
Zagorulya等利用免疫荧光成像研究了Tregs如何抑制DC1和随后的T细胞启动,他们发现,在OT-I微生态中(以至少包含一个DC1的OT-I T细胞簇为中心的圆形区域),在mLNs中,Tregs和DC1之间的距离比在iLNs中更近,而在OT-I微生态外,它们之间的距离更远。用抗体阻断或敲除DC1s的MHC-II后,ZsG+ DC1s的CD80、CD86和IL-12的表达增加,CD8+ T细胞的启动恢复,提示Tregs通过直接与DC的MHC-II相互作用抑制DC1s的启动能力。
为了更好地理解为什么Treg对引流肿瘤的mLNs的抑制比对引流肿瘤的iLNs的抑制更强,研究者发现Treg的丰度和SIINFEKL反应性CD8+ T细胞:Treg的比值在两个部位之间具有可比性。配对的RNA和TCRseq显示,tdLNs中的Treg(而不是初始淋巴结)富集了一簇克隆扩增增加的“活化c1”Treg。在该Treg簇中,mLN细胞表达更多与免疫抑制、IFN应答和Th1极化相关的转录本,而iLN细胞表达更多与T细胞活化和Treg存活和稳定相关的转录本。在典型的Th1、Th2和Th17极化转录本中,研究人员发现了与Th1表型相关的Tbx21(编码T-bet)高表达。经典的Th2和Th17转录因子(分别为Gata3和RORγt)没有增加,进一步证实了Th1极化。此外,mLN中的Treg细胞表达更高水平的Treg标记物(NRP1、Helios)、效应激活分子(PD-1、CTLA-4)和抑制分子(NRP1、CTLA4、CD39、CD73),而iLN中的Treg细胞产生更高水平的TGFβ1和CD25,表明不同部位的Treg细胞具有不同的表型和抑制机制。
虽然研究发现DC1s是调节性T细胞向Th1表型极化所必需的,它介导了T-bet和T-bet+CXCR3+ Th1样效应性调节性T细胞的增加,但它们不能解释调节性T细胞极化的组织特异性差异。相反,研究人员假设IFN信号传导可能发挥了作用,因为IFN转录本优先富集于来自mLN的Treg中。对此,研究人员通过IFNγR敲除表明,IFN信号传导负责两个tdLN中T-bet、CXCR3和CD39的诱导,但这一程序主要在IFNγ更丰富的mLN中诱导。IFNγ水平的这一差异在初始小鼠中也很明显,但在无菌小鼠中达到平衡,提示mLN中IFNγ的增加与肺部的共生微生物相关。在肿瘤植入后早期使用抗体特异性清除IFNγ或短暂阻断IFNγ有效地减少了mLN中Th1样Treg并恢复了CD8+ T细胞的启动。
最后,Zagorulyaet等分析了人类黑色素瘤TILs的RNAseq数据,发现IFN应答程序的Treg表达以及TBX21或CXCR3转录本与ICB应答相关,而CD8+/Treg比例与ICB应答无关,这表明他们在小鼠中的发现可能也与患者相关。
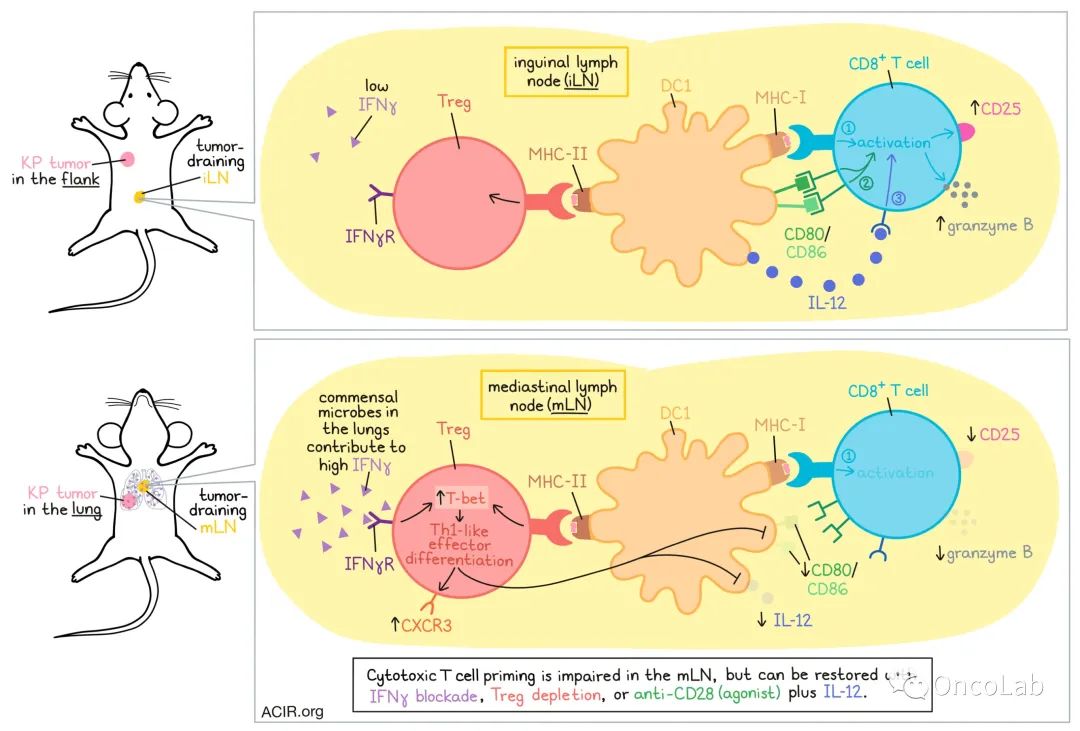
总之,这些结果表明,mLN中与局部肺组织微生物组相关的IFNγ增加,使Treg向Th1样效应表型极化,这依赖于DC1的存在。通过直接与DC1上的MHC-II相互作用,这些Th1样Treg抑制了DC1上的信号2和3,降低了它们对CD8+ T细胞的有效启动。清除Treg细胞、阻断IFNγ、使用抗CD28和IL-12补充信号2和3均是逆转细胞毒性T细胞应答的有效策略,为进一步探索提高抗肿瘤免疫开辟了新的途径。
▉ 强烈推荐
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号: OncoLab



 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏