针对PD-1/PD-L1轴的药物,如nivolumab,已经彻底改变了治疗转移性黑色素瘤患者的方式。然而,许多…
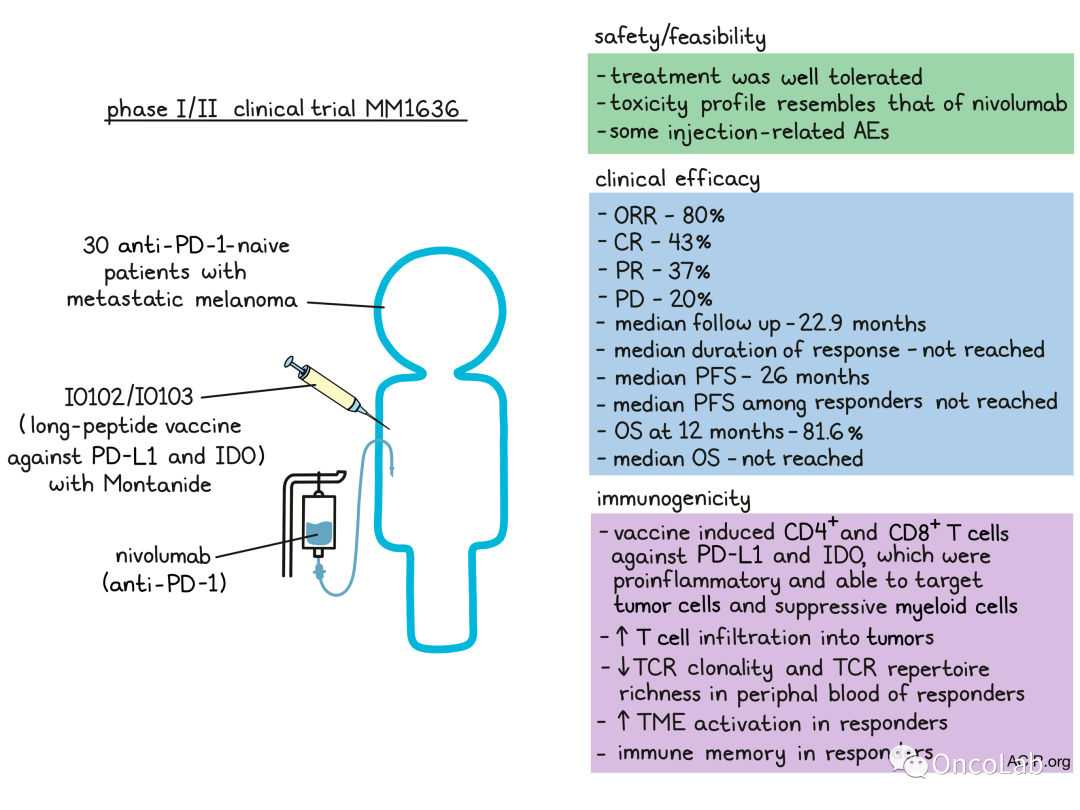
针对PD-1/PD-L1轴的药物,如nivolumab,已经彻底改变了治疗转移性黑色素瘤患者的方式。然而,许多患者仍然无法对疗法产生反应或者对疗法产生抗药性。为了调节肿瘤微环境(TME),增强抗PD-1疗法的反应,Kjeldsen和Lorentzen等人测试了一种免疫调节疫苗IO102/IO103,以诱导针对IDO和PD-L1的细胞毒性T细胞。这一策略旨在瞄准癌细胞和相关的抑制性免疫细胞,从而调节TME,以支持抗PD-1的反应。在一项I/II期临床试验MM1636中,这一策略得到了验证,主要终点是安全性和可行性,次要终点是临床疗效和免疫原性。Nature Medicine最近报道了该试验第一组患者的结果。
在MM1636试验中,对30名尚未接受抗PD-1治疗的转移性黑色素瘤患者进行了IDO/PD-L1长肽疫苗(IO102/IO103)联合佐剂Montanide的治疗。前6剂每隔一周给药一次,之后每隔四周给药。患者接受了3至15剂不等的治疗,平均为10.5剂。在疫苗接种期间,nivolumab每隔一周同时给药,疫苗接种后每隔四周给药。截止数据统计时间,仍有几名患者在继续治疗。
总的来说,研究的主要终点得到了满足,因为治疗是安全且耐受性良好的,毒性副作用与nivolumab单药治疗相似。1-2级不良事件(AEs)很常见。四名患者出现了3-4级不良事件,一名患者因nivolumab相关的毒性死亡。归因于疫苗的不良事件较少,仅限于疫苗注射部位的反应。两名患者因肉芽肿、压痛和与注射有关的疼痛决定停止治疗,这些情况最有可能是由于佐剂Montanide引起的。
在接受治疗的30名患者中,总体反应率(ORR)为80%,完全反应(CRs)为43%,部分反应(PRs)为37%。其余20%的患者病情恶化。在治疗初期观察到反应,30名患者中有22名在治疗12周的第一次评估时显示出反应迹象。部分反应的中位时间为75天,完全反应的中位时间为327天。PD-L1阳性患者的ORR为94.1%,PD-L1阴性患者的ORR为61.5%。经外部审查确定,ORR为76.6%,CR为53.3%,PR为23.3%,SD为3.3%。
为了评估IO102/IO103疫苗的贡献,研究人员确定了一个与29名患者匹配的历史对照组,这些患者接受了nivolumab单药治疗。与对照组相比,接受疫苗加nivolumab治疗的患者总体反应率更高(79.9%对比41.7%),完全反应的比例也更高(41.4%对比12%)。匹配对照组的反应率数据与接受nivolumab单药治疗的患者的大规模研究数据一致。
患者的随访时间长达35个月,中位随访时间为22.9个月。截至数据统计时间,尚未达到反应持续时间的中位数,87%的反应患者在12个月时无病进展。所有接受治疗的患者的中位PFS为26个月,反应患者的中位PFS尚未达到。12个月时的OS为81.6%,所有患者的中位OS尚未达到。在匹配的历史对照组中,中位PFS为8.3个月,中位OS为23.2个月。
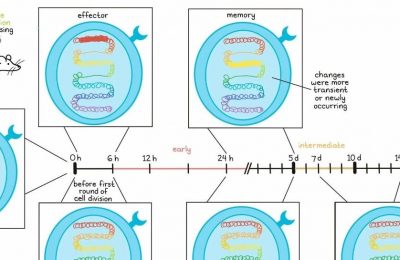
为了评估疫苗诱导的免疫反应,研究人员比较了治疗前后采集的PBMC样本。在治疗前,10名患者(33%)对IDO产生了T细胞反应,8名(27%)对PD-L1产生了反应,4名(13.3%)对两者都产生了反应。在疫苗接种期间,28名患者(93%)检测到IDO特异性反应,26名患者(86%)检测到PD-L1特异性反应。无论临床反应如何,患者均诱发了免疫反应,这表明其他因素也影响了临床反应。在几名经历了持久临床反应的患者中,免疫反应在最后一次疫苗接种后的3个月和6个月仍能维持,这提示产生了免疫记忆。
从PBMC样本中分离出的IDO-和PD-L1特异性T细胞经体外扩增,发现包括CD4+和CD8+T细胞,并显示出促炎特性,包括CD107a的表达和IFNγ和TNFα的分泌。疫苗特异性T细胞能够识别癌细胞系上的靶分子(只要它们也表达HLA-II)和肽脉冲的髓样细胞系。此外,针对用肿瘤细胞调节的介质诱导表达PD-L1和IDO的CD14+髓样细胞的反应得到了增强。疫苗特异性反应还可以在PBMC样本和皮肤中检测到。
接下来,研究人员使用患者的血液和活检样本来确定富集的IDO/PD-L1特异性T细胞克隆,并在疫苗接种后追踪克隆扩增。这表明,在不同时间点,IDO-和PD-L1特异性T细胞克隆在外周增加。尽管疫苗特异性克隆的富集与临床反应无关,但应答者确实表现出T细胞比例的增加以及TCR克隆性和TCR组库丰富度的降低,而非应答者则表现出相反的情况。此外,高度扩增的克隆在治疗前经常出现,并在稍后与肿瘤的治疗效果相关,这与外周扩增的克隆定位到肿瘤部位是一致的。在肿瘤活检样本中,应答患者在治疗后观察到T细胞的涌入。
在评估TME中其他治疗诱导的炎症时,Kjeldsen和Lorentzen等人发现在治疗后的活检中,与适应性免疫相关的基因(如T细胞激活、效应功能和细胞毒性)表达上调。他们还在肿瘤内发现了与检查点抑制剂相关基因(编码TIM3、IDO、PD-L1、PD-L2、PD-1和CTLA-4)的表达增加,并在应答者的肿瘤细胞中观察到PD-L1、IDO、MHC-I和MHC-II的上调。此外,在应答者活检的IHC分析中,活检中CD8+T细胞与PD-L1表达细胞之间的距离较非应答者缩短。
综上所述,这些早期临床数据表明,将IO102/IO103疫苗与nivolumab联合可以诱导针对PD-L1和IDO的T细胞反应,调节TME,并增强对抗PD-1的临床反应。尽管这是一个小型、单中心、非随机试验,但早期结果显示mPFS是nivolumab单独治疗的两倍以上,PD-L1阴性患者的ORR明显较高。更大规模的随机试验将揭示更多信息。
本周,丹麦癌症免疫治疗中心(CCIT-DK)的医学博士、博士生Cathrine Lund Lorentzen回答了我们的问题。
是什么促使您研究这个问题?
在丹麦癌症免疫治疗国家中心(CCIT-DK),我们的目标是将免疫检查点抑制剂(ICI)与一种能够增加响应率、为晚期黑素瘤患者提供持久反应且不引起联合ICI治疗中观察到的大量毒性的疗法相结合。CCIT-DK以前的研究显示,在肿瘤微环境和癌症患者及健康供体的外周血中,T细胞对PD-L1和IDO蛋白质存在自发活性反应。IDO和PD-L1特异性CD8+ T细胞可识别和杀死IDO+和/或PD-L1+肿瘤细胞以及免疫抑制细胞。
基于这些结果,我们计划了一项临床试验,将nivolumab与肽疫苗相结合,该疫苗旨在激活IDO和PD-L1特异性T细胞,诱导转移性黑素瘤患者的强大抗肿瘤免疫反应,而nivolumab则作为标准治疗手段。
对您来说,这项研究中最令人惊讶的发现是什么?
对于治疗前未受治疗的患者,nivolumab单药治疗的总体响应率(ORR)约为45%。本试验的ORR为80%,其中43%的患者获得完全缓解(CR)。经过32个月的中位随访,中位无进展生存期(PFS)为26个月,这是接受标准治疗的患者预期的两倍。令人惊讶的是,在纳入试验时基线预后不良的患者中,也观察到了令人印象深刻的响应率和生存数据。
在工作之外,您最近了解到的最酷的事情是什么?
我最近了解到英国獒犬是世界上最大、最重的犬种之一。我认识的一个人养了一只体重100公斤的英国獒犬。尽管体型庞大,但它经常和家里其他成员一起坐在沙发上。尽管我已经看过照片,但我仍然难以相信这么大的狗真的存在。
▉ 强烈推荐
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号: OncoLab




 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏