22.1 介绍
免疫检查点抑制剂是当前备受关注的癌症研究领域。它已在多种肿瘤中显示出了抗肿瘤活性和生存优势,包括转移性晚期尿路上皮癌(UC)。实际上,使用免疫检查点抑制剂治疗UC是有充分理由的,因为UC已经从静脉注射卡介苗(BCG)的免疫疗法中受益了40多年。尿路上皮癌是证明免疫检查点疗法有效的几种初始癌症之一,而免疫检查点治疗目前仍然是非肌层浸润性膀胱癌(NMIBC)患者的一线治疗方案。对于转移性尿路上皮癌的研究表明,免疫检查点阻断疗法将成为治疗晚期尿路上皮癌的重要疗法,可用于尿路上皮癌的各个阶段,以改善患者的症状。虽然在UC中有许多其他基于免疫的治疗方法正在进行研究,例如癌症疫苗和嵌合抗原受体,但本综述将重点介绍程序性细胞死亡1(PD-1)和程序性死亡配体1(PD-L1)抑制剂在UC中的应用,并简要介绍卡介苗在膀胱癌中的发展历史和应用。请注意,本章不涉及PD-1和PD-L1轴的生物学问题,因为后续会有专门的章节来关注这一领域。
22.2 卡介苗(BCG)
22.2.1 BCG的当前适应症
免疫治疗在早期膀胱癌中已经建立了40年,其中静脉内注射卡介苗用于非肌层浸润性膀胱癌(NMIBC)是最有效的治疗方法之一。卡介苗是一种牛分枝杆菌减毒活疫苗,最初是为预防结核病而开发的。经尿道切除膀胱肿瘤(TURBT)后进行的卡介苗免疫疗法被认为是免疫治疗在癌症治疗方面最成功的应用之一。
卡介苗在癌症治疗中的潜力可以追溯到1929年,当时的一项研究报告称,结核病患者的癌症发病率降低。后续研究发现,膀胱对BCG的反应与皮肤上的迟发性超敏反应雷同发生。一个经典的临床病例表明,皮内的BCG治疗对转移到膀胱的黑色素瘤具有一定的疗效。这促使研究人员对卡介苗在膀胱癌动物模型中的作用进行评估,结果显示每周六次静脉内加经皮给药可使膀胱肿瘤的复发率降低12倍。随后的第一个卡介苗对照试验显示,在54名可评估的患者中,肿瘤复发率有明显的下降。在风险更大的患者中也报告了类似的结果。两项Meta分析表明,卡介苗治疗可以预防或至少延缓中度和高度风险的NMIBC在TURBT后的肿瘤进展风险。
目前,卡介苗被推荐用于中危和高危肿瘤患者(3级、原位癌[CIS]、T1期)。使用卡介苗的理由包括预防或延缓复发,减少进展,以及避免根治性膀胱切除术。
22.2.2 BCG的作用机制
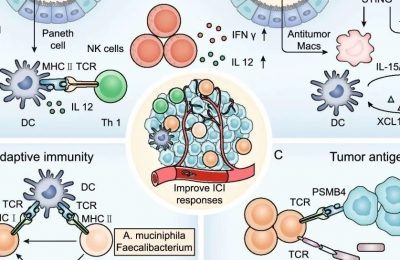
对于BCG诱导免疫介导的抗肿瘤反应的机制目前尚不完全清楚。BCG可以通过特异性纤维连接蛋白和整合素受体与膀胱肿瘤细胞和尿路上皮细胞粘附并被内化。内化的BCG特异性抗原会在肿瘤细胞表面表达,此时肿瘤细胞上的主要组织相容性复合体(MHC) II类抗原表达上调。然而,BCG的疗效需要一个有效的免疫系统和具有抗肿瘤免疫功能的T细胞亚型(如NK细胞、巨噬细胞、粒细胞和树突状细胞),以及各种细胞因子和白细胞介素。这些细胞会被招募到膀胱并在治疗后的尿液中大量出现。
BCG可以通过局部和系统的免疫反应来介导膀胱壁内的炎症反应,其中局部炎症反应与粒细胞、巨噬细胞和淋巴细胞,特别是与辅助T细胞的浸润有关。中性粒细胞和单核细胞产生的趋化因子是BCG初始反应的关键介质。中性粒细胞调节效应细胞(如单核细胞和CD4+T淋巴细胞)向膀胱壁的迁移。CD4+ T细胞被T细胞受体(TCR)激活,并诱导Th1细胞产生免疫反应。BCG动物实验已经证实,在肿瘤浸润淋巴细胞(TIL)中,CD4+和CD8+表型缺一不可,其中任何一个的缺失都会导致BCG介导的抗肿瘤活性的丧失。
在BCG治疗后,多种细胞因子被诱导,包括白细胞介素(IL)-1、IL-2、IL-6、IL-8、IL-10、IL-12、TNF-a、干扰素(IFN)g、粒细胞/巨噬细胞集落刺激因子和可溶性细胞间黏附分子I。为了获得最佳疗效,在患者第一次使用BCG治疗后,后续治疗中也要有计划地继续使用BCG。EORTC-GU组的Meta分析表明,只有持续接受BCG治疗的患者才会受益,但是这项分析无法确定哪种BCG维持治疗方案计划最有效。
22.2.3 BCG耐药机制
然而,使用BCG治疗的患者中有40-50%仍然会出现疾病进展或复发。那么问题来了,是什么导致了BCG治疗对部分NMIBC患者无效呢?以下提出了一些假设:
第一,虽然免疫细胞浸润广泛,但肿瘤相关抗原的特异性可能不够强。
第二,虽然存在抗原特异性T细胞反应,但在肿瘤微环境中,当NK细胞释放高浓度的Th1细胞因子(如IFNγ)时,PD-1/PD-L1上调,从而损害了T细胞的抗肿瘤反应。
肿瘤细胞PD-L1表达的增加可以预测局部尿路上皮癌的分期进展,与肿瘤分级无关。此外,PD-L1在原位癌(CIS)和BCG治疗失败的患者膀胱肉芽肿内表达水平较高。在BCG治疗前,约40%的CIS肿瘤存在PD-L1,但这些肿瘤细胞的PD-L1表达量相对较低(约占肿瘤细胞的5%)。
相反,在BCG治疗最终失败的CIS病例中,PD-L1表达水平高出15-20倍,且主要存在于BCG肉芽肿中。因此,膀胱肿瘤(包括CIS)表达的PD-L1可能为尿路上皮肿瘤细胞提供一种破坏宿主抗肿瘤免疫细胞并推动恶性肿瘤进展的分子机制。此外,BCG治疗后被招募到膀胱组织中的单核细胞对T细胞抑制性PD-L1的表达增加可能会导致随着时间的推移,BCG治疗效果下降。
在使用荧光素酶标记的小鼠膀胱癌细胞MB49(luc)进行研究时,发现MB49(luc)膀胱肿瘤的PD-L1表达高度阳性,并且阿维单抗(avelumab)诱导了显著的抗肿瘤作用。这些抗肿瘤作用更依赖于CD4+而不是CD8+ T细胞的存在,且这是由体内免疫细胞消耗的水平决定的。研究结果表明,在该膀胱肿瘤模型中,免疫抑制PD-1/PD-L1复合物可激活局部适应性的免疫反应,从而减缓肿瘤生长。
综上所述,这些数据表明PD-L1的存在可能与宿主免疫相关反应的损伤及膀胱癌的进展有关。这也表明PD-1/PD-L1相互作用具有潜在的生物学作用,可以作为NMIBC新的免疫治疗靶点。目前正在进行的几项一期临床试验旨在研究PD-1或PD-L1抑制剂在BCG难治性NMIBC患者及未接受过BCG治疗的高危NMIBC患者中的作用。
22.3 PD-1 和 PD-L1 抑制剂
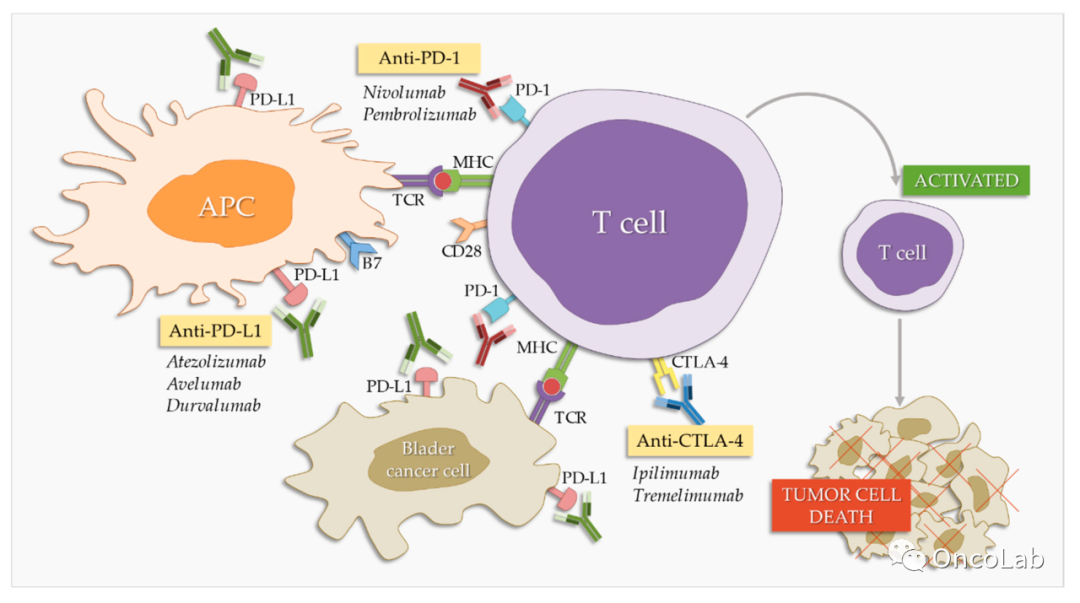
22.3.1 PD-1 和 PD-L1 抑制剂的作用原理
正如上述所述,BCG治疗NMIBC已经使用了数十年。除了BCG的临床疗效外,尿道癌的生物特征提示PD-1和PD-L1抑制剂可能对膀胱癌有效。首先,已经证实新抗原、癌症的免疫调节和PD-1轴阻断的临床疗效之间存在关联,包括黑色素瘤和肺癌在内的各种类型的癌症。在这些报道中,具有高肿瘤突变负荷和高新抗原的患者更容易对CTLA-4抑制剂或PD-1/PD-L1抑制剂产生反应。总体而言,这些研究表明免疫微环境中的总体突变负荷、新抗原负荷和细胞溶解标志物表达与免疫疗法的临床效益显著相关。
与肺癌一样,吸烟在膀胱癌患者中会诱发多种蛋白质水平的错误,导致肿瘤微环境中出现大量恶性的相关新抗原。基因组研究证实,尿路上皮癌具有高度突变的特点,每兆碱基突变中位数为8。当列出突变负荷从高到低的癌症时,尿路上皮癌排名第三,紧随黑色素瘤和肺癌之后。这些研究结果表明,PD-1/PD-L1抑制剂可能是治疗膀胱癌的有效方法之一。
其次,PD-L1在尿路上皮癌的所有阶段都很常见,并且与NMIBC和肌层浸润性膀胱肿瘤(MIBC)的不良预后有关。在接受根治性膀胱切除术的非转移性MIBC患者中,肿瘤细胞(TC)PD-L1状态与晚期疾病和生存率下降有关。一项针对302名患者的大型研究揭示了PD-L1状态与进行了膀胱切除术的器官局限性疾病患者的死亡风险增加之间存在相似的关联趋势。
最近的研究表明,免疫细胞(IC)PD-L1的表达与转移性铂类难治性尿路上皮癌患者的生存改善有关。另一项研究通过免疫组化(IHC)证实了PD-L1染色与顺铂新辅助化疗的疗效具有相关性。对于那些在新辅助化疗中没有反应的患者,通常在肿瘤中会有PD-L1的表达(40%),这提示这些患者可能适用于抗PD-L1疗法。
总之,这些数据表明PD-L1在肿瘤细胞或免疫细胞上的表达以及可以在尿路上皮癌中观察到的高突变负载,为研究尿路上皮癌的免疫检查点抑制剂奠定了基础。这一发现为开发治疗尿路上皮癌的新型免疫疗法提供了指导方向。
22.3.2 PD-1 和 PD-L1 抑制剂的概念验证研究
基于一项1期扩展试验的数据,阿替利珠单抗(Atezolizumab)在治疗尿路上皮癌领域取得了突破性进展,该试验对象为68例重度预处理的转移性尿路上皮癌患者。研究对免疫细胞和肿瘤细胞进行了评估,它们的PD-L1免疫组化评分为0、1、2、3,分别对应染色<1%、1-5%、5-10%和>10%。
在预先筛选的人群中,27%的患者的肿瘤浸润性免疫细胞PD-L1表达阳性(免疫组化评分为2或3)。首先,对浸润性肿瘤的免疫细胞进行PD-L1免疫组化,以验证PD-L1阳性患者可能对阿替利珠单抗具有特异性反应的假设。随后,该试验扩大到治疗无论PD-L1状态如何的患者,以确定PD-L1阴性的患者是否也会有反应。总共筛查了205例患者,其中23%的患者的免疫细胞PD-L1为阳性,4%的患者的肿瘤细胞PD-L1为阳性。
总的来说,68例重度预处理的转移性尿路上皮癌患者接受了治疗,并评估了该药物的安全性。对67例患者进行了疗效评估。大多数患者(93%)曾接受过以顺铂或卡铂为基础的化疗,近70%的患者曾接受过两次或两次以上的全身治疗。免疫组化评分为2/3的肿瘤患者的客观缓解率为43%,免疫组化评分为0或1的肿瘤患者的客观缓解率为11%。在该试验中,免疫组化评分2/3的肿瘤患者中,达到了52%的缓解率,其中包括7%的完全缓解率。且治疗效果持续时间相当长(对于IHC 2/3肿瘤的患者,持续时间为0.1+到30.3+周;对于IHC 0/1肿瘤的患者,持续时间为0.1+到6.0+周)。只有4%的患者出现了3级治疗相关不良事件,其中有虚弱、血小板减少和血磷下降各发生1例。
随着随访时间的延长,单药阿替利珠单抗在本1期研究的重度预处理转移性尿路上皮癌患者中表现出良好的耐受性,并观察到了在大量预处理的转移性尿路上皮癌人群中的良好临床效益。所有患者的2年总生存期(OS)率为30%,而免疫组化评分为2/3的肿瘤患者的2年总生存期率为43%,其化疗史生存率高于既往生存率。
这些早期结果使得阿替利珠单抗能够在更大规模的国际2期试验(IMVIGOR 2010年研究)中进行更大量的研究。在这项单臂、双队列、2期试验中,不能手术的局部晚期或转移性UC患者在接受过铂基化疗的基础上,每3周给予阿替利珠单抗1200 mg。该疗法下,患者的症状得到了缓解。共同的主要终点是独立审查机构根据RECIST v1.1评估的客观缓解率和研究者根据免疫修改的RECIST评估的客观缓解率,并按治疗意向进行分析。
在这项试验中,共有310名患者接受了阿替利珠单抗治疗。初步分析表明,与历史对照10%的化疗总缓解率相比,阿替利珠单抗治疗使每个预先指定的免疫细胞组(IC2/3:27%;IC1/2/3:18%)和所有患者(15%)的RECIST V1.1目标应答率显著提高。正如在1期研究中所指出的,许多有应答的患者表现出持久的应答。在中位时间约为2年的随访中,84%的应答者都出现了持续的应答。
在310例治疗患者中,只有5%的患者出现了3-4级免疫介导不良事件,其中肺炎、天门冬氨酸转氨酶升高、丙氨酸转氨酶升高、皮疹和呼吸困难是最常见的。
与此同时,在没有经过化疗治疗的转移性尿路上皮癌患者中研究了阿替利珠单抗在早期治疗中的疗效。大约40%的患者不适合接受以顺铂为基础的化疗,然后是接受以卡铂为基础的化疗,甚至只能接受支持性治疗。因为其出色的安全性,阿替利珠单抗在不适合接受以顺铂为基础的化疗的转移性尿路上皮癌患者中的作用正在研究中。主要的假设是早期使用阿替利珠单抗可以为这些患者提供良好的治疗效果。
因此,一项单臂、多中心、2期临床研究在123例既往未接受治疗的局部晚期或转移性尿路上皮癌患者中进行,这些患者均为不适合接受顺铂治疗的患者。主要终点是根据PD-L1表达在预先指定的亚组和所有患者中独立确定的客观缓解率。总的来说,有119人接受了一剂或多剂阿替利珠单抗治疗。客观疾病缓解率为23%,完全缓解率为9%。在试验结束后,27个出现缓解反应的患者中有19个患者的疾病缓解程度仍在加深。
中位生存期OS(50%的患者达到的生存时间)为15.9个月,远好于该人群接受化疗(约为9个月)的预期OS。同样,该治疗的耐受性良好,只有8%的患者经历了导致治疗中断的不良事件,12%的患者出现了免疫介导不良事件。
总的来说,阿替利珠单抗的1期和2期研究数据表明,在晚期尿路上皮癌患者中,PD-L1抑制剂具有良好的耐受性,在部分患者中具有显著的治疗活性。基于这些报道,阿替利珠单抗于2016年5月获得美国食品药品监督管理局(FDA)批准,用于治疗在含铂化疗期间或化疗后12个月内,或在手术治疗前或手术治疗后,病情恶化的局部晚期或转移性尿路上皮癌患者。
除了阿替利珠单抗,目前许多免疫检查点抑制剂也在研究中,包括PD-1抑制剂派姆单抗(pembrolizumab)、纳武单抗(nivolumab)以及PD-L1抑制剂德瓦鲁单抗(durvalumab)和阿维单抗(avelumab)。
总的来说,在1期和2期试验中,转移性UC化疗患者的总体缓解率为20-25%,早期缓解(在前两个月内)和持久缓解(在试验分析时通常没有达到)的结果一致(Table 22.1)。此外,PD-1和PD-L1抑制剂具有良好的安全性,治疗相关的3-4级事件很少(<15%),几乎没有治疗相关的死亡。
综上所述,这些数据超过了二线化疗通常观察到的数据,二线化疗的历史反应率为10%。此外,使用免疫检查点抑制剂的安全性也较好,这进一步支持了将其作为治疗早期或转移性UC的一种有效选择的潜力。
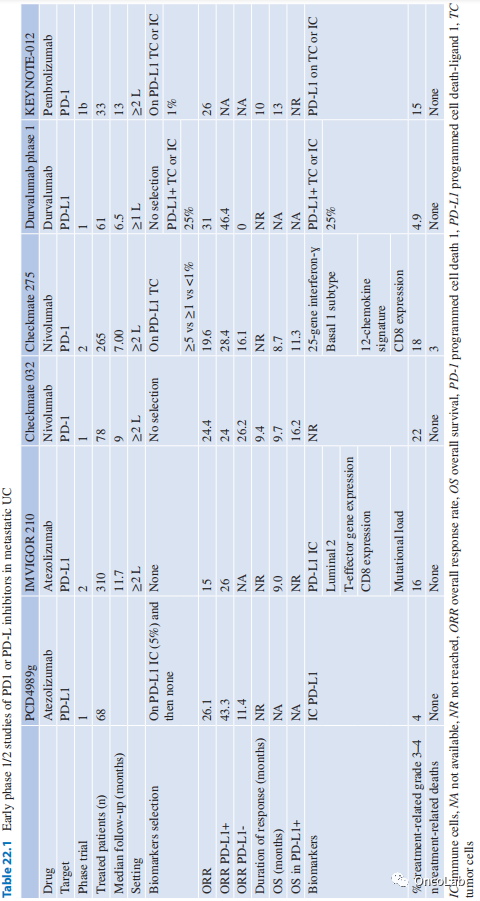
Table 22.1 PD1或PD-L抑制剂在转移性UC中的早期1/2期研究数据。其中IC表示免疫细胞,NA表示不可用,NR表示未达到,ORR代表总应答率,OS代表总生存率,PD-1代表程序性细胞死亡1,PD-L1代表程序性细胞死亡配体1,TC代表肿瘤细胞。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
作者 | Pernelle Lavaud and Yohann Loriot
初稿翻译 | 陈晓意 郭子 罗佳佳
编辑排版 | 林子畅
审核修改 | 王坤 胡珊
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏