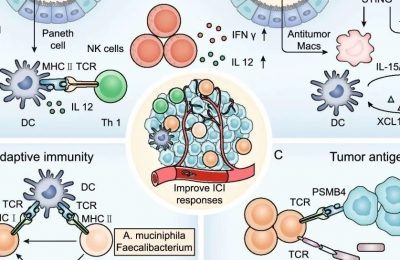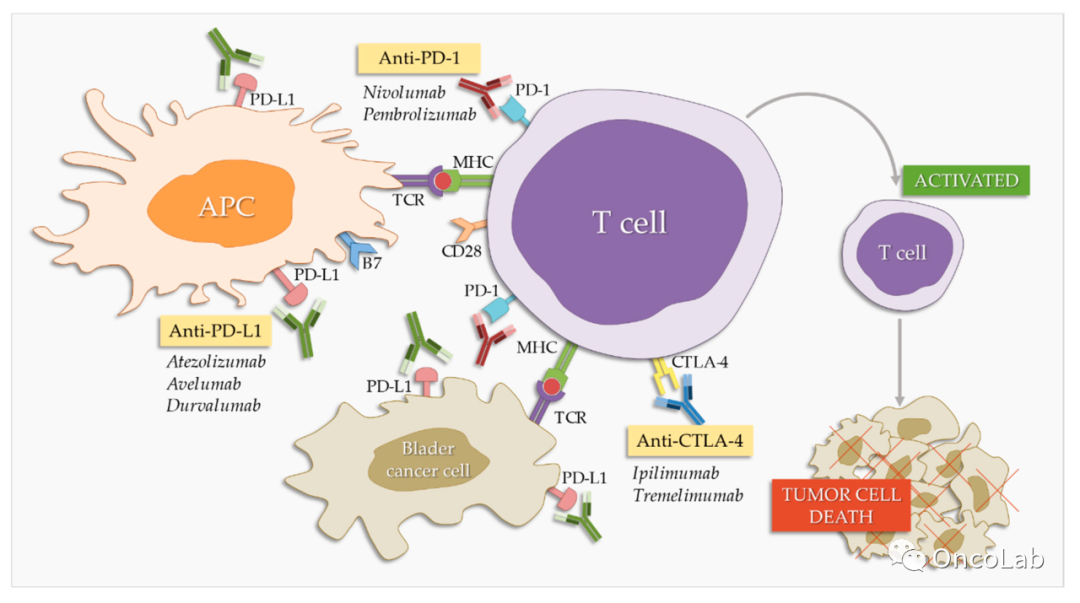
22.3.3 PD-1 和 PD-L1 抑制剂会改变转移性尿路上皮肿瘤的护理标准
研究人员基于早期研究数据进行了两项大型3期临床试验,旨在比较阿替利珠单抗或派姆单抗与化疗在转移性肿瘤治疗中的疗效。这些研究主要关注患者的总生存期和PD-L1阳性患者在二线(2L)或三线(3L)治疗中的总无进展生存期(PFS)。
其中,2016年报导的KEYNOTE-045试验在542例患者中比较了派姆单抗与化疗(文夫卢宁、紫杉醇或多烯紫杉醇)的疗效。在二次中期分析时,中位随访14.1个月后,派姆单抗组中位总生存期为10.3个月(95% CI: 8-11.8),而化疗组中位总生存期为7.4个月(95% IC: 6.1-8.3)。派姆单抗治疗将死亡风险降低了27%(HR: 0.73, 95% CI: 0.59-0.91, p = 0.0022)。
当集中分析肿瘤和周围免疫细胞上PD-L1表达水平的联合评分(CPS)≥10%的患者时,派姆单抗和化疗药物的死亡风险差异更大(HR:0.57,CI 95%:0.37-0.88,P=0.0048),但两种药物的无进展生存期没有显示出差异。派姆单抗的治疗缓解率接近20%(21.1%),明显优于化疗(11.4%),且缓解效果持久。CPS≥10%并未表现出更好的缓解率。
在KEYNOTE-045试验中,只有15%接受派姆单抗治疗的患者发生3-5级不良事件,其中4例死亡与派姆单抗有关。这是第一个证明PD-1/PD-L1抑制剂对尿路上皮癌具有疗效的三期临床试验。2017年,派姆单抗已被批准用于转移性尿路上皮癌患者的二线和三线治疗中。
至于将阿替利珠单抗与二线或三线化疗进行比较的3期试验结果,将会在2017年公布。
22.3.4 我们可以筛选出哪些患者更有可能对PD-1和PD-L1抑制剂作出反应吗?
虽然PD-1和PD-L1抑制剂已经被批准用于治疗转移性UC,但只有20%的患者会对检查点阻断免疫疗法产生反应。因此,为了更有效地应用免疫疗法治疗尿路上皮癌患者,我们需要采取一些策略。第一个策略是筛选可能会对这些药物产生反应的患者。与其他肿瘤类型一样,研究人员一直在探索可能预测免疫检查点阻断剂疗效的因素。然而,目前的研究结果并不一致,因此无法进行准确预测。例如,肿瘤类型(如膀胱癌/上呼吸道疾病)、性别(男性/女性)以及既往治疗路线的数量都与疗效无关。不过,根据KEYNOTE-045试验的报告,吸烟者更有可能从派姆单抗治疗中受益。除此之外,没有其他研究表明吸烟与预测患者的疗效有关。此外,转移性肿瘤的部位与疗效也有关系。只有淋巴结转移的患者对PD-1和PD-L1抑制剂的反应率高于内脏转移的患者。这也引发了一个问题,即特定的肿瘤部位微环境是否可以在预测疗效方面发挥作用。因此,我们需要进一步的研究来确定预测免疫检查点阻断疗效的合适因素,并帮助更多的患者从免疫疗法中受益。
目前已经发现了许多潜在的生物标志物,用于预测免疫治疗的疗效。这些标志物包括基于微环境和基于肿瘤细胞的标志物(Table 22.2)。最先进的预测PD-1和PD-L1抑制剂疗效的生物标志物包括突变负荷、肿瘤或免疫细胞PD-L1的表达水平以及肿瘤内免疫细胞的浸润程度。目前,PD-1和PD-L1的表达量尚未被认为是可靠且可复制的标志物,用于预测其疗效或机体对其耐药性。在二线治疗中,肿瘤细胞或免疫细胞上的PD-L1表达与机体对PD-1/PD-L1抑制剂的反应存在相关性,但此相关性尚不足以在临床实践中应用。
使用PD-1/PD-L1染色的一个主要缺点是免疫组化PD-L1阳性的评估方法存在异质性。目前,不同的抗体制造商已经开发出多种不同的检测方法作为辅助诊断。评估PD-L1的抗体具有不同的特性,这影响了不同研究间的比较。此外,还存在许多未解决的问题,例如PD-L1阳性染色的界定标准。大多数研究认为,在肿瘤细胞或免疫细胞中,PD-L1染色的细胞数应该大于5%(IHC染色评分2/3)才能判断为PD-L1阳性,但也有其他研究认为大于1%即为阳性界限。因此,迫切需要其他诊断来辅助诊断。蓝图计划将有助于在批准前阶段为PD-1/PD-L1辅助诊断特征建立证据基础。一旦测试被批准,产生的信息可以为批准后的研究奠定基础,帮助患者、医生和病理学家决定如何最好地利用测试结果做出治疗决策。
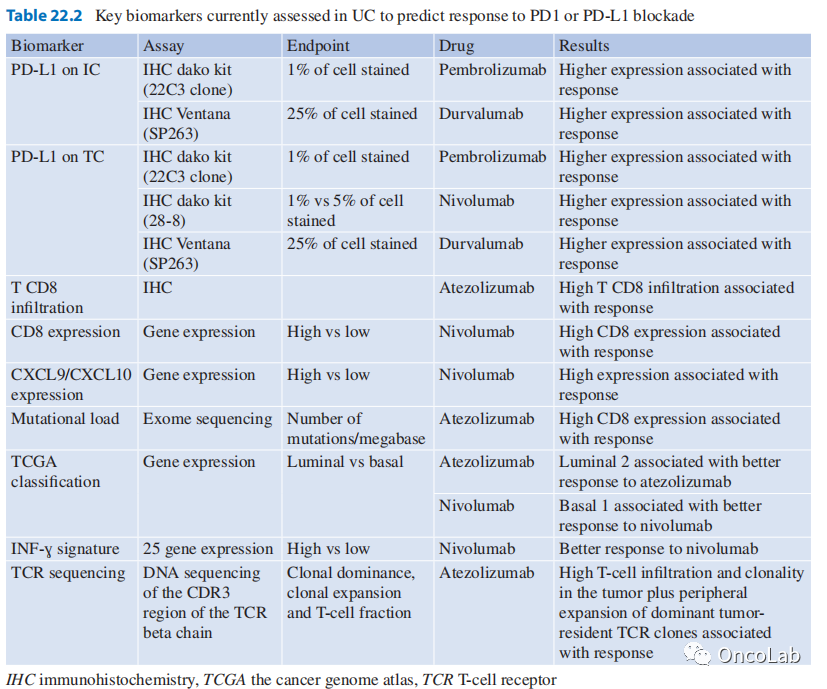
Table 22.2 目前在UC中评估预测PD1或PD-L1阻断反应的关键生物标志物。IHC, 免疫组化;TCGA, 癌症基因组图谱;TCR, T细胞受体。
根据癌症基因组图谱(TCGA)的分类,尿路上皮癌存在治疗效果与转录组特征之间的关联问题。最近的数据表明,肌层浸润性膀胱癌(MIBC)可以根据基因表达分为四种亚型,其中有两种腔内亚型(腔内1和腔内2)和两种基底亚型 (Fig 22.1)。探索性分析显示,在MIBC患者中,基底型(60%)患者的免疫细胞PD-L1表达高于腔内型(23%)患者。肿瘤细胞上PD-L1的表达仅在基底亚型中较高(基底亚型39%,腔内亚型4%)。
此外,CD8+T效应基因在腔内II型和基底亚型中都表达增加,而在腔内I型中表达不明显。值得一提的是,这些高表达CD8+T效应基因的亚型在阿替利珠单抗应答者中观察到较高的基线IFN-ɣ应答基因(较高水平的干扰素ɣ,由CD8+T细胞释放)。这些数据与Th1和CTL免疫反应是一致的。
所有TCGA亚型对阿替利珠单抗均有应答,但与其他亚型相比,腔内II型亚型的MIBC对阿替利珠单抗的应答明显更高。综上所述,这些数据表明这些MIBC亚型具有不同的肿瘤免疫特性,而不同的肿瘤免疫特性就导致了不同亚型MIBC对阿替利珠单抗的反应性不同:
-
腔内I型肿瘤具有较低的效应T细胞相关基因表达(“免疫荒漠”)
-
腔内II型有高效应T细胞表达和低基质基因表达(“炎症肿瘤”)
-
基底亚型高表达效应T细胞和基质基因(“免疫抑制”)
需要指出的是,这些初步数据与CheckMate 275研究中报道的PD-1抑制剂纳武单抗的数据并不完全一致。该研究显示肿瘤微环境中IFN-ɣ的含量与较高的应答率和较高的PD-L1表达相关。在基质I亚型的MIBC患者中IFN-ɣ表达的含量是最高的,该亚型患者的应答者比例也是最高,CXCL9或CXCL10表达最高。这些数据需要在研究阿替利珠单抗和派姆单抗的三期临床试验中进一步得到证实,这可能反映了PD-1/PD-L1抑制剂之间靶点分布的差异。
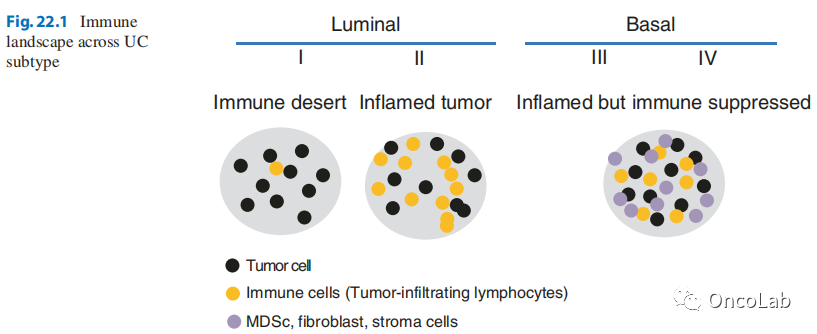
Fig 22.1 跨尿路上皮癌亚型的免疫景观
22.3.5 我们该如何增加PD-1/PD-L1免疫抑制疗法的临床疗效?
第二个待解决的问题是如何增加PD-1和PD-L1抑制剂的反应患者比例。晚期铂基化疗患者中,只有20%对PD-1阻断剂有反应。与其他肿瘤(如黑色素瘤或肺癌)一样,联合免疫疗法在膀胱肿瘤中可能比单一疗法更有效。联合免疫治疗已被证明比单药治疗更能提高临床疗效。例如,对晚期黑色素瘤患者同时给予纳武单抗和伊匹单抗比单药治疗产生更高的缓解率。联合免疫反应能为患者带来更有效、更持久的疗效。
评估CTLA-4和PD-1抑制剂联合应用的基本原理是,CTLA-4和PD-1的机制是相互独立的。这表明靶向两者都可能具有添加或协同活性,无论PD-L1阳性或PD-L1阴性人群。此外,CTLA-4抑制剂已被证明可上调PD-1,而PD-1也已被证明可上调CTLA-4。这为联合使用替西木单抗和德瓦鲁单抗提供了强有力的现实依据。目前正在进行的研究表明,PD-L1阴性的非小细胞肺癌患者接受PD-1抑制剂(纳武单抗或度伐利尤单抗)+ CTLA-4抑制剂(伊匹单抗或曲美木单抗)联合治疗比度伐利尤单抗单药治疗的缓解率(分别为30和70%)和疾病控制率(分别为10和42%)更高。这种方法目前正在尿路上皮癌患者中进行1/2期试验。
此外,正在进行的1期试验研究了以PD-1抑制剂或PD-L1抑制剂为骨架的其他免疫检查点抑制剂(如LAG-3、VISTA)或激活剂免疫检查点(如OX40、CD27)的组合。另一种策略是将化疗或放疗等DNA损伤剂与免疫检查点抑制剂相结合。理由是常规药物可能会增加肿瘤细胞中的突变负荷,从而导致患者在免疫检查点抑制剂有更高的响应率。
22.4 展望
早期的临床试验已经证明,在经过化疗治疗的尿路上皮癌患者中,免疫检查点抑制剂具有显著的疾病缓解率、持久的疗效以及良好的安全性。最近的三项临床试验表明,PD-1抑制剂可以改善致死性转移性尿路上皮癌患者的预后。考虑到这些研究数据,未来几个月内将会进行PD-1/PD-L1阻断剂在没有经过化疗治疗的转移性MIBC、非转移性MIBC,甚至在卡介苗治疗无反应的高级别非肌层浸润性膀胱癌(NMIBC)的疾病早期的潜在应用研究(Table 22.3)。
因此,PD-1和PD-L1抑制剂将成为未来基础免疫治疗的骨干,特别是在晚期尿路上皮癌患者中。未来PD-1和PD-L1抑制剂的发展需要与其他免疫抑制剂合理地组合使用。
然而,新的问题是如何提高可能受益于免疫检查点阻断疗法的患者数量。目前正在进行多期1期试验,评估各种联合治疗组合。理想情况下,这些药物组合应该基于潜在的肿瘤抗药机制。腔内I型肿瘤的特点是“免疫荒漠”和FGFR2和FGFR3基因畸变。这表明,通过化疗、放疗或FGFR抑制剂可诱导肿瘤细胞死亡,死亡的肿瘤细胞释放肿瘤抗原激活T细胞,导致对随后的免疫检查点抑制剂效果更加敏感。
另一种方法是在使用免疫检查点抑制剂之前,使用携带肿瘤特异性抗原的疫苗来激活T细胞,从而提高对免疫检查点抑制剂的反应率。对于以髓系细胞高浸润为特征的基底肿瘤,联合用药应针对抑制免疫环境。吲哚胺2,3-双加氧酶(Indoleamine 2,3-dioxygenase, IDO)和细胞内高浓度的腺苷在诱导抑制细胞毒性T细胞功能的途径中发挥着关键作用,因此靶向IDO1和腺苷A2a受体(A2aR)也是尿路上皮癌治疗的一个很有希望的靶点。
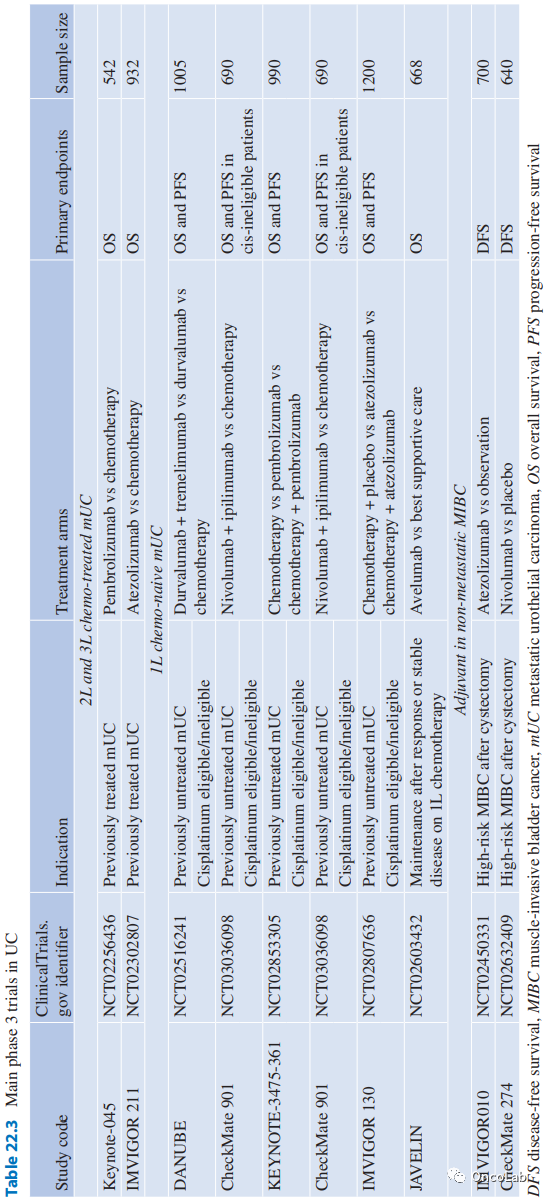
Table 22.3 UC的主要3期试验。DFS, 无病生存期;MIBC, 肌肉浸润性膀胱癌;mUC, 转移性尿路上皮癌;OS, 总生存期;PFS, 无进展生存期。
未来的研究工作应该集中在“明确可以预测患者对免疫抑制剂是否有反应的预测性生物标志物”上。在这方面,识别创新的相关生物标志物将有望帮助医生在患者个体层面上预测患者是否可以从特定的免疫治疗或联合免疫治疗中受益。这些生物标志物可以通过特定的肿瘤或宿主标记物(例如,血清、微生物群等)或两者共同决定,以综合考虑肿瘤和免疫系统高度复杂的相互作用,从而决定治疗方案,以诱导机体产生更有效的抗肿瘤反应。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
作者 | Pernelle Lavaud and Yohann Loriot
初稿翻译 | 陈晓意 郭子 罗佳佳
编辑排版 | 应正
审核修改 | 王坤 胡珊
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏