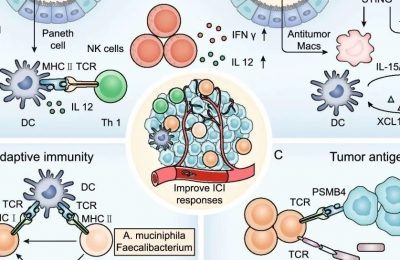
23.1 引言
随着免疫疗法加入主流癌症治疗手段的行列,人们便开始关注与反应性和耐药性有关的生物标记物。治疗前生物标记物可能有助于患者选择更加合理的治疗方法,甚至可能对筛选出非常规反应模式(如延迟反应或肿瘤在明显消退前 “进展”)的患者也有帮助。这些生物标记物也可能有助于预测某些严重的免疫相关的不良事件。此外,昂贵的治疗费用也是推动该领域深入研究的一个因素。
研究最充分的影响治疗反应的因素是通过免疫组化法测量的PD-L1蛋白表达。研究表明,在多种实体肿瘤类型中,抗PD -1和PD-L1单药治疗的客观应答率(ORR)都比较高,近期又发现联合抗PD -1/CTLA-4阻断剂可用于治疗非小细胞肺癌(NSCLC)患者。本章将综述PD-L1作为生物标志物在多种肿瘤中的应用,以及其在临床实践中实施的问题,例如不同的商业化PD-L1检测方法。同时也将介绍其他新兴的基于肿瘤组织的生物标志物,如肿瘤的突变负荷、CD8+肿瘤浸润淋巴细胞(TIL)密度、T细胞克隆研究、基因表达特征以及外周血生物标志物。
23.2 抗PD-1/PD-L1疗法及PD-L1表达作为生物标志物的作用
23.2.1 实体瘤的早期治疗经验
通过免疫组织化学(IHC)检测PD-L1的表达可能与抗PD-1的应答有关,这样的第一个联想来自2010年报道的抗PD-1的I期研究(MDX1106,nivolumab)。在这项研究中,来自于9名患者提供的可供研究的组织显示,细胞膜表面PD-L1的表达与能否产生反应之间存在一定的相关性。该发现随后在有治疗前肿瘤样本的扩展研究中得到进一步证实:42名患者患有多种肿瘤类型(包括黑色素瘤、非小细胞肺癌、肾细胞癌、前列腺癌和结直肠癌)。当评估肿瘤细胞PD-L1的表达时,PD-L1阴性的患者没有一例对该疗法产生反应(0/17),而免疫组化PD-L1阳性的肿瘤患者有36%(9/25)的患者有客观反应(p=0.006)。
2014年报道的另一项里程碑式的临床试验评估了抗PD-L1抗体(Atezolizumab)在不同实体恶性肿瘤(非小细胞肺癌、黑色素瘤、肾癌、头颈部、乳腺、结直肠等)中的活性,并将PD-L1作为潜在的反应生物标志物进行了研究。然而,他们强调PD-L1在免疫细胞上表达,而不在肿瘤细胞。他们指出免疫细胞上PD-L1的表达与患者的ORR显著相关(PD-L1(+)和PD-L1(−)肿瘤分别为45%和16%)。随后,大多数关于PD-1/PD-L1阻断剂的临床试验都评估了治疗前肿瘤标本中肿瘤和/或浸润免疫细胞的PD-L1蛋白表达以及与临床结果的关系。下面总结了其中一些主要的临床试验,图23.1中显示了按PD-L1状态分类的综合反应率。
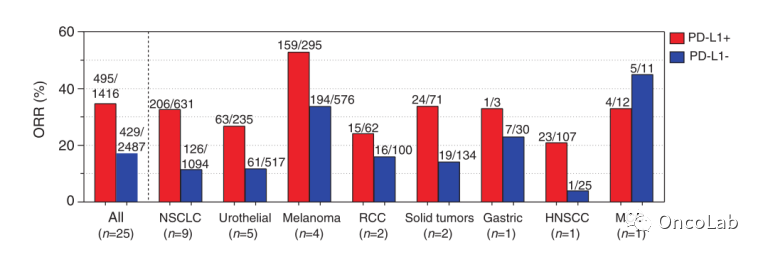
Fig. 23.1 免疫组织化学检测肿瘤标本中PD-L1的表达与多种实体肿瘤类型对抗PD-1/L1的客观反应率(ORR)相关。
23.2.2 非小细胞肺癌(NSCLC)
就PD-1/PD-L1阻滞剂的活性研究而言,非小细胞肺癌可能是研究最充分的肿瘤类型。9项临床实验显示,有1725例非小细胞肺癌患者接受了三种不同的抗PD-1或抗PD- L1疗法[nivolumab, pembrolizumab(人IgG4抗pd -1单克隆抗体)和atezolizumab]中的一种治疗,他们的总体ORR为17%。 从所有患者收集的数据——无论他们是否在一线或更高级别的环境中接受药物,或用于确定 PD-L1 阳性的检测方法——显示 PD-L1(+) 的肿瘤患者的 ORR 为 33%, PD-L1(−) 肿瘤患者的ORR为11%。当每种治疗方法被单独评估时,这种关系保持不变:nivolumab单抗(5项研究,538名治疗患者)的ORR为30%PD-L1(+)与13%PD-L1(−);pembrolizumab单抗(2项研究,1015名治疗患者)的ORR为33%PD-L1(+)与11%PD-L1(−);atezolizumab单抗(2项研究,190名治疗患者)的ORR为 42%PD-L1(+)与11%PD-L1(−)。
近期的一项研究比较了抗PD-1单一疗法和联合抗PD-1/CTLA-4阻断作为NSCLC患者一线治疗的效果,发现了两个与PD-L1作为生物标志物有关的有趣现象。第一个发现是,治疗前肿瘤微环境中PD-L1水平的增加提高了抗PD-1的ORR。值得注意的是,该结果与根据PD-L1状态进行二分法的结论相反。第二个值得注意的发现是,治疗前肿瘤标本中PD-L1表达水平的增加不仅预示着对抗PD-1反应的改善,而且还与接受联合治疗方案的患者ORR的增加有关。
此外,相关人员还研究了非小细胞肺癌患者的组织学亚型、潜在的基因改变、吸烟状态、PD-L1状态和治疗效果的关系。亚型组分析表明,肿瘤组织学可能影响PD-L1的表达和治疗反应之间的关系,在非鳞状NSCLC中,PD-L1的富集与反应相关,但在表现为鳞状组织学的肿瘤中则无反应。这可能是由于PD-L1在肺腺癌中的表达与IFN-γ有关,而IFN-γ与PD-L1在肺鳞癌中的表达则不相关(见下文“肿瘤微环境中PD-L1表达的意义是什么?”)。
EGFR、TP53和KRAS基因的突变都与PD-L1表达增加有关,通常是通过PI3K-AKT-mTOR通路的激活。其中,TP53和KRAS突变与较高的ORR相关,而EGFR突变被认为与抗PD-1检查点阻断的耐药性部分相关。最后,几项研究报告了有吸烟史的患者的ORR更高或PFS更长。
23.2.3 泌尿生殖系统恶性肿瘤(尿路上皮癌和肾癌)
尿路上皮癌(膀胱癌、输尿管癌和肾盂癌)是另一种对PD-1/PD-L1阻断高度敏感的肿瘤类型。针对尿路上皮癌的大多数临床试验都评估了抗PD-L1而不是抗PD-1的活性。在包含752名尿路上皮癌患者的5个不同的相关临床试验中观察到,他们总的ORR为16%。
根据PD-L1在TME中的表达进行分级时,肿瘤或者免疫细胞PD-L1(+)患者的ORR为27%,而PD-L1(−)患者的ORR为11%。当按治疗药物细分时,PD-L1表达与反应的关联并不取决于所接受的抗PD-L1药物。例如,在阿特珠单抗试验(3项研究和 695 名接受治疗的患者)中观察到 PD-L1(+) 患者的 ORR 为 27%,而 PD-L1(-) 患者的 ORR 为 11%,并且在一项针对 42 名患者的临床试验中发现 PD-L1(+) 患者的 ORR 为 45%,而 PD-L1(-) 患者的 ORR 为 0%。
值得注意的是,唯一一项关注抗PD-1药物(纳武单抗,67名患者)疗效的研究发现,PD-L1(+)和PD-L1(-)肿瘤患者的ORR相似(分别为24%和26%)。虽然没有观察到ORR的差异,但与PD-L1(−)肿瘤相比,PD-L1(+)肿瘤患者的中位总生存期有所改善。该研究仅关注肿瘤细胞PD-L1的表达量,并将表达量超过1%这个阈值的肿瘤定性为PD-L1(+),这比使用抗PD-L1药物研究时划定的阈值要低。未来的研究无疑将集中在研究免疫细胞上PD-L1的表达成分是否能更好地对纳武单抗的反应进行分级。
两项专注于转移性肾细胞癌(RCC)治疗的临床试验报告了有关PD-L1状态及其与疗效的关系的信息。一项研究使用纳武单抗(n=107),另一项研究使用阿特珠单抗(n=55),两项研究的总ORR为19%。在这两项研究中,TME中的PD-L1表达没有明显的益处。另一项有10名患者参加的小型研究比较了阿特珠单抗与贝伐单抗(人源化单克隆抗VEGF)在PD-L1(+)和PD-L1(-)肿瘤之间的活性,也没有发现差异。就像肺鳞状细胞癌(上文讨论过)一样,这种缺乏反应可能是由于肾癌中PD-L1的表达与干扰素-γ的表达无关,这与许多其他实体肿瘤类型相反。
23.2.4 黑色素瘤
在所研究的实体肿瘤类型中,晚期黑色素瘤对PD-1/PD-L1阻断的应答率最高。包括871名被标注了肿瘤PD-L1表达的黑色素瘤患者的四项临床试验表明,总体ORR为40%。其中PD-L1(+)(以肿瘤细胞中有超过5%的PD-L1表达为分界线)肿瘤患者的ORR为53%,而PD-L1(−)肿瘤患者的ORR值为34%。随着一些试验的成熟,科研人员已经可以评估其他终点,如无进展生存(PFS)和总体生存(OS),而不仅仅是ORR。目前发现,PD-L1(+)黑色素瘤患者的PFS和OS比PD-L1(−)患者更长。
此外,PD-L1表达水平较高的黑色素瘤患者比表达水平较低的黑色素瘤患者更有可能产生药效,这使人们对连续变量的二分评分系统的使用提出了质疑。目前尚未确定BRAFV600E突变与PD-L1表达或患者对PD-1/PD-L1阻断的反应之间的关联。这也具有重要的生物标志物意义,因为它表明在为晚期黑色素瘤患者做出治疗方法的决定时,BRAFV600E突变和PD-L1表达应被视为单独的生物标志物。
目前也将PD-L1的表达评估为黑色素瘤患者对双重抗PD-1/CTLA-4检查点阻断反应的潜在生物标志物。与接受抗PD-1单药治疗的患者相比,PD-L1的表达并不影响抗PD-1/CTLA-4检查点联合阻断方案观察到的显著高应答率,这表明联合阻断疗法可能能够“克服PD-L1(−)状态”。有人提出 PD-L1的表达在未来用于对不同方案之间的患者进行分类,PD-L1(+)患者接受抗PD-1单一治疗,这只会产生较低的副作用,而PD-L1(−)患者更适合接受联合抗PD-1/CTLA-4检查点阻断疗法。
23.2.5 病毒相关癌症
头颈部鳞状细胞癌(HNSCC)、胃癌和默克尔细胞癌(MCC)是公认的与病毒感染相关的疾病,分别是由人乳头瘤病毒、EB病毒和默克尔细胞多瘤病毒引起的。在这些肿瘤中,病毒阳性的肿瘤的PD-L1表达量比病毒阴性的肿瘤更高。如今认为病毒抗原的存在有助于抗肿瘤免疫反应,因此免疫检查点阻滞剂可能对这些肿瘤的治疗有一定的效果。初步研究表明,与上述其他实体肿瘤类型一样,如果HSNCC患者的肿瘤是PD-L1阳性,则抗PD-1/PD-L1阻断治疗有效的可能性更大: PD–L1阳性与阴性ORR分别为21%对4%。
在一项使用派姆单抗治疗胃癌患者的小型研究中,观察到的ORR为22%。PD-L1表达量需要以1%为阈值进行登记阳性和阴性; 因此,本研究中无法比较PD-L1(+)与(-)之间潜在的差异反应,本研究也没有评估EB病毒状态。
在一项研究中,MCC患者对抗PD-1抗体的治疗反应与病毒的存在或PD-L1的表达并不显著相关。这可能是因为病毒阴性的MCCs具有非常高的突变密度,这一特征也被认为是抗PD-1的反应的生物标志物(见下面的突变负荷部分)。病毒状态和对免疫检查点阻断的反应之间的关系是一个正在积极进行研究的领域。
23.3 PD-L1免疫组化检测
最初关于PD-L1表达与抗PD-1反应相关的报道是通过实验室衍生的IHC试验进行的。很快在两个不同的免疫染色平台上开发了四种不同的专利、商业PD-L1检测方法,并进行了各自公司的抗PD-1/PD-L1试剂的临床试验,见Table. 23.1。许多分析使用不同的评分系统和不同的阈值来区分PD-L1(+)与PD-L1(−)的病例。除了让病理学家和肿瘤学家感到困惑外,这种情况对外科病理实验室来说也是不切实际的,因为他们不太可能有充足的资源在两个不同的免疫染色平台上支持四种不同的PD-L1检测。大多数实验室只有一台免疫染色仪,而且它不一定是市场上的检测方法所要求的Dako Link 48或Ventana BenchMark平台。
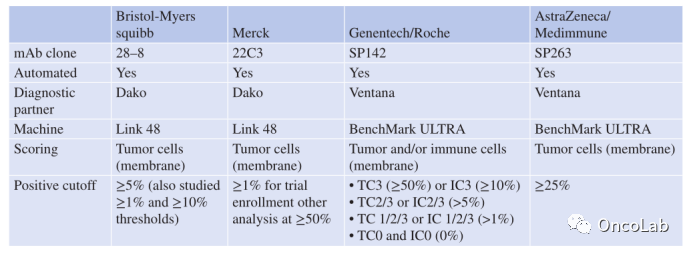
Table. 23.1 四种不同的市售PD-L1免疫组织化学检测方法
FDA认识到这种“一种检测/一种药物”模式的潜在危险,并支持比较了四种不同的市售PD-L1检测方法的性能。有四家掌握抗PD-1/PD-L1疗法的公司和两家生产PD-L1 免疫组化检测分析的公司参与了这项工作。在这项被称为“蓝图工作”的最终研究中,科学家收集了40例NSCLC患者的外科病理病例,并用每种检测方法对连续的FFPE肿瘤切片进行了染色。然后,三位不同的病理学家对肿瘤细胞和免疫细胞PD-L1的表达进行PD-L1评分,取其结果的平均值。重要的是,它没有使用公司建议的评分系统进行评估,而是简单地以肿瘤细胞或免疫细胞染色的百分比进行评估。他们发现其中三种检测方法的表现非常相似(22C3、28-8和SP263检测方法),而SP142检测方法明显比其他三种检测方法标记出了更少的肿瘤细胞的PD-L1表达。
还有两项值得注意的研究集中在检测方法的比较上。其中一项由百时美施贵宝(Bristol-Myers Squibb)支持的国家综合癌症网络(National Comprehensive Cancer Network)领导,有13名学术病理学家参与。这项工作比较了22C3检测、28-8检测、使用SP142抗体克隆的实验室衍生检测(LDT),旨在模仿SP142商业检测,以及使用E1L3N克隆的LDT,对90例NSCLC的手术病理档案进行了比较。在这项规模较大且有统计学依据的研究中,SP142检测方法不仅标记的肿瘤细胞染色的PD-L1表达较少,而且免疫细胞表达也较少。有趣的是,在这项比较中,当13位病理学家对每个病例进行平均打分时,22C3检测方法标记的肿瘤细胞比28-8和E1L3N检测方法略少。然而,个别病理学家之间的打分差异大于22C3检测方法与28-8检测方法和E1L3N LDT之间观察到的PD-L1标记的差异;因此,在常规外科病理实践中,这种检测性能的差异永远不会被发现。
第三项工作研究了数量最多的病例—近500例存档的非小细胞肺癌病例—由一名病理学家根据PD-L1表达进行评分。另一位病理学家也对一部分病例进行了评分。在肿瘤细胞染色的多个切点上,他们显示SP263法、28-8法和22C3法的一致性>90%。在进行这项研究时,SP142检测还没有商业化,因此没有与其他三种检测方法一起进行一致性评估。
关于商业上可获得的PD-L1检测的术语可能会令人困惑,因为检测本身包括克隆名称。例如,“SP142抗体克隆”不同于“SP142检测”,SP142检测包括许多试剂的集合体,也包含SP142抗体克隆,这些试剂以特定的顺序并在精确的技术条件下使用,以形成一个检测系统。因此,PD-L1免疫组化检测中观察到的性能差异可能是由一抗浓度、抗体亲和力、抗体靶向的表位、抗原检索试剂、特异性试剂的pH值或扩增步骤等因素造成的。商业化化验的化验系统是专有的;所以关于扩展的组件列表的细节很少。已经进行了两项不同的研究,保持其他检测条件基本不变,专注于探究抗PD-L1抗体克隆的一致性。对于非小细胞肺癌标本和黑色素瘤标本,当所有其他检测条件保持不变时,SP142抗体的表现与28-8、22C3和SP263克隆的抗体一样好。当观察到抗体克隆之间的差异时,对切片的审查表明,这些差异是由于PD-L1表达的局域性和异质性,在不同的肿瘤切片上有所不同,而不是在肿瘤细胞或免疫细胞标记的检测灵敏度上有明显的差异。标记PD-L1分子的胞内区或胞外区的抗体对一致性没有显著影响,Fig. 23.2。因此,这些研究表明,与其他商业检测方法相比,SP142抗体克隆本身以外的检测系统的某些其他组件导致了观察到的SP142检测性能的差异。
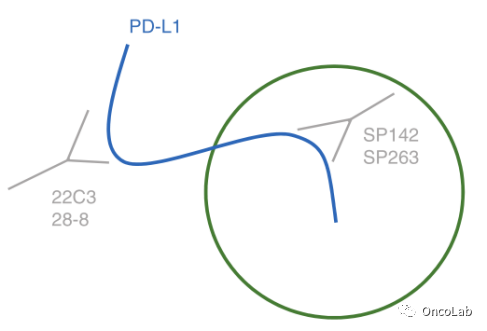
Fig. 23.2 商用PD-L1抗体含有不同的一抗,其中一些针对PD-L1分子的胞外区(22C3和28-8),而另一些针对胞内区(SP142和SP263)
综上所述,这些共同发现表明,在未来,外科病理实验室可能只能提供三种具有类似性能的商业PD-L1测定方法(28-8、22C3或SP263测定)中的一种,或提供具有同等性能特征的LDT(包括使用SP142克隆的方法),或者其他的特异性的,商业化设计并经过临床测试的PD-L1表达评分系统并与适当的抗PD -1/PD-L1治疗药物匹配。由于PD-L1表达的局灶性,以及密切相关的时间和空间异质性问题,需要进行额外的研究来确定理想的组织类型(标本大小和病变数量等),以优化PD-L1在治疗前肿瘤微环境中表达的预测价值。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
作者 | Nicolas A. Giraldo and Janis M. Taube
初稿翻译 | 罗佳佳 章震
编辑排版 | 杜轻松
审核修改 | 王坤 胡珊
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏