杂志名称:Sci Transl Med. 发表日期:2023.11.01 DOI:10.1126/scitra…
杂志名称:Sci Transl Med.
发表日期:2023.11.01
DOI:10.1126/scitranslmed.adg3049.
PubMed:https://pubmed.ncbi.nlm.nih.gov/37910602/
影响因子:17.1
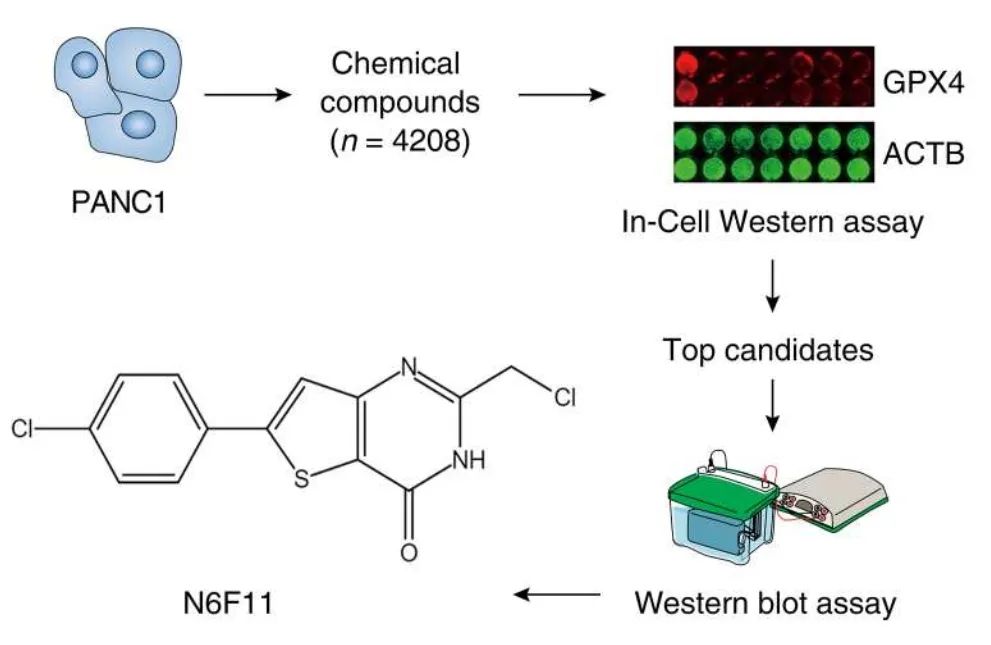
脂质过氧化依赖性的铁死亡已成为肿瘤治疗的新策略。然而,当前的策略不仅在恶性细胞中选择性诱导铁死亡,同时也在免疫细胞中引发铁死亡,这可能削弱抗肿瘤免疫。在此,我们利用In-Cell Western分析结合无偏药物筛选,发现化合物N6F11可作为铁死亡诱导剂,特异性地在癌细胞中诱导谷胱甘肽过氧化酶4(GPX4,一种关键的铁死亡抑制因子)的降解。N6F11并未在包括树突状细胞、T细胞、自然杀伤细胞和中性粒细胞在内的免疫细胞中引起GPX4的降解。在机制上,N6F11结合到癌细胞中E3泛素连接酶三联体基序含量25(TRIM25)的RING结构域,触发TRIM25介导的GPX4的K48连结泛素化,从而导致其蛋白酶体降解。在功能上,N6F11处理引起铁死亡的癌细胞死亡,引发了由CD8+ T细胞介导的HMGB1依赖性抗肿瘤免疫。在包括由KRAS和TP53突变驱动的胰腺癌的基因工程小鼠模型在内的晚期癌症模型中,N6F11还增强了针对CD274/PD-L1的免疫检查点阻断的敏感性。这些发现可能为提高铁死亡驱动的抗肿瘤免疫策略提供一种安全和有效的方法。
这篇文章的主题是探索如何通过降解肿瘤细胞中的谷胱甘肽过氧化物酶4 (GPX4) 来增强铁死亡启动的抗肿瘤免疫反应,这是治疗胰腺癌的新策略。研究者发现化合物N6F11可以在癌细胞中特异性地诱导GPX4的降解,从而引发铁死亡。值得注意的是,N6F11并未在免疫细胞中引起GPX4的降解,这可能避免了削弱抗肿瘤免疫力的问题。
该研究的创新性在于,通过N6F11的介入,研究者找到了一种在肿瘤细胞中特异性诱导铁死亡的方式,而无需影响免疫细胞。这种策略能够避免削弱抗肿瘤免疫力的问题,从而提高铁死亡引发的抗肿瘤免疫反应。
该研究的意义在于它提供了一种可能的新策略,通过调控肿瘤细胞中的GPX4,以增强铁死亡启动的抗肿瘤免疫反应。这可能为胰腺癌和其他类型的癌症治疗提供新的治疗途径。
此外,N6F11还增强了免疫检查点阻断对CD274/PD-L1靶向的敏感性,这在晚期癌症模型中具有重要意义,如由KRAS和TP53突变驱动的胰腺癌的基因工程小鼠模型。这意味着N6F11的使用可能有助于提高免疫检查点阻断疗法的效果。
总的来说,这篇文章提出了一个新的策略来增强铁死亡启动的抗肿瘤免疫反应,这对于癌症治疗来说是一个重要的进步。然而,此项研究尚在早期阶段,需要进一步的研究和临床试验来验证其安全性和有效性。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab