OncoLab实验室 文献阅读 Lancet:阿特珠单抗联合贝伐珠单抗和化疗治疗转移性、持续性或复发性宫颈癌(BEATcc):一项随机、开放标签的三期临床试验
杂志名称:Lancet 发表日期:2023.12.01 DOI:10.1016/S0140-6736(23)0…
杂志名称:Lancet
发表日期:2023.12.01
DOI:10.1016/S0140-6736(23)02405-4.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38048793/
影响因子:168.9
GOG240试验确定了贝伐珠单抗联合化疗作为转移性或复发宫颈癌的标准一线治疗方案。在BEATcc试验(ENGOT-Cx10-GEICO 68-C-JGOG1084-GOG-3030)中,研究者旨在评估在这一标准治疗方案中添加一种免疫检查点抑制剂的效果。
在这项研究者发起的随机、开放标签、第三阶段试验中,来自欧洲、日本和美国92个地点的患者,他们患有可测量、之前未经治疗且无法通过手术或放疗治愈的转移性(IVB期)、持续性或复发性宫颈癌,被随机分配1:1接受标准治疗(每3周周期的第1天使用顺铂50 mg/m2或卡铂曲线下面积为5,紫杉醇175 mg/m2,以及贝伐珠单抗15 mg/kg)加上或不加上阿特珠单抗1200 mg。治疗将继续进行,直到疾病进展、不可接受的毒性、患者退出或死亡。分层因素包括之前是否接受过同时化疗放疗(是与否)、组织学类型(鳞状细胞癌与腺癌包括腺鳞癌)和铂药物基础(顺铂与卡铂)。双主要终点是根据实体瘤反应评价标准1.1版的研究者评估的无进展生存期和在意向治疗人群中分析的总生存期。这项研究已在ClinicalTrials.gov注册,NCT03556839,并且正在进行中。
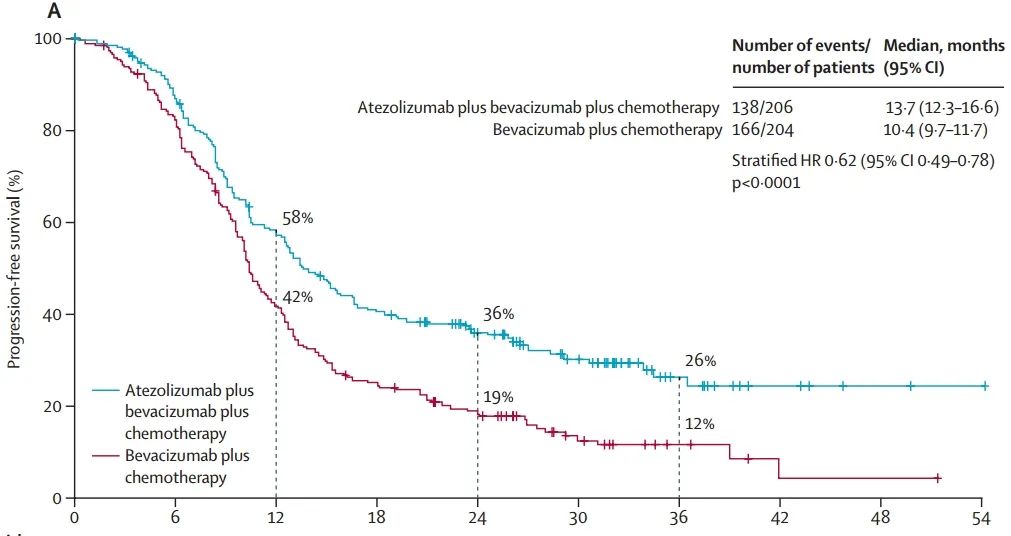
在2018年10月8日至2021年8月20日期间,评估资格的519名患者中有410名被招募。使用阿特珠单抗的中位无进展生存期为13.7个月(95%置信区间12.3-16.6),而标准治疗组为10.4个月(9.7-11.7)(风险比[HR]=0.62 [95%置信区间0.49-0.78];p<0.0001);在中期总生存期分析中,中位总生存期分别为32.1个月(25.3-36.8)对22.8个月(20.3-28.0),(HR 0.68 [95%置信区间0.52-0.88];p=0.0046)。3级或更严重的不良事件在实验组的患者中发生率为79%,在标准组的患者中为75%。1-2级的腹泻、关节痛、发热和皮疹在使用阿特珠单抗的患者中有所增加。
在转移性、持续性或复发性宫颈癌的标准贝伐珠单抗加铂药物方案中添加阿特珠单抗,显著改善了无进展生存期和总生存期,应该作为新的一线治疗方案考虑。
本研究探讨了在标准的贝伐珠单抗加铂类药物治疗方案中加入免疫检查点抑制剂阿特珠单抗,用于治疗转移性、持续性或复发性宫颈癌的疗效。随机、开放标签、第三阶段的BEATcc试验结果显示,阿特珠单抗不仅延长了无进展生存期,也显著提高了总生存期,即便伴随着一些轻至中度的副作用。
该研究的创新性在于将免疫疗法引入宫颈癌的一线治疗,这在以往的治疗方案中并不常见。阿特珠单抗作为一种免疫检查点抑制剂,通过激活患者自身的免疫系统来攻击癌细胞,这一机制与传统的化疗和靶向疗法有所不同。研究结果表明,该疗法在提高宫颈癌患者的生存率方面具有重要意义,并可能改变未来宫颈癌治疗的标准疗法。
从研究意义上来说,这项研究不仅为宫颈癌患者提供了一种新的治疗选择,同时也为免疫疗法在其他种类的癌症治疗中的联合应用开辟了道路。随着这类研究的深入,我们对于免疫系统在癌症治疗中的作用有了更深的理解,未来有望开发出更多的治疗方案,以提高癌症患者的生存质量和生存率。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab