27.1 引言
近年来,科学界越来越认识到肠道微生物群对宿主健康和病理生理的重要影响。肠道菌群执行多种基础功能,包括降解营养物质以提供能量、清除外来生物、培养免疫系统、支持肠上皮细胞的生长与分化、促进肠蠕动、产生抗菌肽以根除病原体并维持定植抵抗力。肠道是免疫系统中最大的部分,它不仅暴露于我们必须耐受的食物和共生抗原,还是许多病原体的潜在入口。沿着胃肠道向下,细菌数量逐渐增多,在结肠可达每毫升1012个。好氧菌主要存在于小肠上部,而厌氧菌则在结肠中占主导。厚壁菌门、拟杆菌门、变形菌门和放线菌门是最常见的菌群,古菌也是其成员之一。
肠道菌群在调节先天和获得性免疫反应中扮演关键角色,对炎症和耐受性之间的平衡产生影响。随着测序技术的进步,对人类微生物群的深入了解已经可能,显著提升了我们对微生物在健康和疾病中作用的认识。例如,通过人类微生物组项目及MetaHIT和HMP研究,我们知道健康个体的微生物群在肠道、口腔、皮肤或阴道等不同栖息地表现出高度的细菌多样性,并且在物种水平上存在显著的个体差异。尽管不同部位的物种多样性不同,特定组织位点上的功能和细菌基因图谱显示出一定的稳定性。例如,厌氧的厚壁菌门和拟杆菌门在肠道中占据主导地位,而放线菌门和变形菌门在皮肤中极为丰富。确定“正常微生物群”的任务充满挑战,因为同一种微生物可能根据饮食、营养环境、宿主的遗传背景和潜在的合并感染的不同,表现为共生或病原体。尽管如此,被认为共生的细菌有助于维持免疫内稳态,而病原体则与自身免疫反应相关。有趣的是,在健康人的血清中,我们可以发现对非致病性细菌的共生菌特异性抗体和循环T细胞的反应。
肠道微生物群在出生时的定植对触发粘膜免疫系统的成熟至关重要。在这一发育阶段,肠道菌群对先天和获得性免疫反应的建立、炎症、感染和耐受性之间的平衡发挥着关键作用。无菌小鼠显示出Peyer斑块的发育不良,肠道中缺乏孤立的淋巴滤泡,血清中IgM自然抗体水平低,这种表型可以通过肠道菌群的定植得以逆转。特别地,节段丝状细菌(SFB)在远端小肠的定植对于新生肠道中树突状细胞分泌IL-6和IL-22及伴随的Th17和调节性T细胞(Treg)的分化至关重要。对于脆弱拟杆菌和TLR2以及梭状芽胞杆菌诱导的Treg细胞之间联系的发现引起了极大的兴趣。然而,结肠中Treg细胞的内稳态更多依赖于不同菌株的协同作用及由跨界生态系统创造的平衡微环境,这有助于维持和产生消炎环境。
27.2 评估癌症携带者的肠道失调
尽管我们对肠道微生物的遗传和功能多样性有了一定了解,但目前的认识仍然不够完整。传统的qPCR和FISH分析方法在全面性、专一性和灵敏度方面有所不足。近期,通过靶向16S rRNA基因的焦磷酸测序和宏基因组的霰弹枪测序,我们的知识得到了显著扩展,尽管这些方法成本高昂且需要大量数据分析。通过综合MetaHIT、人类微生物组项目(HMP)以及一项大型中国糖尿病研究的数据,建立了一个涵盖超过500个肠道相关细菌和古菌基因组的人类肠道微生物组参考基因目录,包含约9,879,896个基因的非冗余参考目录,已经公布于(http://meta.genomics.cn)并存储在GigaScience数据库。这表明我们可能已经达到了对核心基因内容和功能的全面覆盖。
值得注意的是,超过一半的受试者的基因数量保持在30万以下,突出显示了个体特异性基因在细胞壁/膜/包膜生物生成及DNA复制、重组和修复过程中的富集,而普通基因则在信号转导机制、能量生产、碳水化合物运输与代谢、氨基酸运输与代谢中占主导地位。
近年来,几个研究小组对健康人和癌症患者的肠道菌群进行了调查,以探索微生物与癌症之间的关系。例如,Goedert 等人使用16S rRNA测序分析了绝经后妇女的肠道菌群,并观察到乳腺癌患者的α多样性(种群数量)较低,而β多样性(种群组成差异)与健康个体存在显著变化。
Dejea 等人利用FISH和16S rRNA测序分析了患有或未患结直肠癌(CRC)的受试者的结直肠黏膜,发现了细菌生物膜的存在,尽管没有发现一致的细菌属与结直肠癌相关。其他利用16S rRNA或宏基因组测序的研究揭示了CRC患者与对照组肠道菌群组成的显著差异,特别是梭杆菌和卟啉单胞菌在CRC受试者中的患病率和水平显著高于对照组。这些差异可能受到研究人群的饮食、药物使用以及实验方法和病例对照匹配等因素的影响。
此外,在当前的宏基因组学研究中,无法检测到低于10^5个细菌/克的浓度。只有大约15%的已鉴定种类同时被培养组和宏基因组检测到,突出了培养依赖方法与培养独立方法的互补性。通过培养条件的多样化和基质辅助激光解吸电离飞行时间质谱(MALDI-TOF MS)的应用,分类基因组学取得了重大进展。这些努力将有助于未来在不同类型的癌症队列中定义“癌症相关的肠道指纹”,进一步建立癌症对肠道失调影响的地理分布。
27.3 微生物组与癌症发病率
寄居在肠道及身体其他部位的共生微生物群体,似乎在肠道和肠外癌症的发展中发挥了重要但尚未完全理解的作用。在无菌条件下或经免疫抑制、抗生素处理的啮齿类动物中进行的开创性研究显示,这些微生物在肿瘤形成过程中有不容忽视的影响,不论炎症是否存在。在结肠癌或肝癌的发展中,微生物可通过产生有毒代谢物、致癌物或诱导炎症环境(最终导致基因组不稳定、DNA损伤响应或免疫逃逸)直接促进癌变。共生微生物还可能通过形成协同的生物膜,促进交叉营养或代谢作用,重新定义癌症微环境。
最近的研究发现,肠道外(如乳腺和卵巢)肿瘤的发展与由肠道微生物引发的、TLR5介导的全身性炎症有关,这种炎症通常由IL-6或IL-17驱动。相对地,也有研究表明细菌在对抗癌症方面可能发挥有益作用。例如,延长使用甲硝唑和环丙沙星的抗生素治疗在HER2/neu基因驱动的转基因小鼠中使乳腺癌(BC)的发病率增加了三倍。在人类中,流行病学研究表明抗生素使用与乳腺癌风险之间存在剂量依赖关系。Knekt等人首次报道了抗生素摄入与乳腺癌发病率之间的关联,研究显示,小于50岁的女性报告以前和/或目前使用抗生素治疗尿道感染(但没有细菌尿)的情况下,乳腺癌风险增加。
此外,多项研究报告了人体不同入口处的局部微生物组成改变与癌症发生之间的联系,如头颈癌中的口腔癌,非小细胞肺癌中的支气管癌,以及肠道和结肠恶性肿瘤与宫颈癌中的阴道癌。
然而,这些研究往往存在缺陷或偏见:(a) 缺乏严格的方法学,如PCR、16S 焦磷酸测序分析、深度测序(宏基因组学)、文化组学;(b) 忽视了可能独立增加癌症风险的生活方式因素,如社会环境、久坐不动的生活方式、营养不良、酗酒或吸烟行为;(c) 缺乏验证队列(根据REMARK标准);(d) 微生物优势与潜在的病理生理之间缺乏明确的因果关系。当前对肠道菌群对癌症影响的研究将激励临床医生开展前瞻性研究,评估抗生素使用、营养、遗传和环境因素在驱动或影响肿瘤发生过程中的作用。
27.4 放射治疗与微生物群
放射治疗对微生物群及其在癌症免疫治疗中的影响尚未被广泛研究。目前大部分研究集中在辐射引起的肠道损伤及其由宿主微生物组调控的影响上。
Crawford 等人首次报告指出,肠道微生物群是辐射诱导的肠道损伤的一个关键调节因子,研究显示无菌动物对辐射性肠炎表现出更强的抵抗力。辐射显著改变了小鼠体内的微生物组成。实验证明,全身照射后,通过粪便微生物移植(FMT)调节肠道微生物群可以提高生存率,并通过刺激血管生成部分恢复肠上皮的完整性。TLR信号通路可能在辐射对肠道的保护中发挥重要作用。
Ciorba 等人在辐射诱导的肠损伤的临床前模型中发现,乳酸菌通过TLR2以及表达COX-2的间充质干细胞的迁移发挥保护作用。此外,一些临床研究也报道了辐射诱导肠损伤后肠道菌群的变化。Wang 等人发现,盆腔照射诱发患者肠道炎症标志物的释放,与乏力相关。较低的肠道微生物多样性同样预示着辐射诱导的结肠炎的发展。Demers 等人的研究表明,双歧杆菌/乳酸杆菌显著降低腹泻的发生。然而,没有单一的细菌菌株被一致认为对辐射引起的肠损伤有益。
微生物群在放射治疗效果中的积极作用仍需进一步验证。有理由相信,破坏粘膜屏障和促进黏膜微生物的易位可能激活先天免疫系统。Paulos 等人首次报告了这一发现,他们表明全身照射促进了依赖于LPS-TLR4的抗原提呈细胞的激活,从而增强了过继T细胞转移的疗效。
辐射诱导的肠损伤促进共生细菌的易位和LPS的释放,这导致树突状细胞的激活和过继转移T细胞的活化。这一过程与治疗效果及在小鼠中长期治愈黑色素瘤B16F10相关。因此,调节肠道微生物群与免疫系统之间的平衡可能增强细胞肿瘤免疫治疗的效果。然而,Espinosa-Carrasco 的后续研究表明,LPS的易位只能部分解释Paulos 等人观察到的效果。至今,尚无数据支持微生物组成分在放射免疫治疗中作为调节剂的作用。
27.5 环磷酰胺与肠道微生物群的相互作用
众所周知,化疗会诱发粘膜炎和中性粒细胞减少症,这两种主要的副作用可能会导致使用抗生素并导致生物失调。研究人员探讨了肠道菌群对化疗药物,特别是能够影响肠道内稳态的药物疗效的影响问题。环磷酰胺(CTX)是一种dna烷基化剂,属于氮家族,具有免疫调节和抗血管生成的特性,目前用于治疗乳腺癌、肉瘤和儿童恶性肿瘤的临床,其疗效取决于其诱导小肠内的选择性革兰氏阳性细菌易位的能力,如hirrae肠球菌或johnsonii乳杆菌进入次级淋巴器官。事实上,CTX负责破坏肠道屏障的完整性和肠道内稳态(包括上皮和免疫隔室)。
CTX治疗的患者肠道屏障较弱,这打破了对肠道菌群的耐受性,导致其对某些菌株免疫。这种免疫是由CD4+效应淋巴细胞“致病Th17”产生IFNγ和IL-17,帮助肿瘤浸润Th1淋巴细胞控制小鼠肿瘤生长。有趣的是,广谱抗生素以及万古霉素(主要杀死革兰氏阳性菌)和粘菌素(主要消除革兰氏阴性菌)都损害了pTh17在脾脏中的极性,以及CTX在P815乳腺细胞瘤和MCA205肉瘤小鼠体内的全面抗癌活性,支持了环磷酰胺的功效与菌群有关的的观点。进一步的研究表明,在易位革兰氏阳性细菌中,hirae诱导Th17和Th1 CD4+ T淋巴细胞,并刺激肿瘤特异性CD8+ T细胞,因为它减少了免疫抑制瘤内treg和产生il -17的γδ T细胞(Fig 27.1)。抗生素处理的小鼠与hirai大肠杆菌的单一联合作用大大提高了CTX对肿瘤生长的抑制作用,这种作用被消耗CD8+ T细胞或中和IFNγ的抗体所阻断,这表明它需要抗癌免疫应答。
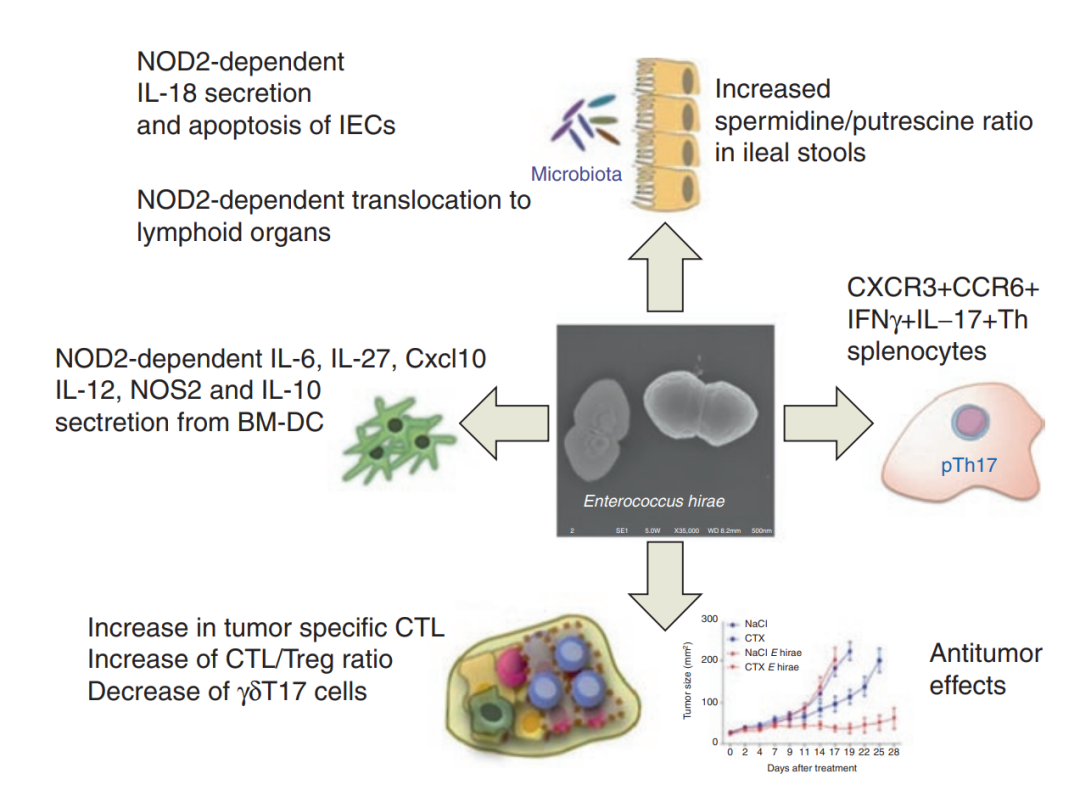
Fig 27.1 E. hirae的免疫原性。在大约25%的个体中,E. hirae寄居在空肠和结肠中。在古斯塔夫·鲁西维勒让夫的鼠肠道中,这种肠球菌非常占优势。这种肠球菌不具病原性,并且得益于环磷酰胺介导的肠道通透性增加,能够转移到次级淋巴器官,激活特定的致病性CXCR3+ CCR3+ T细胞,这些T细胞迁移到肿瘤病变处,并重新编程肿瘤微环境,即减少调节性T细胞和γδT17细胞,增强针对癌症的CTL反应。E. hirae还作用于肠上皮细胞,以NOD2依赖的方式调节凋亡和IL-18分泌。骨髓树突状细胞识别E. hirae,以NOD2依赖的方式诱导IL-12和IL-27的产生。所有这些特性共同参与其佐剂效应,增强环磷酰胺介导的免疫激活能力和抗癌效果。
27.6 铂盐与肠道菌群
Giorgio Trinchieri 博士的研究小组指出了肠道菌群对抗癌药物功效的重要影响。Iida 等人的研究表明,在基于铂类的抗癌治疗中,肿瘤浸润的骨髓细胞产生的活性氧(ROS)介导的抗肿瘤作用与细菌存在关联。研究发现,铂盐(包括奥沙利铂和顺铂)的疗效依赖于肿瘤内髓系细胞(包括髓系抑制细胞、单核细胞和未成熟树突状细胞)通过依赖MyD88的机制产生活性氧。活性氧引发DNA损伤,进而导致肿瘤细胞DNA加合物的形成和细胞凋亡,这是奥沙利铂在MC38或EL4荷瘤小鼠模型中部分杀伤活性的机制。
有趣的是,研究发现与无特定病原体(SPF)动物相比,无菌或接受抗结核治疗的小鼠中化疗效果不明显。进一步的研究探讨了抗结核治疗对奥沙利铂介导的ROS产生的影响,发现编码活性氧生成酶NOX2的Cybb基因表达在接受抗结核治疗的小鼠中被抑制。
此外,当使用嗜酸乳杆菌对这些小鼠进行微生物补偿后,恢复了基于顺铂的化疗效果,并重建了与顺铂功能相关的炎症基因表达。总体来说,这些结果支持了一个观点:肠道菌群通过影响肿瘤微环境中的氧化还原平衡,进而影响当前临床上使用的铂盐治疗的效果。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 罗荷
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏