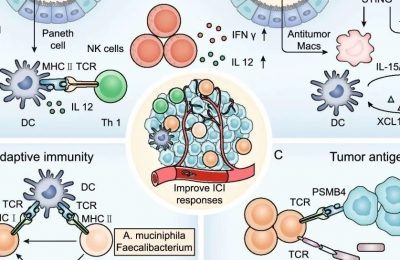
39.4 神经胶质瘤中的检查点抑制剂
临床前研究表明,单药治疗或与检查点抑制剂联合使用,能够有效根除已建立的原位同基因化学诱导胶质瘤。因此,原则上,中枢神经系统并不是对外周诱导的抗肿瘤T细胞反应的不可逾越的屏障。目前,全球有超过20项I-III期试验在胶质瘤患者中使用检查点抑制剂。虽然现有的数据表明毒性特征是可以接受的,并且与其他肿瘤实体相比没有显著差异,但其疗效数据仍然不足。
Anti-CTLA4(抗CTLA-4抗体)作为单一药物的优先级已降低,大多数临床研究集中在使用抗PD-1或抗PD-L1抗体。例如,CheckMate 143(NCT02017717)是一项比较PD-1抗体纳武单抗与贝伐单抗在复发性胶质母细胞瘤患者中的疗效的III期研究,但该研究尚未显示纳武单抗的疗效。另一项研究测试了抗PD-1抗体派姆单抗的安全性和有效性,参与者为80名患有复发性胶质母细胞瘤的患者。该试验已完成(NCT02337491),将比较派姆单抗/贝伐单抗联合治疗与贝伐单抗单药治疗。目前进行的CheckMate 498和548研究(NCT02617589和NCT02667587)则分别分析了纳武单抗在II期和III期设计中,联合放疗或TMZ放化疗对新诊断胶质母细胞瘤患者的疗效。另外,PD-L1抗体Durvalumab也正在复发性胶质母细胞瘤患者的随机II期临床试验中进行测试。
虽然评估这些疗法在胶质瘤中的疗效还为时过早,但反对在未筛选患者中使用检查点抑制剂单药治疗的主要理由是胶质瘤的突变负荷相对较低。胶质瘤的平均非同义突变数为40-80个,比黑色素瘤或小细胞肺癌低一个数量级。反过来,临床前动物模型中的治疗效果可能归因于实验小鼠胶质瘤(如GL261模型)中的相对较高的突变负荷。这些发现表明,不应在未选择的胶质瘤患者中继续进行检查点抑制剂的试验。
相反,研究应聚焦于高突变负荷的患者,这可能由于生殖系错配修复缺陷或长期烷基化化疗引起。在此研究中,高突变负荷胶质瘤患者显示出显著的检查点阻断疗效,部分病例甚至出现了病变缓解。
未来的临床试验应专注于精心筛选的患者群体,并由具有假设检验支持的转化程序推动,尤其是检查点抑制剂与辐射疗法、病毒治疗或特定疫苗的联合使用。这种转化方法要求在治疗后对肿瘤组织进行分析,以评估肿瘤内的免疫反应,但这在胶质瘤中是一个特殊挑战。为此,新辅助试验设计可以一定程度上规避其他肿瘤(如黑色素瘤或胃肠道癌症)中难以执行的活检-治疗-活检概念的困境。
选择用于胶质瘤治疗的检查点抑制剂的类型将取决于靶细胞的分布。例如,PD-L1抑制剂不一定需要穿过血脑屏障,因为PD-L1不仅在胶质瘤的肿瘤微环境中表达,还在患者的循环抗原呈递细胞(APC)中表达升高。与其他肿瘤实体类似,肿瘤内或外周的PD-L1表达可能作为预测反应的生物标志物,为神经胶质瘤的治疗效果提供重要参考。
如果过早进入随机III期试验,且未筛选患者,可能会损害治疗概念的成功,正如在抗血管生成治疗的研究中所看到的那样。胶质母细胞瘤患者中进行的抗血管生成的III期研究未能证明疗效,导致该领域的研究基本上停止。
39.5 T细胞治疗
与其他实体肿瘤类似,T细胞疗法在胶质瘤中的应用仍处于实验阶段。早期研究采用从外周血循环中分离的非特异性活化淋巴细胞(即淋巴因子活化杀伤细胞,LAK),并将其局部注射到肿瘤切除腔中,然而其成功率有限。随着近年来在胶质瘤中发现免疫原性新表位(neo表位),以及在淋巴瘤和实体瘤中采用类似的治疗策略,研究的重点已经转向TCR转基因T细胞的过继转移。
目前,靶向EGFRvIII的CAR-T细胞治疗正在胶质母细胞瘤患者中进行研究,但基于EGFRvIII疫苗试验的阴性结果,这种治疗的成功性依然值得怀疑。最近,使用含有4-1BB和突变IgG4-Fc连接体的修饰CAR转导T细胞,靶向识别肿瘤相关抗原IL13Rα2(白细胞介素-13受体α2),在复发性胶质母细胞瘤和伴有软脑膜和脑脊液扩散的患者中进行局部过继转移治疗(NCT00730613,NCT01082926)。部分患者在接受局部治疗后,出现了中枢神经系统远端病灶的持续部分缓解。然而,最终的肿瘤进展表明免疫逃逸可能与抗原丢失有关。
原则上,这些研究结果指出了两个关键点:(a) 靶向肿瘤相关抗原是有效的;(b) 局部递送(例如通过脑脊液)能够有效将具有特异性活性的抗原特异性T细胞递送至胶质瘤。然而,是否全身递送同样有效,或者是否需要局部递送来克服血脑屏障或血脑脊液屏障,仍需进一步研究验证。
39.6 靶向免疫微环境在胶质瘤中的作用
即使有效的抗肿瘤T细胞反应能够被成功引导至胶质瘤微环境,免疫抑制性质仍然是最终的挑战。胶质瘤微环境中的物理因素,如低pH值和缺氧,特别是在胶质母细胞瘤的坏死区和伪栅栏样坏死区域,广泛存在。这些问题只能通过在免疫治疗前切除大的坏死肿瘤来部分解决。
化疗诱导的细胞死亡在神经胶质瘤中并未显著增强其免疫原性,主要原因是肿瘤对能够诱导免疫原性细胞死亡的药物具有耐药性。其他能够提升免疫原性的治疗手段包括放射治疗和病毒治疗。从机制上讲,这些方法可能通过增强抗原呈递、诱导表位扩散以及利用抗病毒免疫反应来增加对免疫原性抗原的综合免疫反应。
胶质瘤的免疫抑制微环境中,其他影响因素还包括细胞因子(如IL-10)、生长因子(如TGF-β)以及代谢产物(如犬尿氨酸)。目前,这些免疫抑制因子的抑制剂已被开发或正在研发中,然而它们作为单一疗法的效果有限。因此,必须在精心挑选的患者群体中进行适当的组合治疗试验(Fig 39.1)。
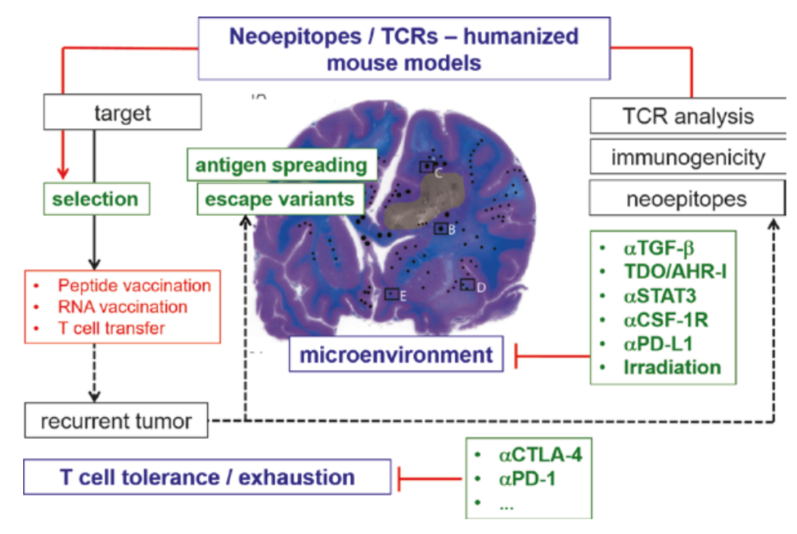
Fig. 39.1 神经肿瘤学中免疫治疗发现和组合治疗方法的工作流程
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 任振阳
图文排版 | 郭震远 麦思淋
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏