导 读
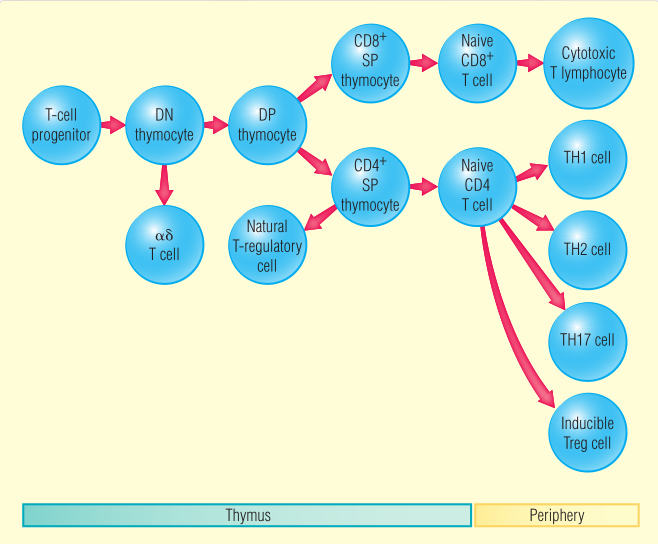
为了保护宿主免受感染,T细胞必须包含针对各种各样抗原的TCR(T cell receptor)的亚群。每个单独的T细胞都表达一种独特的受体,这种受体能够识别由自身主要组织相容性复合体(MHC)分子呈递的外源性多肽抗原。如上图所示,本章主要讲解机体如何产生各种具有不同抗原特异性TCR的成熟T淋巴细胞,以实现对宿主多样化的保护功能。
T淋巴细胞在胸腺中产生,其发育涉及多个步骤并依赖于几个内置检查点来确保T细胞的正常分化。在建立T淋巴细胞库的过程中,只有小部分祖T细胞(胸腺细胞)发育为成熟T细胞进入外周血液和外周淋巴组织;其余大部分祖T细胞(>98%)在选择的过程中死亡。胸腺的选择过程使机体能够形成具有自身耐受但又自我限制的T淋巴细胞库(第八章)。这意味着被选择后发育成熟的T细胞能够识别与自身MHC分子结合的非自身抗原肽,且通常不识别自身多肽。
不同的成熟T细胞亚群执行不同的细胞免疫功能,其中包括了杀死被病毒感染的细胞以及肿瘤细胞(CD8+T细胞),调节免疫系统(CD4+T细胞)等。
胸腺
第13章介绍了胸腺的结构,胸腺分为三个主要区域:被膜下区、皮质层和髓质(Fig. 15.1)。
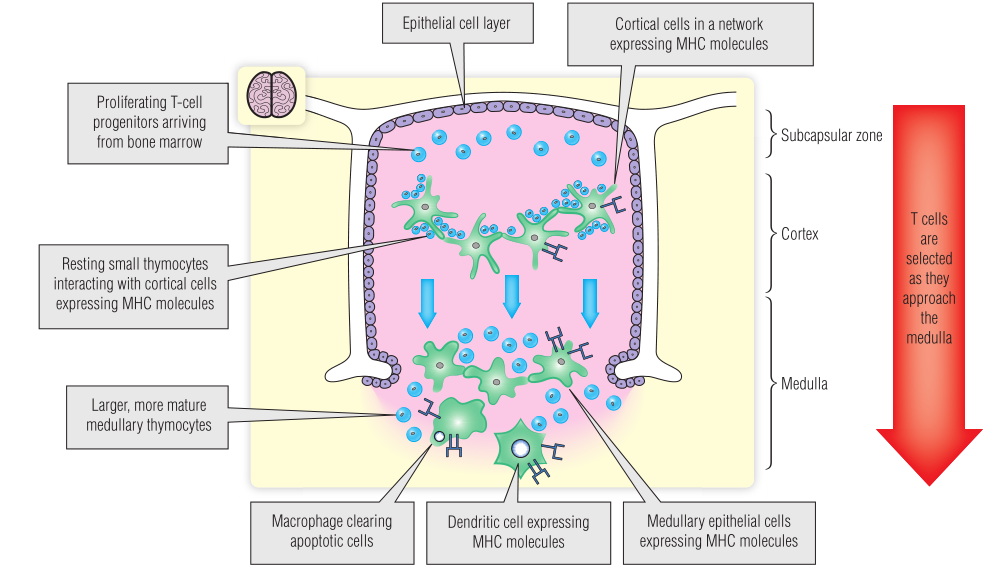
Fig 15.1 胸腺组织的简化示意图。
在这些结构和功能不同的区域中发现了不同的基质细胞和胸腺细胞群。胸腺在T细胞发育中起着关键作用,胸腺缺陷患者体内成熟的外周T细胞极少(Box 15.1)。尽管胸腺在胎儿形成T细胞群方面起着至关重要的作用,但出生后胸腺不再具有使抗原特异性T细胞成熟的功能。成熟的T细胞在白细胞介素7(IL-7)的影响下可进行分裂,以此来维持外周T细胞的数量,因此胸腺切除对人类的T细胞反应几乎没有影响。
胸腺细胞向成熟T细胞转化的研究进展
胸腺细胞的发育分为了几个阶段,这些阶段在胸腺的不同部位进行(Fig.15.2)。在进行更详细的讨论之前,我们先给出这些阶段的概述。
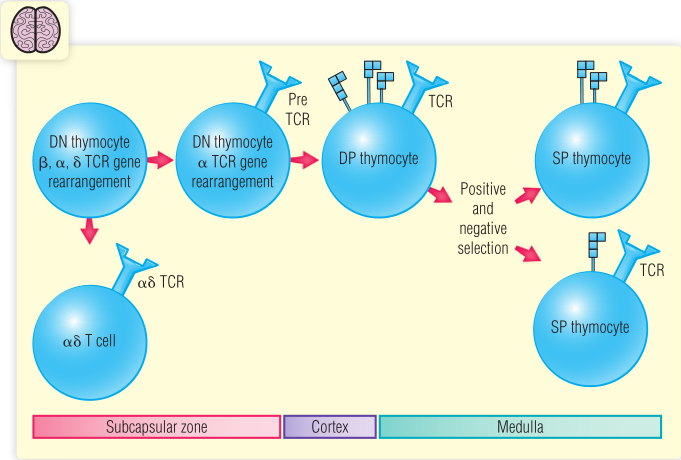
Fig 15.2 胸腺细胞成熟的不同途径概述。
DN,双阴性;DP,双阳性;SP,单阳性;TCR,T细胞受体
骨髓来源的胸腺细胞迁移到胸腺被膜下区域时不表达T细胞特有的CD4和CD8共刺激分子(呈阴性),它们被称为双阴性(DN)细胞(见Fig.15.2)。在这个阶段,T细胞受体(TCR)基因为胚系(未重排)结构。
如Fig15.2所示,DN胸腺细胞亚群经历了几个重要的分化过程。当TCR基因发生重排时,DN细胞开始形成T细胞谱系(稍后描述)。它在这个阶段将做出一个重要选择,形成αβ细胞谱系还是γδT细胞谱系。值得注意的是,这两种T细胞谱系都来自于共同的祖细胞。谱系的形成是一个竞争性过程,这取决于哪种谱系的TCR基因先进行高效重排(与第14章中免疫球蛋白[Ig]轻链基因在B细胞中的表达过程相类似)。大多数胸腺细胞选择αβTCR途径,只有少数胸腺细胞选择γδ途径。因为γδT细胞不受MHC的限制,他们不受胸腺发育的其他过程的影响并且会在这个阶段离开胸腺。
T细胞发育的下一个重要阶段是双阳性(DP)阶段。DP细胞同时表达CD4和CD8,并且只存在于胸腺皮质。在DP阶段,当细胞表达能够识别自身MHC的TCR时,细胞将会通过阳性选择被保留下来。下一步,经过阳性选择存活下来的细胞将迁移到胸腺髓质,在那里它们将会经历阴性选择,也就是说如果它们的TCR可以与自身MHC分子-自身多肽抗原复合物结合以高亲和力结合,那么它们将会发生凋亡。之后DP细胞变为单阳性(SP):CD4–CD8+或CD4–CD8+,这与TCR是与I类还是II类MHC分子相互结合有关。一些CD4+细胞在这个阶段发育成自然调节性T细胞(nTregs)。
T细胞受体基因重排的发生次序
TCR基因重排始于DN阶段,在这个阶段,β,γ和δ基因都可能发生重排。如第7章所述,这涉及到重组激活基因(RAG)和末端脱氧核苷酸转移酶(TDT)的激活,除此之外还有多个基因发生重排。如果产生了功能正常的γδ受体,那么就会产生表达γδTCR的T细胞,从而形成γδ谱系。
然而,大多数DN细胞表达TCRβ链。一旦有功能的TCRβ链在细胞表面表达,它就与恒定的pre-Tα链和CD3分子(第7章、11章)络合,形成Pre-TCR复合体(第7章、11章)。pre-TCR(TCR前体)的表达可促使信号转导的(第11章),来自pre-TCR的信号可阻止β链进一步重排,并使得DP T细胞增殖。重组酶表达后,细胞的增殖进一步促进TCR α链重排。因此,与pre-B细胞受体的作用类似(第14章),pre-T细胞受体的表达是αβTCR组装和αβT细胞群形成的关键步骤。
MHC-自身肽在胸腺中的表达
在发育过程中,未成熟的T细胞会遇到各种表达MHC-自身肽的细胞群。未成熟的T细胞首先会遇到参与阳性选择的胸腺皮质上皮细胞,当其迁移到髓质时,会遇到参与阴性选择的树突状细胞、上皮细胞和巨噬细胞,所有这些细胞群都在主动向未成熟的T细胞递呈抗原肽。
没有感染的情况下抗原提呈细胞(APC)通过第10章所述的途径处理和呈递自身多肽。这意味着正常的细胞质蛋白被蛋白酶消化,并向MHC I类分子呈递。另一方面,胞外蛋白在内体中被消化,向MHC Ⅱ类分子呈递。
胸腺髓质中的细胞能够表达通常在其他器官中表达的蛋白质。例如,通常认为只有胰岛β细胞能分泌胰岛素,胸腺髓细胞也能分泌,这些胰岛素被加工成多肽,呈递在MHC II类分子上。自身免疫调节因子AIRE(一种特殊的转录因子),可使胸腺髓质细胞表达通常仅在其他器官中表达的蛋白质。AIRE基因突变将导致多种自身免疫问题,如自身免疫性多内分泌腺病-念珠菌病-外胚层营养不良综合征(APECED) (Box 15.2)。
阳性选择:自身限制性的形成
为了能够继续发育,DP细胞必须先和胸腺皮质上皮细胞上的MHC分子成功结合。大多数DP细胞在胸腺皮质层凋亡,因为它们缺乏能够与自身MHC分子结合的TCR。只有具有TCR,并且能以适当亲和力识别自身MHC的DP细胞才能存活。阳性选择后的细胞受到自身MHC的限制。
阴性选择:自身免疫耐受的形成
经过阳性选择的细胞群受自身MHC限制,但其中也包括一些能识别自身多肽和MHC的自身反应性细胞。这些自身反应性细胞必须被清除,否则宿主就会有患自身免疫性疾病的风险,这涉及到阴性选择过程。 (Fig. 15.3)
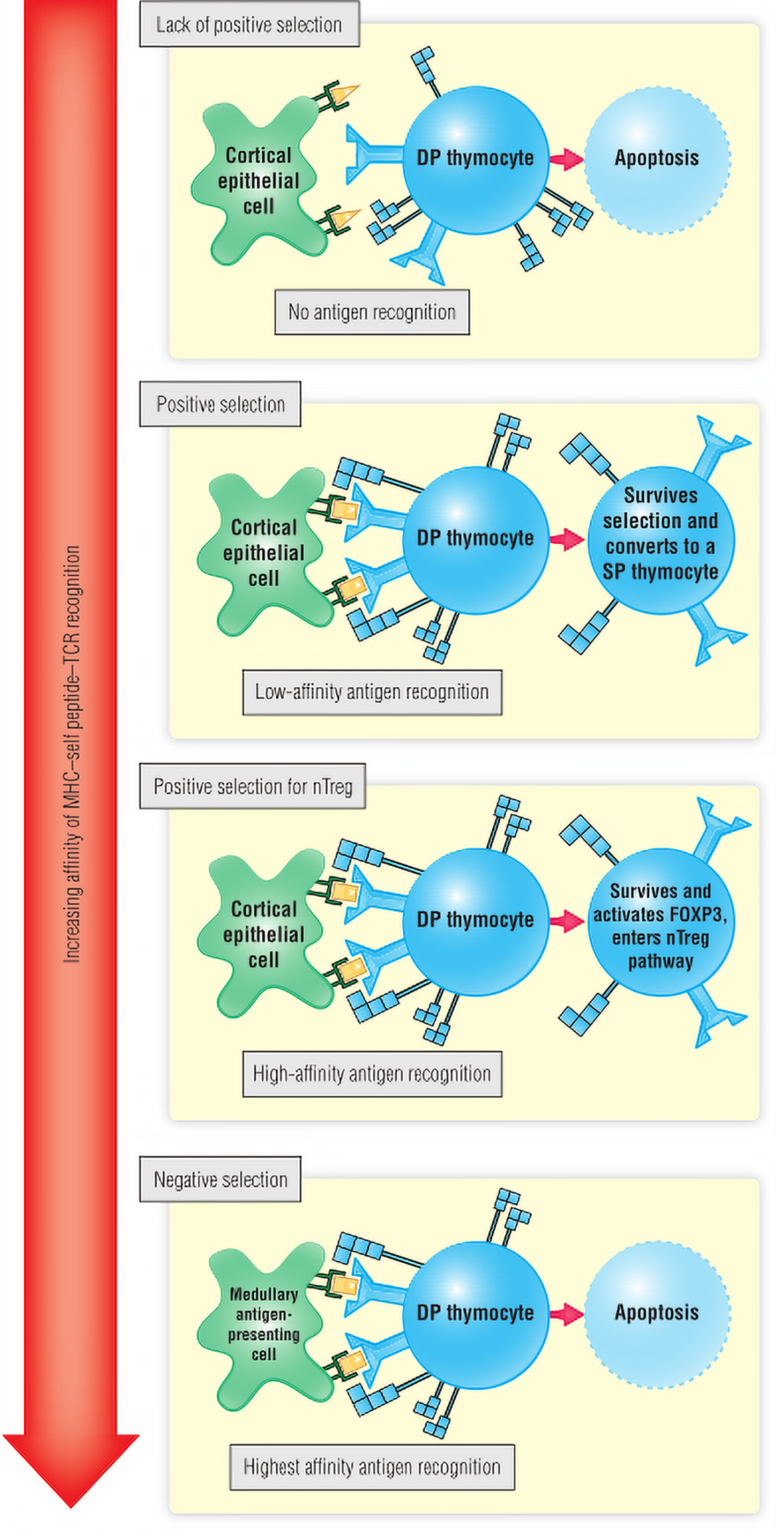
Fig 15.3 双阳性(DP)胸腺细胞与胸腺抗原提呈细胞相互作用可能产生的不同结果。TCR识别MHC-自身肽复合物的亲和力决定了这些结果。DP,双阳性;NT reg,自然T调节细胞;SP,单阳性。
在胸腺髓质发育的DP T细胞暴露在一系列在体内表达的多肽之间,阴性选择过程中,与自身多肽反应非常强烈(高亲和力)的DP细胞被淘汰,以此形成一种自身耐受状态。
接下来是DP细胞能否识别呈递在MHC I类或II类分子上的自身抗原。请记住,CD8分子识别MHC I类,而CD4分子识别MHC II类。识别MHCⅠ类分子上的细胞自身抗原的DP细胞停止表达CD4,转化为单阳性(SP)CD8+细胞。相反,识别MHCⅡ类分子上的细胞自身抗原的DP细胞停止表达CD8,转化为CD4+细胞。
在SP的CD4+细胞中,10%对MHCⅡ类自身抗原具有最高亲和力的细胞激活一种名为FOXP3的转录因子,该转录因子使这些细胞进入不同的分化途径,并最终成熟为自然调节细胞(nTregs)。
阴性选择是通过TCR介导的信号转导诱导细胞凋亡。凋亡的细胞由胸腺巨噬细胞吞噬清除。
据估计,在皮质中通过阳性选择存活下来的细胞中有三分之二随后在髓质中经过阴性选择后凋亡。因此,只有少量的初始胸腺细胞发育为成熟的T细胞进入外周血液和淋巴组织(初始T细胞,antigen-naive, T cells)。“naive”指的是这些细胞还没有遇到与它们的TCR“匹配”的外来的、非自身的抗原。
T细胞受体在阳性选择及阴性选择中的信号转导
TCR与MHC-多肽抗原复合物的结合既介导阳性选择又介导阴性选择(见Fig. 15.3)。
同样类型的受体-配体相互作用怎么会产生截然不同的结果?已有研究表明,TCRs和MHC肽复合物之间相互作用的不同亲和力产生不同的细胞内信号。这些信号可能在数量上或质量上不同。这些信号的性质还在研究中,目前根据现有数据可给出的一个简单解释是,TCR与胸腺细胞上表达的MHC分子以高亲和力结合的细胞发生凋亡,而TCR和MHC分子以较低亲和力(但也不是太低)即“中等亲和力结合”的细胞能够存活并继续发育成熟,B细胞发育过程中也会出现类似的现象。骨髓发育过程中识别大量的膜自身抗原的B细胞也会在类似的阴性选择过程中发生凋亡。
外周:抗原对初始T细胞的激活
离开胸腺的成熟T细胞还没有遇到特异性抗原时被称为幼稚的成熟T细胞(初始T细胞)。这些细胞在遇到抗原或死亡之前,会在血液与中央淋巴器官(如脾、淋巴结、Peyer斑块)间循环达数年之久。
抗原通常会在次级淋巴器官中被专职抗原提呈细胞(APC)获取并提呈(第13章)。如果TCR识别到MHC分子上呈递的抗原(第一信号),并接收到第二个共刺激信号(第16章),T细胞就会被激活(Fig15.4,第11章)。然后被激活的细胞将会增殖、分化为效应细胞,它们大多存活时间较短。初始T细胞接受抗原刺激被激活的这个过程被称为T细胞的活化。这些激活的效应细胞发生了一些变化,其中包括表达新的细胞表面分子,如CD154(CD40配体)和各种黏附分子(第13章和第16章)。效应性T细胞可以移动到周围组织和其他器官直接处理病原体感染,也可以迁移到生发中心发挥作用,如激活对同一抗原具有特异性的B细胞使其分泌抗体。
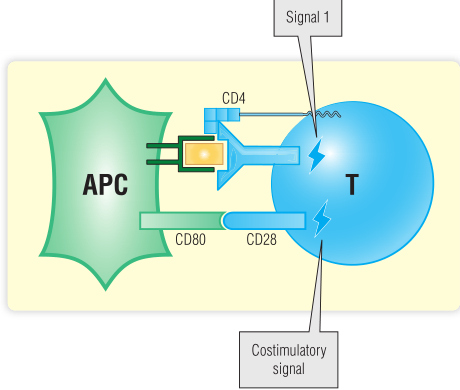
Fig 15.4 激活初始T细胞
最终结果是T细胞的强烈反应和病原体的破坏。然后,大多数激活的T细胞凋亡,从而恢复T细胞群的动态平衡。少数效应细胞成熟为记忆性T细胞,当再次遇到抗原时,记忆性T细胞可以更快更有效地做出反应(第17章)。
外周T细胞耐受性
如上所述,阴性选择产生具有自我耐受性的成熟T细胞群体。在胸腺中发生的阴性选择被称为中枢耐受的诱导。然而,由于不是所有的自身抗原都能在胸腺中遇到,一些自身反应性细胞可能会从胸腺“逃逸”,出现在胸腺之外。在外周有几种机制发挥作用,以确保逃离那里的潜在的自身反应性T细胞的增殖得到控制,并使其对人体无害。
例如:
1.抗原隐藏在免疫赦免区,如大脑、眼睛或睾丸。
2.如果一个T细胞对一种常见的外周抗原是特异的,高水平、持续的抗原刺激导致T细胞被反复活化,那么这个T细胞就会发生凋亡。这种机制被称为活化诱导的细胞凋亡。
3.如果刺激T细胞反应所需的一个成分缺失,T细胞就不会对抗原产生反应。例如,如果相关组织中没有MHC表达或缺少共刺激信号(如CD80/CD28;见Fig15.3),T细胞将处于功能不活跃状态。这种机制被称为“克隆失能”。
4.具有自身抗原特异性的调节性T细胞群“保卫”外周,防止任何自身反应。
这些胸腺外机制被认为可诱导外周免疫耐受的发生,具体将在第18章详细讨论。
成熟T细胞的反应和功能
幼稚成熟T细胞遇到其同源MHC抗原复合物并接收到来自专职APC的共刺激信号后会增殖并分化为效应细胞,然后CD8+和CD4+T细胞亚群可以产生不同的效应功能。
由于CD4+和CD8+效应T细胞的不同特异性,免疫应答可以独立地监测细胞外病原体(如细菌)和细胞内病原体(如病毒)。CD4+T细胞监测MHC II类分子,它提呈内体产生的多肽(例如,来自吞噬作用的细胞外病原体),CD8+T细胞监测MHC I类分子,它提呈细胞质中产生的多肽(例如来自细胞内病原体-在细胞质中复制的病毒等)。
CD4+T细胞
CD4+T细胞识别MHC II类分子上的抗原。正如在第16章中详细讨论的那样,CD4+T细胞可以分化为一系列亚群,包括辅助性亚群,它们促进特定类型的T辅助细胞(TH) (通过TH1、TH2和TH17)和调节性T细胞应答。幼稚T细胞分化为哪种细胞取决于它所处的环境以及先天免疫系统产生的危险信号。例如,当存在危险信号时,IL-12对感染做出反应,那么产生应答的T细胞很可能发育成TH1细胞。n Tregs(自然调节性T细胞)是TCR和MHC Ⅱ类自身多肽之间高亲和力相互作用的结果,但又不足以引起阴性选择。第二种调节性T细胞是适应性调节性T细胞 (iTregs)。这些细胞是在适当的环境中从幼稚的CD4+T细胞中诱导产生的。调节性T细胞将在第18章中详细讨论。
CD8+T细胞:细胞毒性T细胞
CD8+T细胞在胸腺生成。它们需要进一步的活化和分化才能成为效应T细胞,效应T细胞能够识别被病毒感染的靶细胞和肿瘤细胞(Box 15.3)。CD8+T细胞识别MHC I类分子上的抗原。MHC I类分子几乎存在于人体所有有核细胞中,所以CD8+T细胞可以监测所有细胞的感染迹象。CD8+T细胞被激活成为效应T细胞的方式有两种,一种是遇到专职APC上的抗原并同时接受来自MHC-I类分子(第一信号)和共刺激分子(如CD80,第二信号)的激活信号,另一种是遇到非APC靶细胞上的抗原并从CD4+T辅助细胞释放的细胞因子那里接收“第二信号”。CD8+T细胞通过多种机制抑制细胞内感染,诱导感染细胞凋亡。
γδT细胞亚群
如本章前面所述,表达γδTCR的T细胞占所有T细胞中的一小部分(<5%),并且与αβT细胞是不同的谱系。γδTCR识别抗原的方式与αβTCR不同,因为γδTCR可以在没有MHCⅠ类或Ⅱ类分子的情况下识别到某些未经处理的肽和非肽抗原。
γδT细胞作为第一道防线的一部分,主要识别皮肤和肠道粘膜中的微生物入侵者。它们能识别常见的微生物病原体。
它们不需要加工和呈递就能识别一些常见的微生物蛋白和非蛋白抗原,如细菌细胞壁磷脂,这有别于αβT细胞,并使得它们在抵御微生物入侵的第一道防线中具有独特的保护作用。
BOX 15.1 不完全性Di George综合征
一个婴儿被诊断出食道和气管之间有瘘道,并且由于低钙发生了抽搐。面部五官发育不良,胸部X线片显示胸腺缺失,这些是Di George综合征的常见症状。在该综合症中,第三和第四咽囊的结构发育不良,包括控制血液钙水平的胸腺和甲状旁腺。幸运的是这名婴儿没有心脏缺陷(心脏缺陷是Di George 综合征另一种主要异常症状)。进一步的检测显示她的22号染色体有一部分缺失,这也证实了这一诊断。
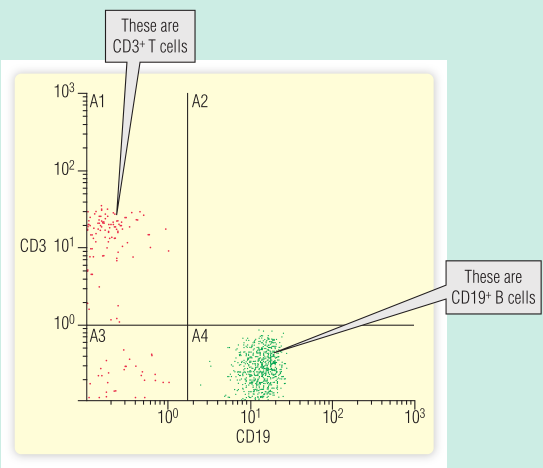
Fig 15.5 一例患有Di George综合征女婴的淋巴细胞的流式细胞仪分析。尽管T细胞数量很低,这个婴儿还是存活了下来。
虽然观察到CD3+T细胞数量减少,但该婴儿的发育仍较正常(Fig. 15.5)。她的免疫球蛋白水平是正常的。因此很好地抵御了正常的儿童时期感染,没有接受任何特殊的免疫治疗。在成年初期,她过着正常的生活(Fig. 15.6)。

Fig 15.6 Di George综合征患者表现出这种微妙的“小精灵样”表情
不完全性Di George综合征的儿童在没有其他相关的疾病,如心脏缺陷的情况下往往能够发育正常,就像我们正常人一样。而完全性Di George综合征患者与患有严重联合免疫缺陷疾病的患者(SCID;第32章)一样,容易发生机会性感染,如真菌和病毒感染等。
BOX 15.2自身免疫性多内分泌腺病-念珠菌病-外胚层营养不良综合征(APECED)
一名4岁男孩有腹泻、体重减轻、低血压及学龄前障碍等症状。诊断出患有乳糜泻(第28章),但开始无麸质饮食后,病情没有改善。随后,诊断肾上腺功能衰竭、甲状腺功能减退和口腔念珠菌感染。他的哥哥也有甲状腺疾病。这些特征提示他可能患有自身免疫性多内分泌腺病-念珠菌病-外胚层营养不良综合征。随后对他进行了基因检测并发现AIRE基因的纯合子突变,这证实了他患有APECED。临床上,甲状腺功能减退症和肾上腺功能衰竭可用激素替代治疗,念珠菌感染也得到了治疗。患此类疾病的病人容易在年轻的时候就发生全秃(并发症)(Fig. 15.7)。

Fig 15.7 自身免疫性多内分泌腺病-念珠菌病-外胚层发育不良综合征患者
APECED是由AIRE基因突变引起,胸腺细胞不能表达其他器官如甲状腺的蛋白质。由于这一缺陷,使得识别来自这些蛋白质的肽的胸腺细胞没有凋亡,使自身反应性T细胞离开胸腺而导致自身免疫性疾病。第16章解释了念珠菌感染的原因。
APECED是一种罕见的自身免疫性疾病,是自身耐受没有形成所造成的严重后果。
本文由Oncolab实验室微信公众号翻译整理自Immunology for Medical Students,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 往期精彩内容推荐

长按上方二维码即可关注本号~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏