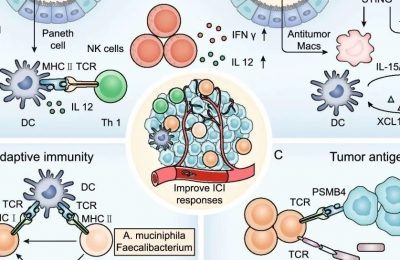
在前面两次的分享中我们已经学习了肿瘤微环境的相关内容,详见人类肿瘤微环境(上)以及人类肿瘤微环境(下),那么在今天以及下期的分享中我们就来学习一下在抗肿瘤免疫中的一种非常关键的细胞亚群-CD8+ T细胞,看看它在目前常用的一些抗肿瘤疗法中究竟起到一个怎样的作用。
3.1 简介
大量研究表明,T细胞(尤其是CD8+ T细胞)浸润到肿瘤微环境中是许多恶性肿瘤预后良好的特征,包括头颈部黑素瘤,乳腺癌,卵巢癌,肾癌,膀胱癌,尿路上皮癌,结肠直肠癌,前列腺癌,胰腺癌和肺癌。瘤内高密度的CD8+ T细胞与患者较长的无病生存期(DFS)和总生存期(OS)相关。有趣的是,CD8+T细胞可能不需要直接接触肿瘤,因为上皮内CD8+ T细胞和间质内CD8+ T细胞在人乳腺癌和卵巢癌中都与良好的预后相关。
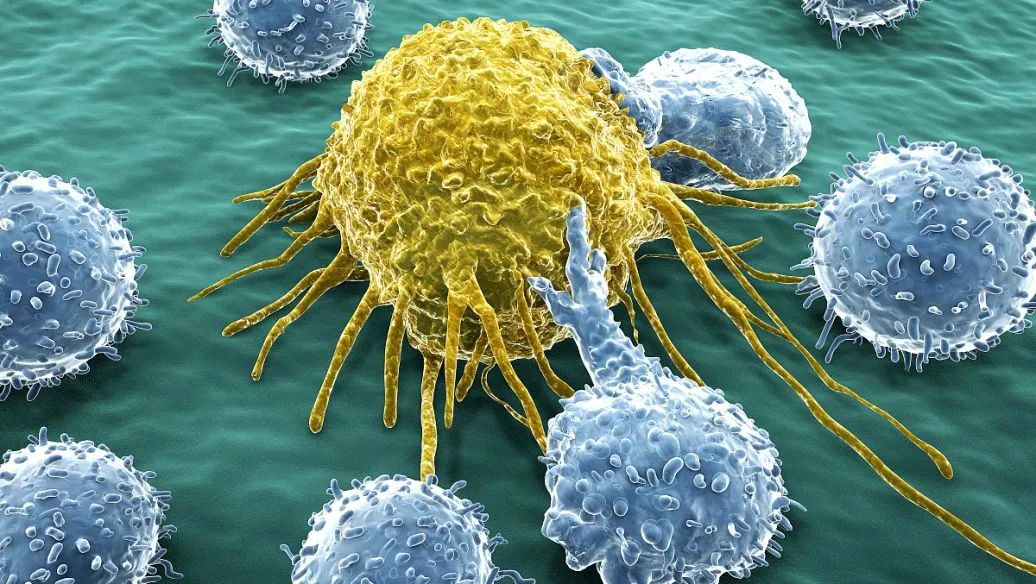
CD8+T细胞(细胞毒性T淋巴细胞,CTLs),能够直接杀死靶细胞。CD8+ T细胞在抗原刺激下逐渐从幼稚T细胞分化为中枢记忆T细胞(central memory T cells, TCM)和效应记忆T细胞(effect memory T cells, TEM)。效应功能随着CD8+ T细胞分化而增强,而记忆功能和增殖功能则下降。效应细胞表面标志为CCR7−CD62L−CD45RO+CD95+IL2Rb+,它们不表达杀伤细胞凝集素样受体G1 (KLRG-1)和程序性死亡受体1(PD-1),分泌高浓度的IFNγ和TNFα,以及少量的IL2。CD8+ T细胞的转运是由趋化因子-趋化因子受体相互作用介导的,其中包括配体CXCL9和CXCL10及其受体CXCR3,CXCL9/10表达的增加与肿瘤微环境中CD8+T细胞数量增加相关。
CD8+T细胞是肿瘤免疫的重要组成部分,它通过多种机制清除肿瘤。首先,CD8+T细胞识别肿瘤细胞上表达的特定肿瘤相关抗原,释放细胞毒性分子颗粒酶B和穿孔素进入肿瘤细胞,诱导caspase激活,最终导致肿瘤细胞凋亡。其次,CD8+T细胞也可以通过Fas/Fas配体途径诱导癌细胞死亡,小鼠肺癌和B细胞淋巴瘤模型已经证明在CD8+T细胞介导的肿瘤消退中Fas配体是必不可少的。CD8+T细胞分泌的IFNγ和TNFα具有抗肿瘤活性,能够控制肿瘤生长,IFNγ和TNFα联合作用可促使癌细胞衰老。此外,IFNγ还可以增强抗原提呈以及抑制肿瘤血管生成,在癌症免疫监视中也起着至关重要的作用。
尽管肿瘤反应性CD8T细胞常在肿瘤活检中被发现,但肿瘤细胞仍会增殖,免疫抑制性的肿瘤微环境可能会导致CD8+T细胞衰老。衰老的CD8+T细胞端粒变短、DNA损伤应答基因被激活,分泌细胞衰老相关分泌表型(SASP)因子。这些细胞的表型表现为共刺激分子CD27和CD28的下调和CD57和KLRG1的高表达。尽管衰老的T细胞细胞周期被阻滞,但仍可保留细胞毒性,衰老的T细胞增殖减少、细胞因子产生减少,细胞毒功能下降,同时它高表达共同抑制分子如PD-1、CD244、CD160、CTLA-4、Lag-3和Tim-3。但值得注意的是,CD8+T细胞的衰老在一定程度上是可逆的。研究表明,阻断CTLA-4或PD-1可以改善CD8+ T细胞的效应功能,从而改善临床效果。此外,过继输注体外扩增的肿瘤特异性T细胞,特别是CD8+T细胞,能够逐渐消除肿瘤,甚至治愈恶性疾病。有趣的是,最近的研究表明,基于抗体的靶向治疗、放疗和化疗可能协同启动或增强抗肿瘤免疫反应,这些疗法的抗肿瘤效果部分依赖于CD8+T细胞免疫。
这篇综述主要关注效应CD8+ T细胞在T细胞过继疗法、检查点阻断、基于抗体的靶向治疗、放疗和细胞毒性化疗中的作用。我们总结了关于这些疗法如何增加肿瘤内CD8+T细胞的浸润,诱导肿瘤抗原特异性CD8+ T细胞反应,激活CD8+ T细胞效应功能,以及如何使肿瘤对CD8+ T细胞敏感。最后,我们讨论了如何合理地将免疫治疗和放疗或化疗相结合,以此来改善癌症患者的预后。
3.2 免疫疗法中的CD8+ T细胞
3.2.1 T细胞过继疗法
T细胞过继转移疗法(ACT)是一种输血疗法,包括输注各种体外扩增的T细胞群。ACT的第一个方法是自体体外扩增的肿瘤浸润淋巴细胞(TILs)的过继转移,这是临床试验中研究最广泛的方法。最近,转基因T细胞的移植正在开发和应用于临床。该方法利用外周血淋巴细胞来源的表达肿瘤抗原特异性T细胞受体的T细胞,或者是“嵌合抗原受体(CAR)”的T细胞等。
CD8+ T在肿瘤浸润性淋巴细胞治疗中的作用
ACT的一般方案包括:
(1)收集循环的或肿瘤浸润性淋巴细胞;
(2)体外选择和扩增肿瘤特异性T细胞亚群;
(3)对选择出的T细胞进行IL-2刺激扩增,对病人进行淋巴细胞清除后重新输入特异性T细胞。
到目前为止,体外扩增TIL的ACT被认为是治疗化疗难治性转移性黑色素瘤患者的最佳治疗方法。从患者身上获取TIL后,用IL-2和CD3进行长期体外刺激,以此来扩增CD4+和CD8+ αβ TCR+ T 细胞 。CD8+T细胞能与肿瘤细胞上表达的MHC-I类分子相互作用,因此认为CD8+T细胞是影响ACT的抗肿瘤活性重要因素,但CD4+T细胞与肿瘤的间接相互作用也不能被忽视。最近的一项临床研究描述了用自体TIL联合淋巴清除和IL-2来治疗转移性黑色素瘤的三个序贯试验,这三个使用了不同淋巴清除方案的试验中,客观应答率为从47%到72%不等。此外,研究还发现,注入的CD27+CD8+细胞的数量与客观反应相关,进一步证实了其他同样发现较高数量的CD8+T细胞输注与临床反应呈正相关的黑色素瘤ACT试验。
多克隆肿瘤浸润性T细胞的非选择性扩增形成了一个能够识别多种肿瘤相关抗原的群体。这些抗原包括在发育过程中表达并在肿瘤中被重新激活的肿瘤-睾丸抗原,如NY-ESO-1和MAGE。黑素细胞系抗原,如gp100、MART-1和酪氨酸酶;以及癌细胞中存在的低保真复制产生的突变抗原。最近一项研究分析了临床上能够有效被TIL识别的抗原,这些TIL来自肿瘤浸润性淋巴细胞ACT治疗后超过5年黑色素瘤完全消退的患者,并鉴定出自体TIL可以识别的非突变和突变抗原。最近,从黑色素瘤患者的血液和原发肿瘤中成功分离出包括CD8+T细胞在内的新抗原特异性T细胞。近期的一份病例报告显示,采用转移性KRAS突变结直肠癌患者TIL进行的ACT可以导致所有转移性病灶的持久消退。相关研究表明,四种对突变的KRAS G12D有特异性反应的CD8+T细胞克隆介导了这一反应。这突显了一种新兴的治疗策略,即可以利用细胞免疫来瞄准一些药物抑制效果不佳的保守突变癌基因。
除了TAA的特异性,新的发现表明T细胞群的分化状态对ACT的抗肿瘤疗效至关重要。体外扩增TIL中的CD8+T细胞主要由分化程度较低的效应记忆T细胞(TEM)、分化程度较高的效应T细胞(TEFF)和终末分化的效应T细胞(TTDE)组成。相对地,体外培养的TIL中很少发现中央记忆型T细胞(TCM),而在临床前和临床模型中,与小鼠黑色素瘤模型中的效应T细胞相比,TCM细胞表现出更强的抗肿瘤活性。目前,对于人类TIL的ACT来说,哪种分化状态的CD8+T细胞是最合适的,还知之甚少。
基因工程T细胞
T细胞可以通过基因工程表达一种对靶抗原具有高度亲和力和特异性的T细胞受体(TCR),TCR基因的导入通过逆转录病毒或慢病毒介导完成。这种TCR修饰的T细胞对肿瘤相关抗原具有特异性,可以在体外快速扩增并回输到患者体内进行ACT,在部分患者中已观察到肿瘤消退和持久的客观反应。
嵌合抗原受体(CARS)是为转导的T细胞提供特异性的另一种方法,CAR分子是由抗体衍生的单链可变区(scFv)与跨膜区和胞浆区融合而成的人工受体。scFv片段以不依赖于MHC的方式识别特定的肿瘤抗原。胞质结构域由一个CD3 Zeta激活结构域和两个共刺激分子CD28和CD137/4-1BB组成。当遇到抗原时,CAR将活化信号传递给T细胞,刺激具有细胞毒功能的T细胞的增殖扩增。临床试验表明CAR-T细胞过继治疗恶性血液病效果良好。几乎所有的B细胞恶性肿瘤以及正常的B细胞都表达CD19,而其他类型细胞则不表达。因此,靶向CD19的CAR-T细胞被设计成以CD19+B细胞为靶点,并且在60-90%的复发或难治性淋巴母细胞白血病患者中有不错的应答率。另外针对一些疾病部位的实体肿瘤的CAR-T细胞疗法也在研发中,但脱靶毒性问题始终是一个阻碍。
类似TIL的方式,用于ACT的转基因T细胞也包含CD4+和CD8+T细胞群,这两种T细胞都能产生抗肿瘤反应。在最近一项针对B细胞恶性肿瘤患者的临床试验中,以1:1的比例输注由体外扩增的CD8+和CD4 T细胞亚群产生CD19-CAR-T细胞,93%的患者得到缓解,这种确定成分的产品显示出显著的抗肿瘤活性。与多克隆TILs相比,基因修饰的T细胞对单个靶抗原具有单克隆特异性,这可能有助于肿瘤免疫编辑的发生,从而允许抗原逃逸的肿瘤亚克隆的形成和生长。
3.2.2 免疫检查点阻断
免疫系统的特点是具有代偿抑制机制,以防止炎症反应引发自身免疫。识别并准备消灭肿瘤细胞的肿瘤浸润性T细胞接收到抑制信号时会抑制激活和降低效应功能。T细胞活化的负向调控点或检查点的分子有细胞毒性T淋巴细胞相关抗原4(CTLA4)、PD-1和PD-L1。阻断这些检查点的药物可以释放T细胞的抗肿瘤活性,并介导持久的癌症消退。阻断CTLA4、PD-1或PD-L1的多种治疗性抗体已被批准使用,并在包括黑色素瘤、非小细胞肺癌、肾癌和霍奇金淋巴瘤在内的多种实体和液体肿瘤的临床治疗中发挥疗效。
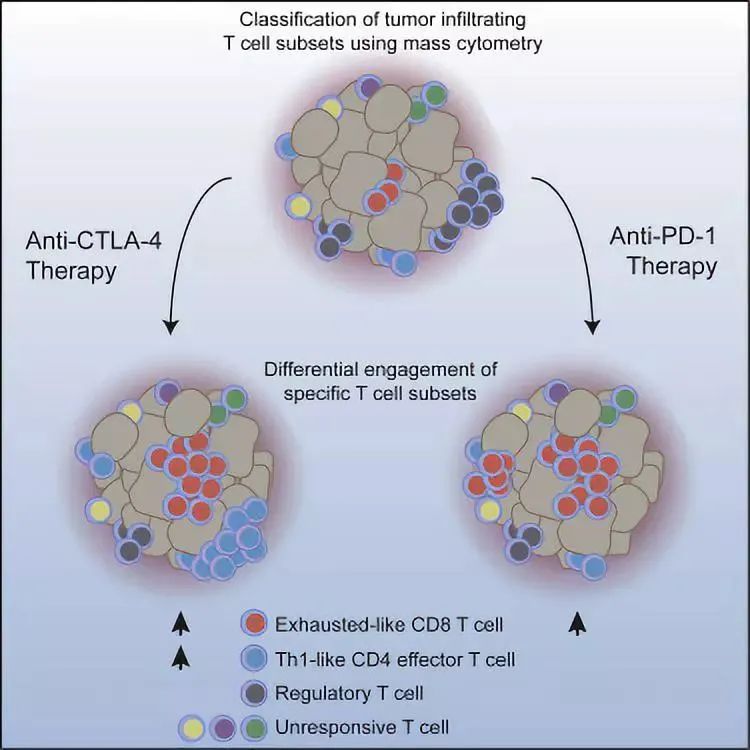
CTLA-4阻断疗法的生物学基础
CTLA-4是一种仅在T细胞上表达的受体,主要调节早期阶段的T细胞激活。CTLA-4很大程度上是通过抑制T细胞共刺激受体CD28的活性来抑制T细胞的功能。TCR对MHC的识别不足以激活T细胞,必须同时通过CD28与其配体CD80和CD86结合才能进行激活扩增。CTLA-4与CD28具有相同的一组配体,但CTLA-4的亲和力要高得多,因此,在结合CD80和CD86方面胜过CD28,同时又主动向T细胞传递抑制信号来抑制T细胞的激活。CTLA-4还通过耗尽抗原提呈细胞表面的CD80和CD86来抑制T细胞的激活。CTLA-4缺陷的小鼠的全身性免疫激活致死性表型证明了CTLA-4在维持正常免疫稳态中的重要作用。
在CTLA-4的生物学基础上,开发了抗CTLA-4的治疗性抗体ipilimumab(伊匹单抗),并批准其用于晚期黑色素瘤患者的治疗。Ipilimumab与CTLA-4的结合阻断了其与CD80和CD86的连接,阻止抑制性信号转导,因此CD28介导的共刺激增强。CTLA-4主要表达在CD4+T细胞上,阻断CTLA-4可通过增强效应分子CD4+T细胞活性和抑制调节性T(Treg)细胞依赖的免疫抑制活性来介导抗肿瘤免疫反应。在Treg细胞中,CTLA-4受转录因子FOXP3的调控而有组织地表达。已有研究表明,抗CTLA-4抗体可通过抗体依赖的细胞毒作用(ADCC)以Fc介导的方式耗尽肿瘤微环境中的Treg细胞群。
CTLA-4阻断疗法中的CD8+T细胞
除了CD4+T细胞,CTLA-4阻断还可增强肿瘤微环境中CD8+T细胞的应答。由于CTLA-4也表达在活化的CD8+效应T细胞上,所以CTLA-4的阻断被认为能够直接调节CD8+T细胞的活性。CTLA-4通过抑制CD8+T细胞中干扰素γ和脱中胚蛋白的产生来调节其效应功能。阻断CTLA-4还被证明可以在体外和体内以一种独立于CD4+T细胞辅助的方式直接促进特定CD8+T细胞的增殖和激活。然而,不同小鼠肿瘤模型的研究表明,阻断CTLA-4也可以通过CD4+T细胞依赖的机制逆转CD8+T细胞耐受,介导抗肿瘤免疫反应。不管CTLA-4阻断针对的是哪种细胞类型,治疗的结果都是使肿瘤特异性CD8+T细胞增强和肿瘤消退。黑色素瘤患者使用ipilimumab治疗可使得肿瘤特异性CD8+T细胞在肿瘤微环境和体循环中克隆性增殖,尽管这与ipilimumab诱导的毒性有关。Ipilimumab还可以增加循环中CD8+T细胞的绝对数量,这与改善临床疗效相关。
PD-L1/PD-1阻断疗法的生物学基础
PD-1是与CD28和CTLA-4同属一个免疫球蛋白家族的细胞表面受体。与CTLA-4类似,PD-1在静息的幼稚T细胞和记忆T细胞上缺失,而在T细胞活化后被诱导产生。但是,与CTLA-4相反,激活的T细胞表面PD-1的表达是在转录水平启动,因此是延迟的。与CTLA-4不同的是CTLA-4主要在T细胞激活的早期阶段调节,PD-1则是在外周组织和肿瘤的效应期抑制效应T细胞的活性。PD-1与配体结合导致抑制磷酸酶SHP-2和PP2A的激活,这两个酶可以抑制T细胞激活所需的激酶发出激活信号。
PD-1的配体是PD-L1(PD-L1,B7-H1,CD274)和PD-L2(PD-L2,B7-DC,CD273) 。PD-L1具有独立于PD-1的免疫调节功能,还可以结合活化的T细胞和APC上的CD80来传递抑制信号,这种相互作用与抗肿瘤免疫耐药的相关性尚未确定。此外,PD-L1的参与使得双向信号传递到T细胞和肿瘤细胞从而调节它们的存活,因此,PD-L1可能通过同时作为配体和受体来调节肿瘤免疫。同样,PD-L2可以通过PD-1传递抑制信号,也可以通过排斥性引导分子b(RGMb)传递信号来促进呼吸耐受。PD-L2信号与癌症免疫的相关性尚不清楚,因为它在肿瘤或免疫细胞中并没有广泛表达。
临床上,PD通路的阻断,可以采用抗PD-1和抗PD-L1抗体,它在不同肿瘤中表现出高且持久的应答率和较低的毒性,适用的肿瘤类型能从实体瘤横跨至血液恶性肿瘤等。从理论上讲,由于表达这两种分子的细胞群体不同,靶向PD-1与靶向PD-L1可能会导致不同的生物学效应。除了活化的T细胞外,B细胞和自然杀伤(NK)细胞上也发现了PD-1的表达,因此,阻断PD-1也可能影响这些细胞的功能。PD-L1在肿瘤细胞和肿瘤相关的APC上高表达,包括DC、巨噬细胞、成纤维细胞和T细胞。不同类型细胞上的PD-L1可能通过不同的机制介导免疫调节。由于临床数据尚不成熟,抗PD-1和抗PD-L1抗体之间的有效性比较尚不能进行,来自临床研究的生物学推断可能因嵌合程度不同和抗体同型亚群不同而受到限制。
PD-L1/PD-1阻断疗法中的CD8+T细胞
虽然细胞和分子机制尚未完全明确,但临床研究表明,PD-1和PD-L1抑制剂均可对肿瘤浸润的CD8+T细胞产生影响。在肿瘤微环境中,PD-1在浸润的淋巴细胞(包括肿瘤特异性CD8+T细胞)上高表达,其与肿瘤细胞或APC上PD-L1的结合可导致CD8+T细胞功能障碍。对接受抗PD-1抗体(Pembrolizumab)治疗的黑色素瘤患者的分析显示,那些对治疗有反应的患者瘤内CD8+记忆T细胞显著增加。PD-1阻断可促进具有衰老表型的效应记忆CD8+T细胞的增殖。此外,PD-L1抑制剂可逆转耗竭性CD8+T细胞的功能,而抗CD27可协同这一作用。这些研究表明,抗PD-1抗体和抗PD-L1抗体均可促进CD8+T细胞增殖和效应细胞因子的产生,从而促进抗肿瘤活性。最近对黑色素瘤的临床研究进一步证明,热肿瘤对PD通路阻断高度敏感。热肿瘤的特征是具有Th1型免疫特征,包括有Th1型趋化因子、CD8+T细胞和高水平的PD-L1表达。治疗性PD阻断介导的肿瘤消退需要肿瘤微环境中预先存在CD8+T细胞。
3.2.3 基于抗体的靶向治疗
基于抗体的癌症治疗已经建立了十多年,这种疗法的基础是与正常组织相比癌细胞表面抗原的差异上调或突变。酪氨酸激酶受体,如EGFR和HER2(ERBB2),已被发现在各种类型的癌症中过表达或突变,包括乳腺癌、肺癌、脑肿瘤、头颈部肿瘤和结肠肿瘤。EGFR和HER2酪氨酸激酶活性异常可促进癌细胞增殖和肿瘤形成。针对HER2和EGFR的单克隆抗体已经得到FDA的批准,目前正被用于各种疾病部位。这些抗体拮抗致癌受体,从而导致肿瘤细胞的增殖减少和凋亡增加。此外,抗体的抗肿瘤作用也是由抗体的Fc区介导的,它可以与巨噬细胞、中性粒细胞和自然杀伤(NK)细胞上的Fc受体结合,并通过激活补体依赖性细胞毒(CDC)和ADCC来诱导细胞死亡。
有趣的是,最近的研究表明,包括CD8+T细胞应答在内的获得性免疫有助于抗HER2和抗EGFR抗体的疗效,一种过表达HER2的小鼠乳腺癌模型表明,抗HER2/neu抗体治疗需要CD8+T细胞。这一结果得到了另一种免疫活性小鼠HER2乳腺癌模型的证实,该模型表明产生干扰素γ的CD8+T细胞是抗体治疗所必需的。同样,一项使用小鼠EGFR+肺癌模型的研究表明,抗EGFR抗体Cetuximab(西妥昔单抗)诱导了肿瘤特异性CD8+T细胞反应,这是抗体发挥效力所必需的。此外,Cetuximab被证明能够促进树突状细胞成熟和CD8+T细胞的活化,使得头颈癌患者肿瘤特异性T细胞激活。
Bevacizumab(贝伐单抗)是一种针对血管内皮生长因子A(VEGF-A)的人源化单克隆抗体,可用于治疗多种恶性肿瘤,包括结肠癌、肺癌、多形性胶质母细胞瘤和肾癌。VEGF-A是一种分泌因子,通过与VEGFR1和VEGFR2受体结合在肿瘤血管生成中起关键作用,贝伐单抗结合并中和所有人类VEGF-A亚型,从而阻断血管生成。除了对肿瘤血管形成有直接作用外,抗VEGF-A抗体还可以调节肿瘤微环境中的免疫细胞。阻断VEGF-A可促进DC成熟,抑制调节性T细胞和MDSCs等免疫抑制细胞的浸润。在结直肠癌小鼠模型中,有报道称VEGF-A通过增强PD-1和其他抑制检查点的表达来调节CD8+T细胞的衰老,这种衰老表型可以被抗VEGF-A抗体治疗所消除,VEGF-A还可通过减少内皮细胞黏附分子的表达来抑制T细胞的浸润。抗VEGF-A抗体对肿瘤血管的调节或正常化可使得肿瘤内T细胞募集和浸润增加。在转移性肾癌患者中,使用Bevacizumab治疗增加了肿瘤内CD4+和CD8+T细胞浸润,Bevacizumab与抗PD-L1抗体联合治疗肾癌也观察到瘤内T细胞增加。
好了,我们本期的分享就到这里,下期再见!
由于微信公众号推送规则变化,为了能够及时收到我们的推送,建议多多点赞、在看、收藏并添加星标哦~~~
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
作者 | Weimin Wang • Michael Green • J. Rebecca Liu •
Theodore S. Lawrence • Weiping Zou
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡-OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频-中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程-中西医结合基础研究中心
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA-I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图-OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
健康养生系列

关注本号~

加入读者交流群~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏