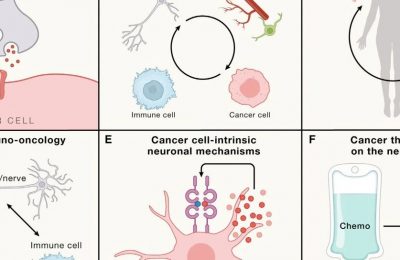
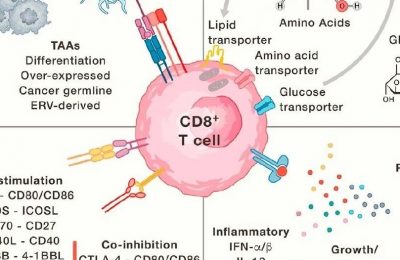
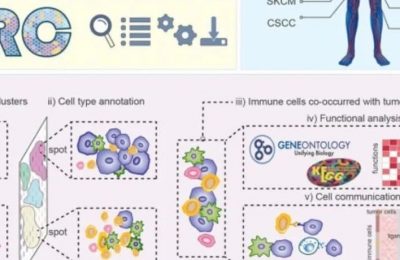
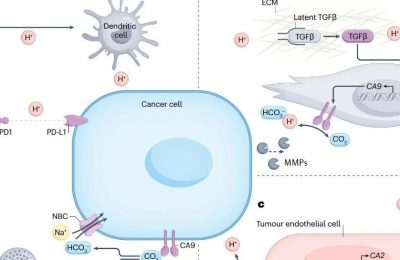
肿瘤相关巨噬细胞(TAM)

肿瘤相关巨噬细胞的存在(TAM)通常与实体瘤预后不良相关。TAMs抑制多种常规治疗,包括化疗,放疗,血管生成抑制剂。因而研究TAM是研究肿瘤免疫学,以及基于此进行免疫治疗的基础。
巨噬细胞来源于胚胎或成人造血干细胞(HSC)祖细胞,在稳态条件下,这些群体的相对贡献因组织而异。单核细胞衍生的巨噬细胞,则在炎症性疾病,包括肿瘤,免疫调节中起着重要作用。发育起源,及组织环境是巨噬细胞极化,并参与免疫调节的基础。
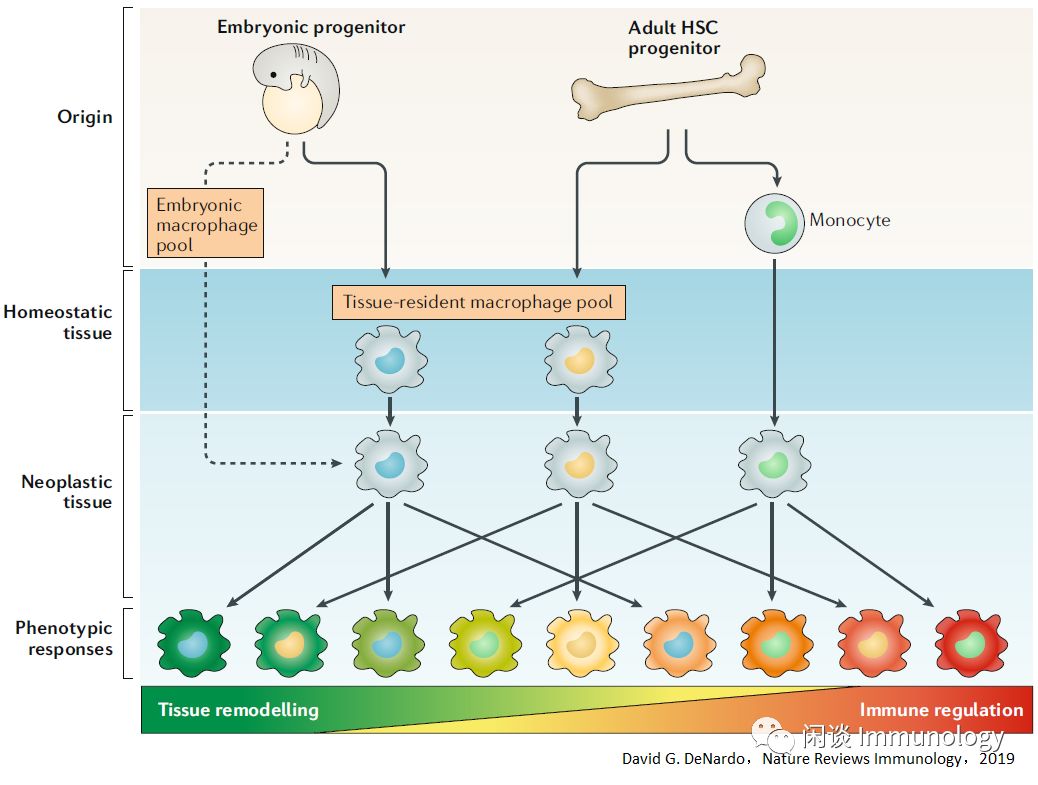
-
调节TAM表型
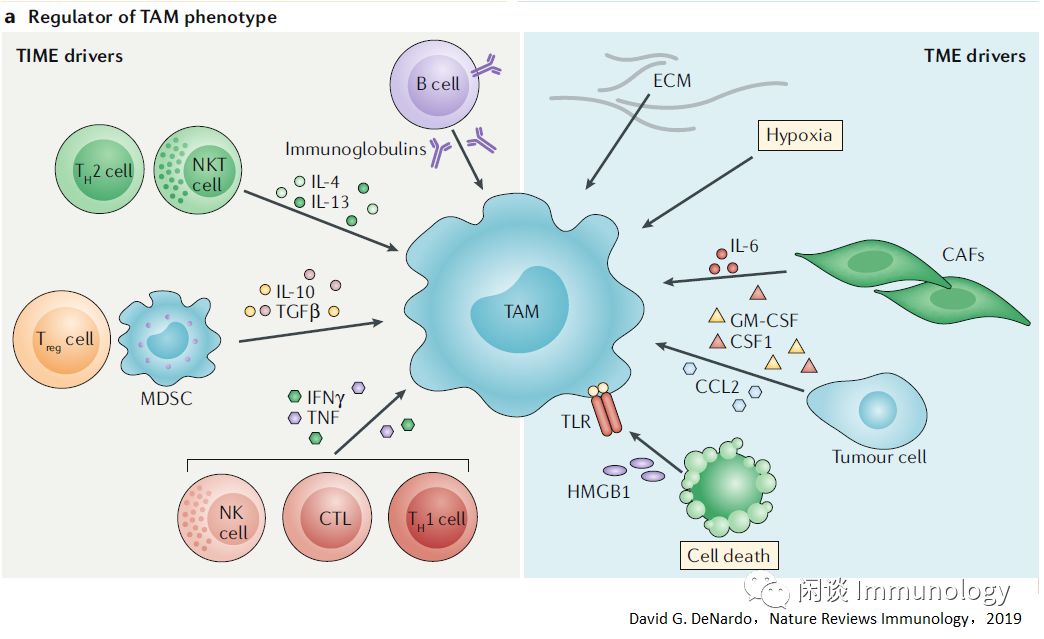
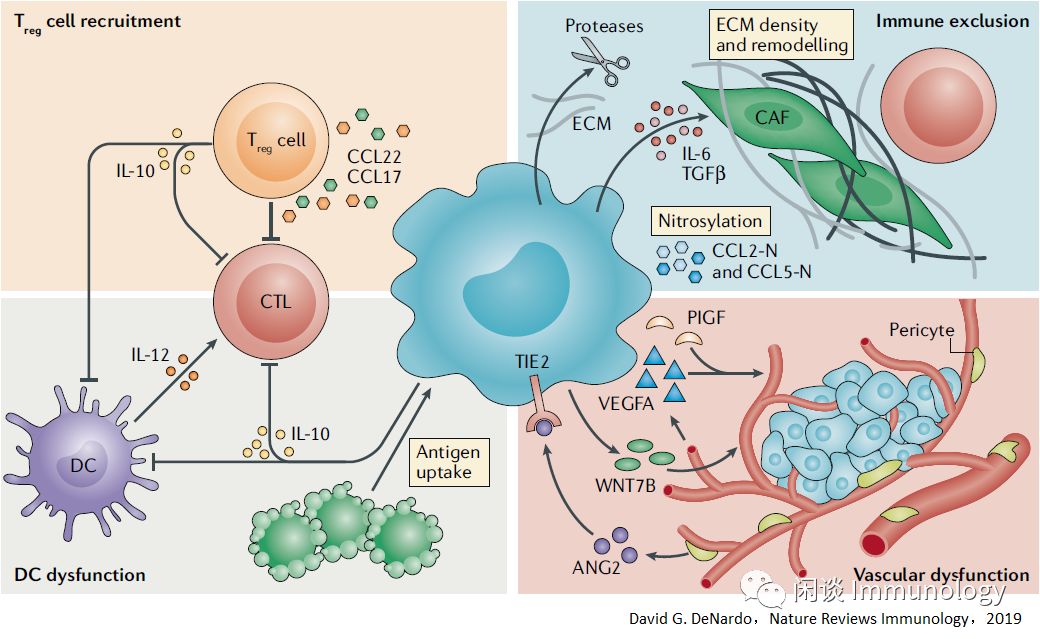
肿瘤相关巨噬细胞(TAM)表型由肿瘤微环境(TME)和肿瘤免疫微环境(TIME)组合驱动。
下图左侧,肿瘤免疫微环境(TIEM)中适应性和先天免疫细胞,提供细胞因子和其它调节因素,调节巨噬细胞表型。
下图右侧,肿瘤微环境(TME)中低氧、纤维化,细胞应力因素调节肿瘤相关巨噬细胞。
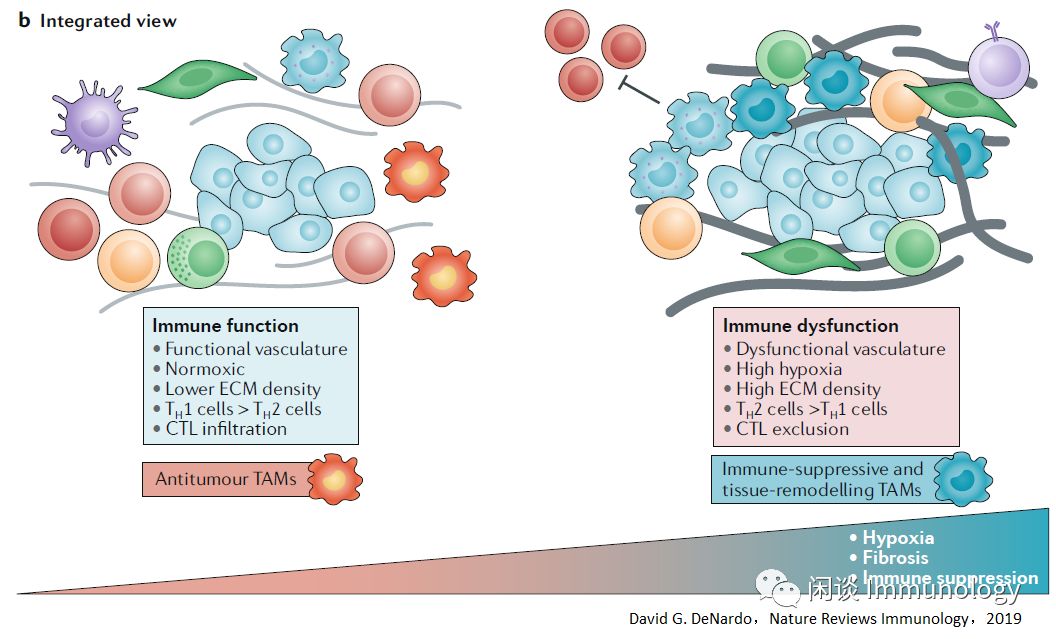
整合因素观点
免疫相关和非免疫相关因素整合在一起,起抗肿瘤免疫,或者引起抗肿瘤免疫功能丧失。
下图左侧:存在强力自适应免疫应答,伴随有限的组织病理学,巨噬细胞被编程为驱动炎症的抗肿瘤TAMs。
下图右侧:肿瘤缺氧,纤维化与大量癌症相关的成纤维细胞(CAFs),免疫抑制细胞浸润集成,以及巨噬细胞被编程以驱动免疫抑制的表型和组织重塑,导致细胞毒性T淋巴细胞(CTL)排除和/或抑制。
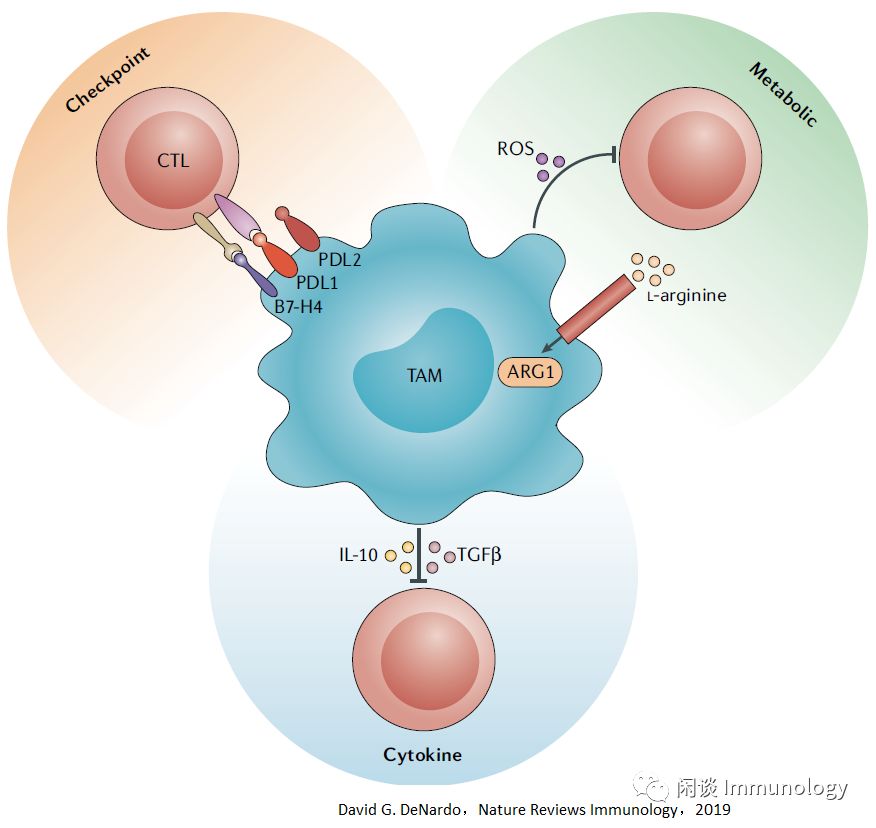
- 肿瘤相关巨噬细胞直接抑制T细胞功能
肿瘤相关巨噬细胞(TAMS)可通过三种不同的机制直接抑制细胞毒性T淋巴细胞(CTL)反应
- 表达PDL- 1等免疫检查点
- 产生抑制性细胞因子,IL-10和转化生长因子-β(TGF-β)
- 改变代谢活性,包括代谢产物耗竭和活性氧(ROS)的产生等
- 肿瘤相关巨噬细胞间接抑制T细胞功能
TAMS还通过控制免疫微环境间接抑制T细胞反应。
- 免疫抑制群体(如调节性T细胞(Treg)细胞)或抑制刺激群体(如树突状细胞(DC))来进行控制。
- TAMS调节血管结构,通过调节细胞外基质(ECM)和趋化因子环境将T细胞排除在瘤内区域来抑制T细胞的吸收。
- 血管功能异常,ANG2,VEGFA等

靶向肿瘤相关巨噬细胞(TAM)

-
靶向TAM招募及存活
消耗TAMs的一种策略是通过减少循环炎性单核细胞来切断它们的补充。
-
CCL2-CCR2抑制剂
循环中的单核细胞高度依赖CCL2-CCR2信号,从骨髓中动员并吸收到炎症部位,因此CCR2的抑制使单核细胞在骨髓中保持,导致循环细胞库的枯竭,原发部位和转移部位TAMs数量的减少。
临床前模型中,CCL2或CCR2阻断可提高化疗、放射治疗和免疫治疗的疗效。因此,几个CCR2阻断联合临床试验正在进行中。胰腺癌的一项早期研究显示,当CCR2抑制剂与FOLFIRINOX方案联合使用时,对化疗的反应性提高了40%以上。虽然CCR2在巨噬细胞的吸收中起着主导作用,但联合疗效的重要考虑因素包括粒细胞的快速补偿和对局部组织寄居TAM群体缺乏影响。还观察到CCL2和/或CCR2的阻断会导致先前被困在骨髓中的单核细胞释放,这已被证明加剧了小鼠乳腺癌模型的转移。在设计未来的临床试验时,这些参数将是至关重要的,可能需要针对这些限制的替代目标来进行持久的反应。
相关药物:
MS-813160 是第一个进入心血管临床开发的双重 CCR2/CCR5 拮抗剂,来自于BMS
一些联合治疗的临床如下表

-
CSF-1-CSFR轴
CSF1-CSF1R轴在临床前模型中也得到了大量的研究。在大多数肿瘤中,CSF1-CSF1R信号的抑制导致大量TAM凋亡死亡,异常值是胶质瘤模型,GM-CSF的代偿活性导致TAM存活和再极化。在大量动物模型中,CSF1R抑制与辐射或化疗药物结合,可改善T细胞反应,而不依赖于其作用机制。此外,CSF1-CSF1R阻断剂提高了多种免疫治疗方式的疗效,包括CD40激动剂、PD1或CTLA-4拮抗剂和过继性T细胞治疗。
一些药物的临床研究见下表:

其他参与巨噬细胞募集的途径包括CXCL12-CXCR4和ANG2-TIE2(NCT03239145a)轴。
在胶质瘤和乳腺癌模型中,放射、化疗和血管破坏已被证明能增加CXCL12的表达,并促进CXCR4依赖的巨噬细胞的重新生长和抵抗。有趣的是,CXCL12似乎是通过优先招募TIE2巨噬细胞来发挥作用的,TIE2巨噬细胞与血管形成密切相关,对肿瘤血管形成很重要。因此,消耗TIE2巨噬细胞可改善血管破坏,中和ANG2可改善对VEGFA阻断的反应,并抑制TIE2阻断化疗诱导的TIE2 TAM在乳腺模型中的吸收,并导致转移减少。虽然TIE2 TAMs对肿瘤免疫的影响和联合免疫治疗的可能性尚不清楚,但ANG2和VEGFA的双重中和促进T细胞浸润,其疗效完全依赖于CD8T细胞。CXCR4的抑制也使胰腺癌模型对检查点阻断更有反应。
-
靶向TAM活化
损耗TAMs的一个内在缺点,是失去了它们作为肿瘤内主要吞噬细胞,和专业抗原提呈细胞的潜在免疫刺激作用。因此,将TAMs重新编程或使其向抗肿瘤表型重新极化,可能是一种更有效、甚至更有毒的方法来增强其他形式的免疫治疗。迄今为止最有效的方法之一是使用一种激动剂CD40抗体,它显示了联合使用gemcitabine+gemcitabine and/or nab-paclitaxel治疗胰腺癌的联合疗效。
由于CD40由cDCs表达,TAM与cDC激活的相对贡献尚不清楚,但关键的是,对PD1和CTLA-4拮抗剂的反应增强已被观察到。
通过抑制组蛋白去乙酰化酶(HDACs),巨噬细胞的表观遗传重组也能诱导T细胞的支持作用。具体来说,在乳腺肿瘤模型中,一种选择性的IIaHDAC抑制剂诱导抗肿瘤巨噬细胞表型,支持T细胞反应,增加对化疗和免疫检查点阻断的反应。Pan-HDAC抑制剂联合PD1拮抗剂进行了试验,巨噬细胞重新编程可能在介导治疗效果方面发挥重要作用。另一种重新编程的方法,涉及到靶向主要的途径来驱动TAMS的免疫抑制功能,包括IL-4、IL-13和免疫球蛋白。然而,尽管这些途径的临床药物存在,但在实体性恶性肿瘤中使用它们来促进免疫的工作却微乎其微。这方面的一个例子是PI3Kγ的靶向(NCT03471351a, NCT02637531a),它被激活在包括FcγR在内的多个通路下游的TAMs中。在肺癌、胰腺癌和黑色素瘤模型中,PI3Kγ信号在巨噬细胞中的激活可驱动TAM免疫抑制活性。在动物模型中,PI3Kγ的药理学抑制导致巨噬细胞重新编程和T细胞应答增强,这既是一种单一的试剂,也可与T细胞检查点阻断联合。
参考文献
David G. DeNardo,Macrophages as regulators of tumour immunity and immunotherapy,Nature Reviews Immunology,2019
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(下)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(上)
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA-I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡-OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频-中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程-中西医结合基础研究中心
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图-OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
中医中药系列
中成药传统方剂交叉检索数据库使用说明(免费开放使用)
关注本号~
加入读者交流群~


本篇文章来源于微信公众号闲谈 Immunology ,作者挑食的喵
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏