导 读
本章主要讨论了在健康人群中存在自身免疫是正常现象,但如果普遍存在耐受性破坏的话就会导致自身免疫性疾病的发生。耐受性的破坏与遗传因素、感染和其他环境因素的相互作用密切相关。
本章中的BOX详细描述了三种自身免疫性疾病——1型糖尿病(T1DM)、乳糜泻以及系统性红斑狼疮(SLE)的自身免疫性和发病机理。本章和第29章至第31章将详细介绍导致几种重要的自身免疫性疾病的不同类型的超敏反应。
部分自身免疫是正常的
自身免疫可以定义为对自身抗原具有特异性的适应性免疫反应,而自身抗体是针对正常细胞成分的抗体,引起反应的这些成分称为自身抗原。大多数健康个体会产生一些自身抗体,但是这些抗体通常水平较低且亲和力不强,需要进行灵敏的检测才能查出。而在一些健康人群中,尤其是女性和老年人中发现了可以通过常规临床测试检测到的较高亲和力的自身抗体。
据估计,免疫球蛋白(Ig)基因重组后,形成的B细胞受体有一半以上对自身抗原具有特异性。B细胞个体发育中的检查点(第14章)阻止大多数B细胞产生自身抗体,自身反应性B细胞也会被抑制或失去功能。在一般情况下,如果没有对同一抗原作出反应的辅助性T细胞(TH)的帮助,大多数自身反应性B细胞无法在外周分泌Ig。
但B1细胞并非如此,它们可以在没有T细胞帮助的情况下分泌Ig(第14章)。B1细胞分泌天然抗体,是健康个体中自身抗体的主要来源。这些B细胞打破了通常适用于其他B细胞的一些规则,不会因抗原暴露而改变其Ig基因,也不会发生体细胞超突变。B1细胞产生的天然抗体永远不会为任何特定抗原而改变自身的适应性。这意味着,尽管天然抗体结合了大量低亲和力的抗原,但它们几乎不会与特定的抗原有较高亲和力结合。
B1细胞分泌的天然抗体具有多种不同的活性(Fig 28.1):
1.天然抗体以低亲和力与多种细菌上存在的抗原结合,这可以激活补体并帮助快速清除入侵细菌。因此,天然抗体的作用就像固有免疫系统的分子一样,它们不依赖基因重组,而是在感染开始之前就存在。
2.天然抗体可与红细胞的A和B抗原发生交叉反应。除非机体遗传了A或B抗原,否则会产生抗A和抗B的IgM,即使机体从未接触过另一个人的红细胞(第29章)。此外,人类还具有针对其他动物物种细胞上表达的糖的天然抗体,这些异种天然抗体将在第34章进一步讨论。
3.天然抗体的低特异性的另一个结果是天然抗体还可以结合一系列正常的细胞成分,例如核蛋白和DNA,这解释了为什么一些健康的人具有抗核抗体。天然抗体的自身抗原结合能力可能是交叉反应的偶然结果,但这些抗体可能具有清除细胞碎片等作用。
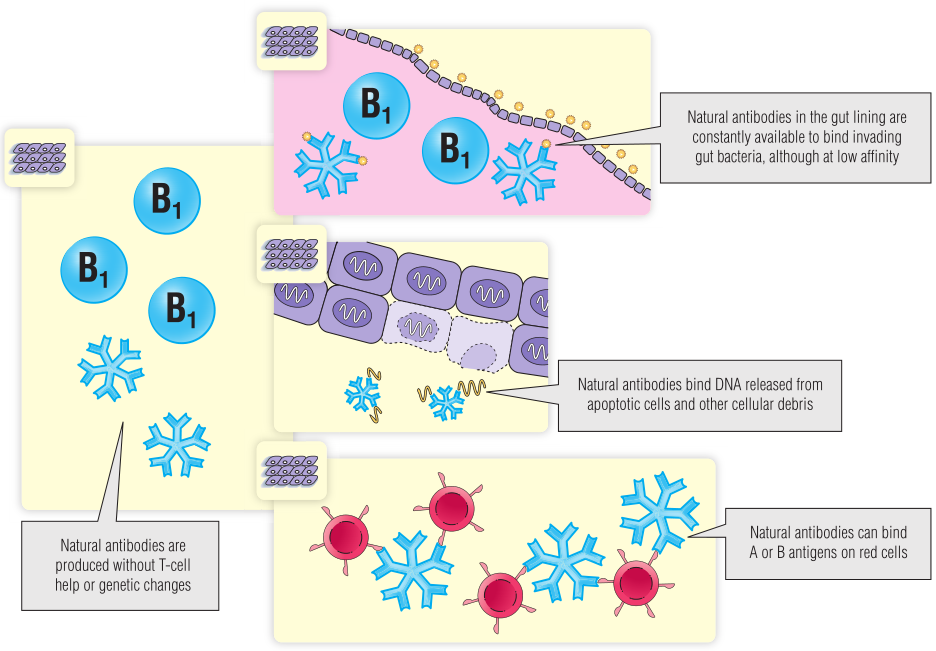
Fig 28.1 天然抗体以低亲和力结合一系列抗原。天然抗体通常是免疫球蛋白M五聚体。
自身免疫性疾病的发生
自身免疫性疾病发生时,自身反应性T细胞或自身抗体通过II至IV型超敏反应引起组织损伤,如第26章所介绍的。与感染性抗原不同,不论免疫系统发挥多大作用,自身抗原都几乎不可能被清除;因此,一旦发生,自身免疫性疾病往往会持续活跃很长一段时间。自身免疫性疾病很常见,往往是持续数月或数年的慢性病,它们可以影响任何器官系统,发生在任何年龄。了解自身免疫性疾病是如何发生的,有助于我们诊断、治疗甚至预防这些问题。
上述天然自身抗体有导致自身免疫性疾病的可能性,同时也有证据表明T细胞可引发以下自身免疫性疾病:
1.即使是由IgG介导的机制(II和III型超敏反应)引起的自身免疫性疾病,也需要T细胞帮助提高亲和力以产生病原性(引起疾病的)抗体。
2.将T细胞从患有自身免疫性疾病的动物转移到健康的动物身上时,健康个体也会患病。
3.自身免疫性疾病通常与特定的主要组织相容性复合体(MHC)基因有关,MHC基因可调节T细胞,但不调节B细胞。
目前尚无证据表明分泌无害天然抗体的B1细胞能产生高亲和力的特异性抗体(这种抗体可以在没有T细胞帮助的情况下导致自身免疫性疾病)。
要让T细胞介导自身免疫性疾病,它们需要克服耐受机制。在介绍T细胞如何做到这一点之前,先简要讲解T细胞对自身抗原的耐受性。
T细胞耐受
耐受可阻止免疫系统对特定抗原作出反应,第18章对此进行了介绍。中枢和外周耐受期间的检查点经过进化,可以阻止T细胞介导自身免疫。T细胞最初对胸腺中的自身抗原具有耐受性,这是中枢耐受性。胸腺中任何与自身肽高亲和力结合的T细胞都将通过阴性选择被清除,这一过程被称为中枢免疫耐受。
但是,不可能所有肽都在胸腺中表达,因此一些自身反应性T细胞可能会从阴性选择中逃逸。来自遥远而复杂的器官(如大脑)的每一种肽不可能都在胸腺中表达,因此一些大脑特有的T细胞可能会到达外周。对于已经逃逸到外周的潜在的自身反应性T细胞,正常情况下,至少还有三个机制可以阻止其激活(Fig 28.2)。
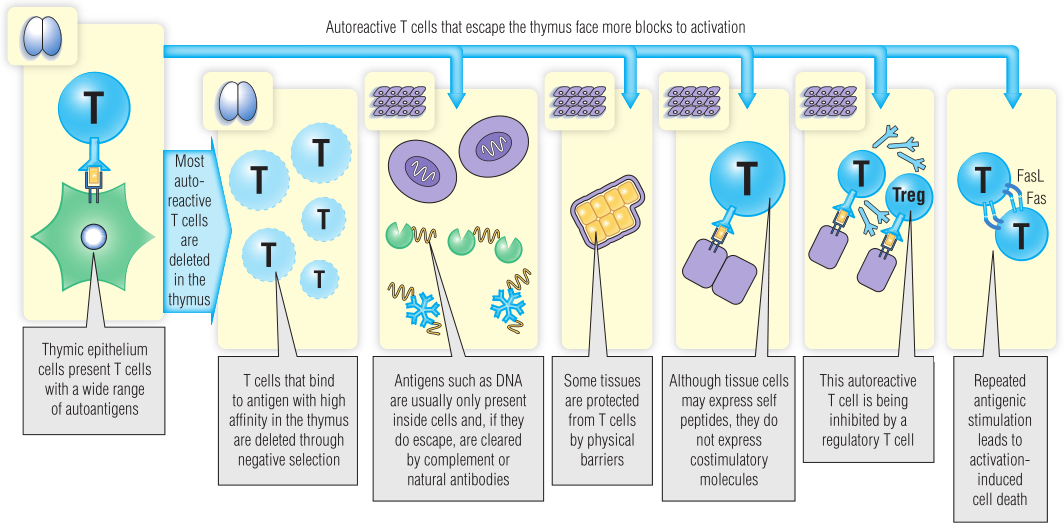
Fig 28.2 T细胞耐受性。大多数高亲和力识别自身抗原的T细胞在胸腺中发生凋亡。在外周耐受过程中还存在几个额外的检查点:抗原的隔离,缺乏共刺激调节性T细胞,以及激活诱导的细胞死亡。这些检查点阻止T细胞与外周自身抗原发生反应。
防止自身反应性T细胞被激活的第一种方法是隔离(隐藏)自身抗原。有些分子,如DNA,通常被隐藏在健康细胞内。如果它们从细胞中渗出,比如细胞凋亡时,它们会被补体或天然抗体迅速清除。
在正常情况下,如果自身反应性T细胞被锁定在免疫赦免区,它可能永远不会遇到特定的抗原。免疫赦免可以通过物理屏障来阻止淋巴细胞或抗体进入。例如,血脑屏障使大脑成为免疫系统的“禁区”。或者,可能有一些分子装置可以阻止某些组织的免疫监视;睾丸细胞表达Fas,它可以诱导任何设法进入睾丸的T细胞凋亡。
其他自身反应性T细胞可能会进入表达特定抗原的组织,但外周耐受通常会阻止这些T细胞做出反应。组织细胞表达MHC-I类基因,也可以被诱导表达MHC-II类基因。然而,胸腺产生的自身反应性T细胞也需要CD80(B7)或CD40等共刺激分子的刺激才能真正激活。当初始T细胞识别非专职抗原提呈细胞(APC)上的抗原时,由于缺乏共刺激信号它们会发生凋亡或功能减弱,而不是被激活,无功能的细胞仍然存活,但不会对抗原作出应答。
逃逸到外周的自身反应性T细胞也可以通过调节性T细胞(Tregs)来阻止反应,Tregs似乎对与其识别相同的抗原的T细胞具有特异性抑制。它们通过多种机制抑制效应T细胞,包括分泌抑制细胞因子,如IL-10和TGF-β。最后,活化诱导的细胞凋亡(AICD)发生在反复暴露于同一抗原(通常是自身抗原)的T细胞中。这些T细胞开始同时表达Fas和Fas配体(FasL),自杀或被邻近细胞杀死。
T细胞耐受性的破坏
自身免疫性疾病往往在家族中传播。具有相同的自身免疫遗传倾向的个体(例如同卵双胞胎)并不总是患上同样的自身免疫性疾病,如果他们患上了自身免疫性疾病,他们可能会在不同的时间发生。这表明,自身免疫性疾病的发生既受遗传因素影响,也受环境因素干扰。至于过敏,很可能需要几个环境触发因素按顺序诱发才能发展成疾病。这种复杂性就解释了为什么很难阐明自身免疫性疾病的发病机制(Fig 28.3)。如第35章所述,产生恶性肿瘤需要类似的“多发”机制,即遗传因素和环境因素的组合。
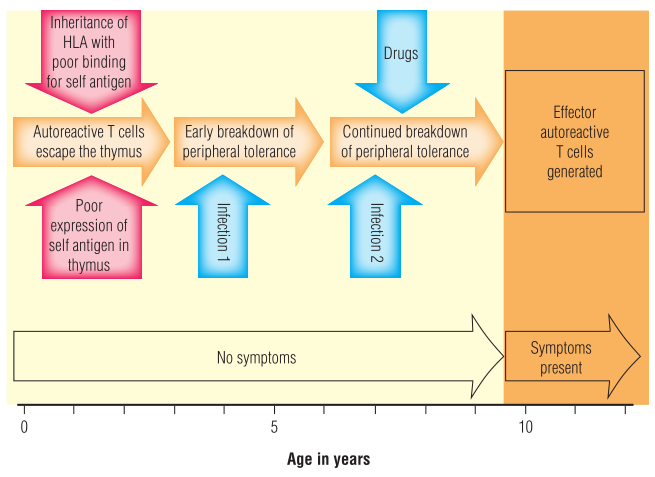
Fig 28.3 启动自身免疫过程可能需要一系列不同的因素
遗传因素与耐受性丧失
一些罕见的遗传病会引起自身免疫。例如,在自身免疫性多内分泌疾病念珠菌病外胚层营养不良症(APECED)(第15章)中,AIRE基因发生突变,不能产生中枢免疫耐受。APECED患者通常会同时经历几种自身免疫性疾病。然而,大多数自身免疫性疾病相对常见,不能用罕见的突变来解释。例如,根据研究人群的不同,Ⅰ型糖尿病和乳糜泻分别影响约1:300和1:100的人。这意味着导致这些疾病的免疫耐受破坏与常见的多态性有关,而不是罕见的突变。
一些遗传多态性影响肽在胸腺中的表达方式。例如,胰岛素在正常胸腺中表达,在胸腺中通过阴性选择耐受性T细胞。胸腺中胰岛素的表达水平是由基因决定的,一些个体表达了胰岛素基因,但其转录水平低于正常水平,因此在胸腺中表达的胰岛素较少,则胰岛素反应性T细胞被清除的可能性较小(Fig 28.4)。此外,某些向T细胞呈递肽效率较低的MHC等位基因的表达可能会增加获得包括Ⅰ型糖尿病在内的自身免疫性疾病的风险。
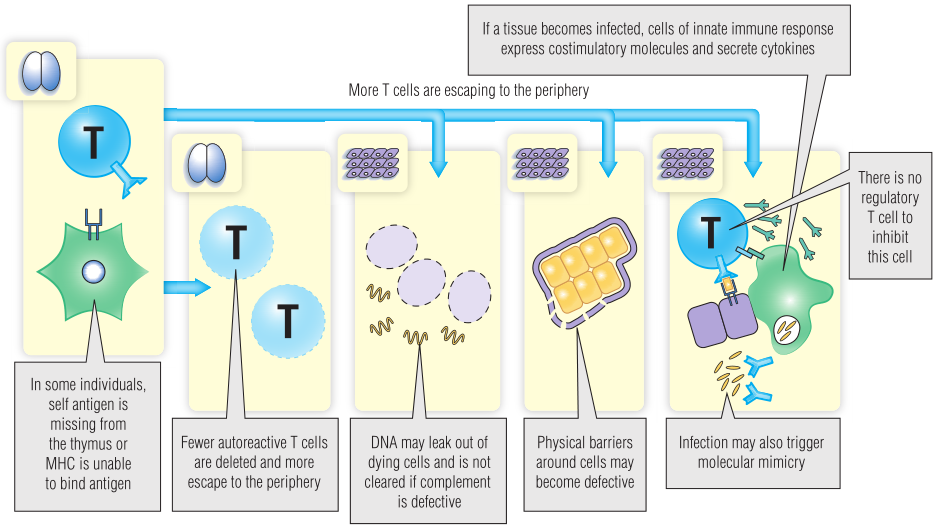
Fig 28.4 T细胞的耐受性是如何被打破的
基因多态性也可能影响外周免疫耐受。例如,隐藏的抗原可能会暴露于免疫系统中,例如通过甘露聚糖结合凝集素(MBL)和补体成分C1之类的分子除去由凋亡细胞释放的DNA。如果无法通过这些机制去除DNA,则可能会引发免疫反应,这可能是SLE发展的第一步(见BOX 28.3)。
环境因素与免疫耐受破坏
在某些个体中,环境因素(例如接触药物和紫外线)(参见BOX 28.3)会触发自身免疫,感染是破坏耐受性更常见的环境因素。
如果组织细胞获得呈递自身多肽的能力,则外周免疫耐受可能会被破坏。APC(例如单核细胞和巨噬细胞)募集到感染部位时,可能会发生这种情况。这些细胞表达共刺激分子和细胞因子,使初始T细胞能够对组织细胞表达的多肽做出应答。在这种情况下,针对感染的适当炎症反应会发生蔓延,引发对自身抗原的反应。
外周免疫耐受破坏的另一种可能的机制是,感染引起的免疫反应引发抗体或T细胞与宿主组织交叉反应,这称为分子拟态。这方面的一个例子是急性风湿热(感染β溶血性链球菌后有一定几率发生这种情况)。患者会出现一系列复杂的症状,包括皮疹以及心脏和神经系统受累。在这些个体中,链球菌感染诱导抗体与心脏组织发生交叉反应,并触发II型超敏反应。在这种情况下,链球菌抗原模拟心脏抗原。该感染能够对阻止自身反应性抗体产生的耐受机制进行抑制,因为链球菌通过其模式识别分子激活了先天免疫反应。风湿热是一种短暂的疾病,不会引起大多数自身免疫性疾病的典型慢性病。相似的细菌可以通过不同的机制引起链球菌病后肾小球肾炎(第26章)。
少数其他罕见的感染可通过分子拟态引起短暂的自身免疫性疾病,但它们都不会超过几周。目前的观点是感染有时可能通过分子拟态引起自身免疫性疾病,但维持其状态还需要其他遗传和环境因素。
最后,在关键时刻,没有感染也有可能触发自身免疫。如果将特定品系的小鼠保持在无微生物条件下,它将会患上Ⅰ型糖尿病。然而,如果这些小鼠暴露在日常微生物中,它们就不会患糖尿病。这一观察结果产生了这样一种观点,即减少与微生物的接触可能是发达国家自身免疫性疾病患病率上升的原因。在第27章中讨论了与过敏有关的问题。到目前为止,在人类身上,还未能鉴定出一种降低患自身免疫性疾病风险的微生物。Table 28.1总结了一些已知的引发自身免疫性疾病的遗传和环境因素。
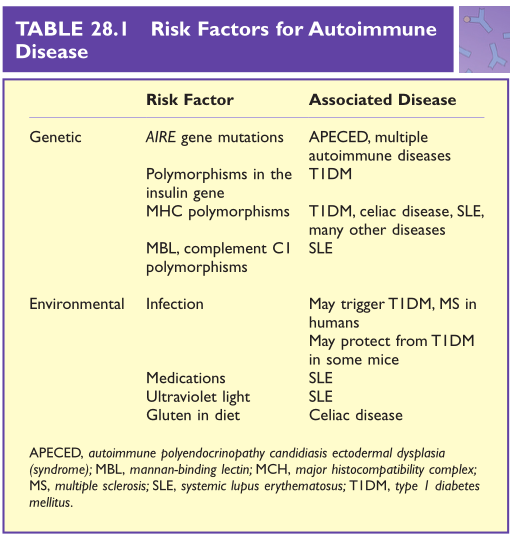
Table 28.1 自身免疫性疾病的危险因素
自身免疫性疾病检测
自身免疫性疾病的检测依赖于自身抗体的检测。第5章介绍了抗体特异性检测的两种主要类型。第一种是直接免疫荧光,用来寻找组织中自身免疫过程的证据。这仅在可接触的组织中是可行的,如BOX 28.3中描述的示例中的皮肤。Fig 28.5简要回顾了直接免疫荧光技术。
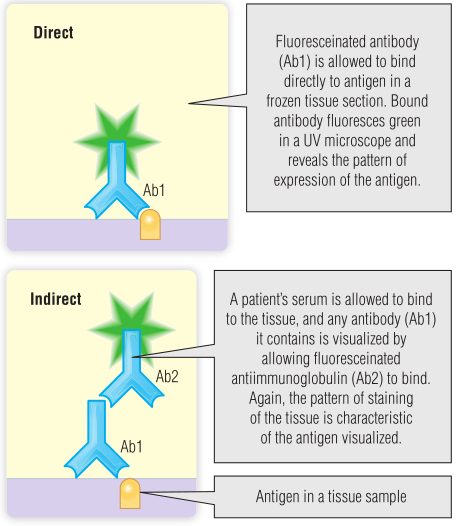
Fig 28.5 直接免疫荧光和间接免疫荧光的原理
大多数情况下,检测血液样本中的自身抗体要简单得多。最初的自身抗体血检是间接免疫荧光法。在这种情况下,抗原是在载玻片上的细胞或组织。检测系统是与荧光标签结合的抗人 IgG,在紫外(UV)显微镜下检测(见Fig 28.5B)。在BOX 28.1至28.3中,胰岛细胞和肌内膜抗体以及抗核细胞质抗体(ANCA)用于介绍间接免疫荧光。较新的检测方法是将抗原固定在固体表面,如第5章所述的酶联免疫吸附试验(ELISA)。血样中的抗体是通过与酶结合的抗人IgG抗体来检测的,这种酶能够产生颜色变化或荧光,颜色或荧光量与样本中存在的自身抗体水平成正比。ELISA的优点是可以提纯抗原(原则上可以提供更具体的结果),对较低水平的抗体具有更高的敏感性,并且可以对抗体水平进行量化。
虽然自身抗体可以帮助诊断自身免疫性疾病,但必须了解一个重要的陷阱。正如前面所解释的,在完全健康的个体中可以发现一些低水平的自身抗体。例如,在系统性红斑狼疮患者中发现的抗核抗体水平较高,而在许多正常人,特别是女性中,也可以发现水平较低的抗核抗体,而且随着年龄的增长,抗核抗体的出现频率更高。其他个体在感染后也可能会产生短暂的自身抗体,这可能是免疫系统的非特异性激活所致。这些假阳性结果导致其中一些测试的特异性较低。
BOX 28.1 1型糖尿病
一名9岁的男孩在学校状态不太好,且饮水量大。他的母亲很担心,因为他的姐姐在4年前8岁时出现了同样的症状,后来被诊断出患有1型糖尿病(T1DM)。
这名男孩的空腹血糖中度升高,但在他的尿液中没有发现酮类物质,这些发现不能诊断为糖尿病。他的血清通过间接免疫荧光检测自身抗体,显示含有胰岛细胞抗体(Fig 28.6),表明可能为T1DM。他开始服用胰岛素,5年后,没有发生糖尿病并发症。
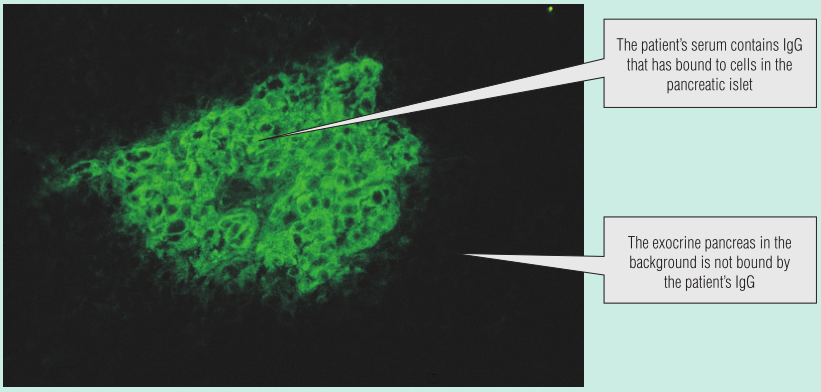
Fig 28.6 间接免疫荧光法检测胰岛β细胞抗体。动物胰腺的一部分被放在切片上。病人的血清孵育切片。病人的免疫球蛋白(Ig)没有与组织结合的,会被洗掉。病人的IgG与组织结合的,用荧光染料标记的抗人IgG的二抗进行检测。
对于尿中有高血糖和酮体的个体,T1DM中的胰岛细胞抗体通常不是诊断所必需的。胰岛细胞抗体的存在一般用于对特征不太明确的患者的诊断,就像这个病例一样。患有T1DM时,胰岛β细胞被T细胞损伤,胰岛细胞抗体是这一过程的标志,其在诱导胰岛细胞损伤方面没有任何作用。
T1DM是IV型超敏反应的一个例子。T细胞侵入胰岛,特异性地破坏分泌胰岛素的β细胞。一旦自身反应性T细胞进入胰岛,β细胞就会在几周内被破坏。而一旦β细胞被破坏,再生的机会微乎其微,患者必须开始终身使用胰岛素替代。
如果一对同卵双胞胎中的一个患上T1DM,另一个有50%的几率也会患上,这就是所谓的符合率。最重要的遗传因素是人类白细胞抗原(HLA)型,它提供了大约90%的遗传风险。在白人中,T1DM经常发生在遗传HLA等位基因DQ2的人中。在大多数人类白细胞抗原-DQ等位基因中,β链的57位被天冬氨酸残基占据。而在HLA-DQ2中,这个位置被另一个氨基酸残基取代。Fig 28.7展示了人类白细胞抗原-DQ2的β链上的这种单一氨基酸残基的变化对于发生T1DM的风险有何影响:57位的非天冬氨酸残基阻止自体肽落在凹槽中,因此自体肽不能被提呈,所以胸腺中不能清除针对自体肽的特异性T细胞。
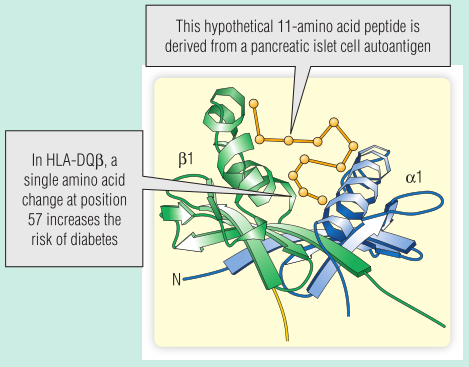
Fig 28.7 目前的观点是人类白细胞抗原DQ2减少了与胰岛细胞抗原的结合。因此,识别胰岛细胞抗原的T细胞不能在胸腺中被清除,发生自身免疫的可能性增加。
其他几种基因多态性也会影响患糖尿病的风险。例如,胰岛素基因附近的多态性会影响胸腺中胰岛素的表达。遗传导致胸腺胰岛素分泌水平降低的多态基因的人患糖尿病的风险增加。这可能是因为低表达使得胰岛素反应性T细胞能够到达外周。
即使是同卵双胞胎,其中一个患有糖尿病且另一个也患的风险仅有50%,因此环境因素肯定有着重要作用。一个可能的环境因素是感染。从理论上讲,不同时间的不同感染可能会增加或降低患T1DM的风险。例如,病毒感染可能会导致胰岛的轻度炎症。炎症信号吸引先天免疫系统细胞,这些细胞表达共刺激分子并分泌细胞因子,这使得组织抗原可以被提呈给自身反应性T细胞。然而,虽然1型糖尿病是一种常见的自身免疫性疾病,但还没有发现某种单一的感染会稳定触发这类疾病。目前,大多数数据认为肠道病毒是可能的触发因素,特别是一种被称为柯萨奇病毒的特殊类型的肠道病毒。
此外,在发达国家儿童感染率下降之际,1型糖尿病的患病率正以每年约3%的速度增长。这导致一些研究人员提出,可能在特定年龄没有感染是触发T1DM的原因。有证据表明,当某些品系的小鼠不接触微生物时,糖尿病在这些品系中很常见,这支持了这种想法。这类似于提出的卫生学假说,用来解释遗传易感性个体过敏症患病率增加的原因(第27章)。这可能是在过于“卫生”的环境下,调节性T细胞不产生,不能阻止自身反应性T细胞破坏胰岛β细胞。
Fig 28.8说明了关于T1DM发病机制的一些观点。在这类模型中,感染的确切时间可能比是否发生感染更重要。
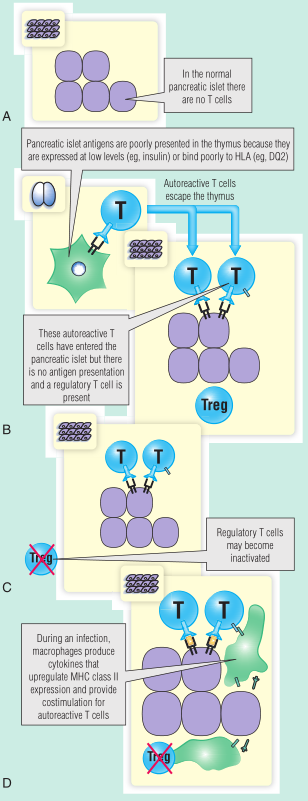
Fig 28.8 胰岛素依赖型糖尿病的发病机制。A,正常胰岛不存在自身反应性T细胞。B,允许自身反应性T细胞逃离胸腺的遗传因素是众所周知的。C,调节性T细胞在1型糖尿病中的确切意义尚不清楚。D,感染在增加主要组织相容性(MHC)的表达中起作用。HLA,人类白细胞抗原;T-reg,T-调节细胞。
1型糖尿病很常见。关于如何预防T1DM,目前正在进行大量研究。当一个家庭有一个受影响的儿童时,可以定期对其他兄弟姐妹进行胰岛细胞抗体筛查。在出现胰岛细胞抗体的儿童中,使用免疫抑制剂如环孢素(第11章)可以将糖尿病的发病延迟长达一年。这些药物通过抑制T细胞发挥作用,但在停药后不久(它们毒性太大,不能长时间使用)疾病就会显现出来。其他方法也试图诱导对胰岛β细胞的耐受,但到目前为止,这些方法都被证明是无效的。如果明确哪些感染(如果有的话)会触发T1DM,疫苗策略可能会有所帮助。
BOX 28.2 乳糜泻
BOX 28.1中讨论的糖尿病患者的妹妹出现腹泻和体重下降,她表现出轻度吸收不良。她的血清通过间接免疫荧光检测,发现含有抗内膜肌的免疫球蛋白A(IgA)自身抗体(Fig 28.9)。酶联免疫吸附试验(ELISA)检测到抗组织转谷氨酰胺酶(TTG)抗体。根据这些血液测试结果,结合这个年龄段的儿童常见病,她被诊断为乳糜泻。患者开始进行无麸质饮食,她的症状显著改善,6个月后内膜抗体不再存在。
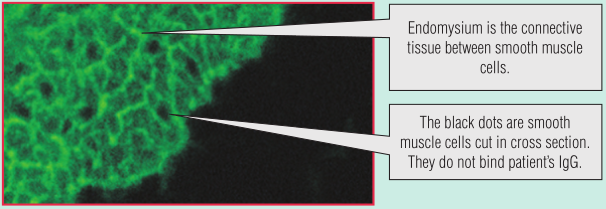
Fig 28.9 乳糜泻患者有抗内膜的自身抗体,内膜是围绕平滑肌纤维束的结缔组织
乳糜泻是发达国家小肠疾病最常见的原因,可引起从轻度贫血到严重营养不良的一系列临床问题。乳糜泻是一种自身免疫性疾病,淋巴细胞和巨噬细胞浸润空肠。因此,它是一种针对外源性抗原、一种称为醇溶蛋白的多肽和一种自身抗原tTG的IV型迟发性超敏反应。
小麦、黑麦和大麦含有一种叫做麸质的蛋白质,而麸质又含有醇溶蛋白。当从饮食中去除醇溶蛋白时,乳糜泻的症状和空肠组织就会改善。
tTG是一种将氨基酸谷氨酰胺转化为谷氨酸的酶。它能不可逆地与底物多肽结合。肌内膜抗体(见Fig 28.9)是检测tTG抗体的间接方法。
同卵双胞胎对乳糜泻的符合率很高(75%)。大多数患者都遗传了人类白细胞抗原(HLA)DQ2等位基因。在乳糜泻中,空肠T细胞识别与HLA-DQ2结合的醇溶蛋白多肽(Fig 28.10)。然而,HLA-DQ2上肽结合槽一侧的口袋只与带电氨基酸结合;除非谷氨酰胺残基被tTG转化为谷氨酸,否则醇溶蛋白不会结合。由于与醇溶蛋白结合,tTG本身成为自身抗体的靶标(Fig 28.11)。
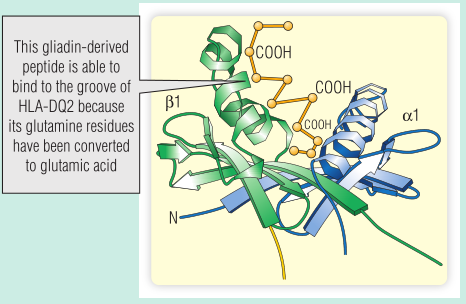
Fig 28.10 与人类白细胞抗原(HLA)DQ2结合的醇溶蛋白肽
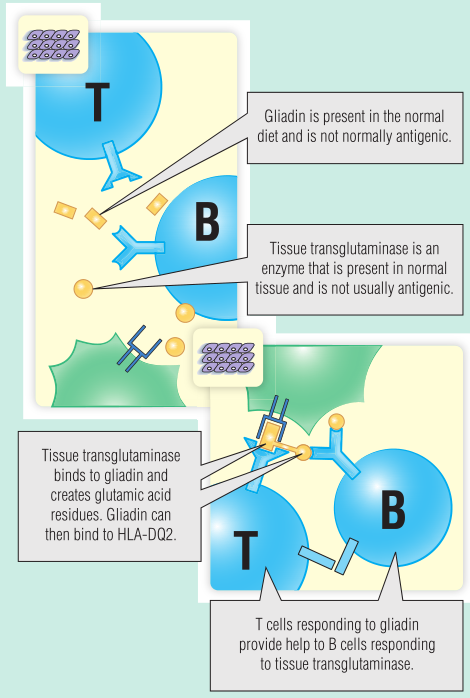
Fig 28.11乳糜泻的发病机制
在平滑肌细胞之间的结缔组织肌内膜中,tTG含量很高。间接免疫荧光法检测子宫内膜抗体与ELISA法检测tTG一样适用于乳糜泻的检测。
同一个家庭的成员通常会都患上1型糖尿病(T1DM)和乳糜泻。家庭成员患自身免疫性甲状腺或肾上腺疾病或胃炎的风险也可能更高。这些疾病经常在同一个体中共存,被称为器官特异性自身免疫性疾病。
人类白细胞抗原(HLA)基因都紧密地位于第6号染色体上,它们往往是一起遗传的,称为单倍型(第8章)。一种相对常见的单倍型由HLA等位基因B8、DR3和DQ2组成。正是这种单倍型的遗传解释了为什么器官特异性自身免疫性疾病在家族中发生。HLA-DQ2等位基因增加了T1DM和乳糜泻的风险。目前还不清楚主要组织相容性复合体(MHC)中的哪些基因与其他器官特异性自身免疫性疾病相关,许多基因可能是候选基因(见Table 8.2)。不同的家庭成员往往患有不同的自身免疫性疾病,这可能是因为引发每种疾病的环境因素略有不同。
BOX 28.3 系统性红斑狼疮
一名年轻女子的脸部出现皮疹(Fig 28.12A)。脚趾也出现了损伤,引起疼痛(Fig 28.12B)。皮肤活检用于直接免疫荧光,提示皮肤含有免疫球蛋白G(IgG)和补体的沉淀物(Fig 28.13)。血液检测也有一些异常,包括通过间接免疫荧光(Fig 28.14)进行的抗核细胞质抗体(ANCA)筛查和抗DNA抗体检测(通过酶联免疫吸附试验[ELISA])。这些发现表明她很可能患有系统性红斑狼疮(SLE)。请注意,在血液样本中发现的DNA抗体并不与体内的细胞核结合。这是因为这些IgG抗体已经与细胞释放的DNA形成了免疫复合物。(此案例将在第29章中继续。)
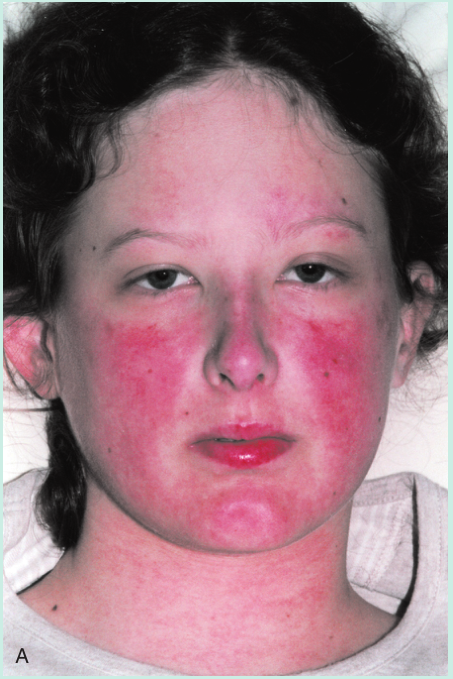
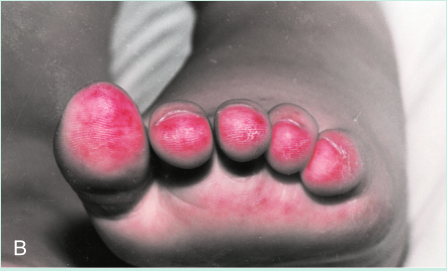
Fig 28.12 A 这名妇女有典型的系统性红斑狼疮面部皮疹。B, 她脚趾上的损伤反映了潜在的血管炎症。
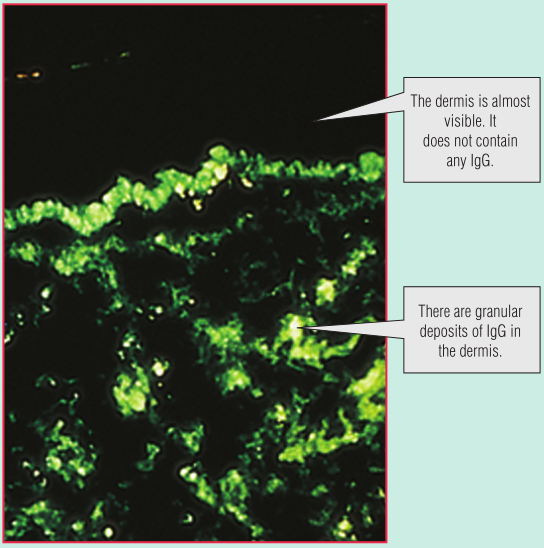
Fig 28.13 新鲜皮肤活检切片与带有荧光标记的抗人免疫球蛋白G(IgG)孵育。当在紫外光显微镜下观察时,组织中的IgG会产生绿色荧光。这些是如何形成的将在第30章讨论。
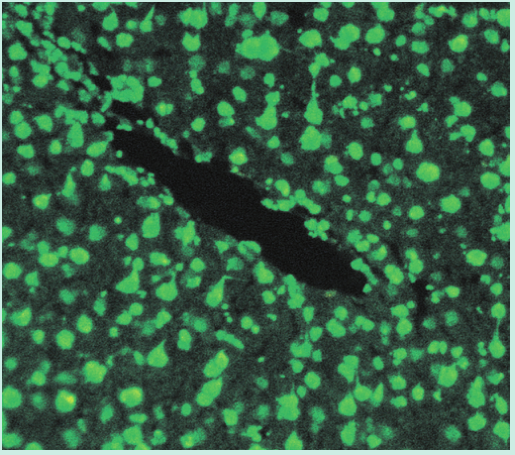
Fig 28.14 间接免疫荧光法检测抗核抗体。一块动物组织被固定在玻片上,病人的免疫球蛋白G与组织中的细胞核结合。
系统性红斑狼疮是一种由免疫复合物介导的自身免疫性疾病,也就是说,它是一种III型超敏反应。系统性红斑狼疮的超敏反应是由针对DNA和其他核成分的抗体介导的,如核糖核蛋白。
关于系统性红斑狼疮如何致病的详细描述见第29章。这一章关注的是如何产生高水平的抗DNA和核糖核蛋白抗体。虽然SLE是一种抗体介导的疾病,但其发病机制中的关键一步是T细胞对DNA的耐受性丧失。
基因在SLE的发病机制中起着重要作用,同卵双生子SLE的符合率约为60%。系统性红斑狼疮在遗传人类白细胞抗原(HLA)等位基因DR2的个体中更为常见。此外,碎片清除蛋白基因的多态性也很重要。
先天免疫系统的一些蛋白质参与清除细胞碎片。例如,甘露聚糖结合凝集素(MBL)和补体成分C1q可以识别和结合细胞死亡期间释放的DNA片段(Fig 28.15)。这被认为是在中性粒细胞形成细胞外陷阱(Net)时发生的。然后,这些碎片被清除,可能是通过吞噬作用。C1q或MBL水平低的患者患SLE的风险更高,可能是因为细胞死亡产生的DNA能够触发抗DNA抗体的产生。一些药物还通过抑制甲基转移酶来干扰DNA的清除。在易患人群中,这些药物可以引发抗DNA抗体的产生。肼苯哒嗪和普鲁卡因胺是两种可能通过这种机制诱发系统性红斑狼疮的药物。
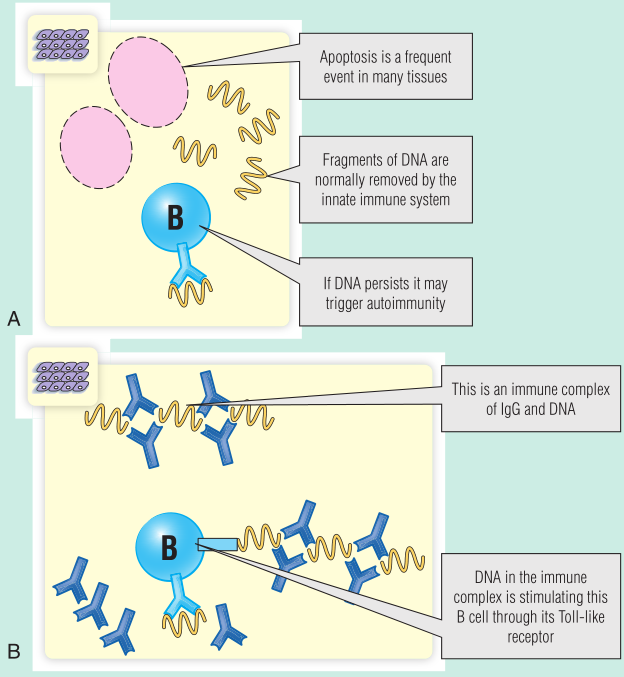
Fig 28.15 A. DNA清除受损最初可能启动抗DNA抗体的产生。B. 然后,含有DNA的免疫复合物可能会刺激Toll样受体,使抗体持续分泌。
Toll样受体(TLR)9表达于B细胞和DC上,通过结合未甲基化的胞嘧啶和鸟嘌呤(CpG)基序,具有识别细菌的生理功能。正常情况下,识别细菌CpG DNA基序会导致B细胞分泌免疫球蛋白或树突状细胞分泌干扰素(IFN)增加。在SLE患者中,含有DNA的免疫复合物能够刺激TLR-9。这会导致1型干扰素的分泌增加,并可能为B细胞提供额外的刺激,以维持抗DNA抗体的分泌(见Fig 28.15)。感染可能通过增加细胞凋亡和触发1型干扰素的额外分泌来促进这一过程。
另外两个因素也会影响系统性红斑狼疮的发生。一般来说,自身免疫性疾病在女性中更常见;而系统性红斑狼疮就是一个极端的例子,女性发生的频率是男性的20倍。女性较高的自身免疫率可能与性激素雌激素水平较高有关。系统性红斑狼疮有时会在服用含有雌激素的避孕药后不久发生,在雌激素水平较高的怀孕期间往往会变得更糟。雌激素具有增加抗体产生的生理作用,因此可能会增加自身抗体的分泌。一些自身免疫性疾病(如1型糖尿病)对男性和女性的影响是一样的。这些自身免疫性疾病往往是由T细胞而不是抗体引起的。
暴露在紫外线(UV)下会引发系统性红斑狼疮(SLE),暴露在阳光下的皮肤通常会受到特征性皮疹的影响。目前还不清楚紫外线是如何产生这些影响的。一种可能是它诱导皮肤细胞凋亡。另一种是紫外线诱导的皮肤损伤触发促炎细胞因子的释放,如肿瘤坏死因子(TNF)或1型干扰素(IFN),它们要么协同刺激B细胞,要么增加局部组织损伤。Fig 28.16说明触发SLE可能需要的一系列因素。
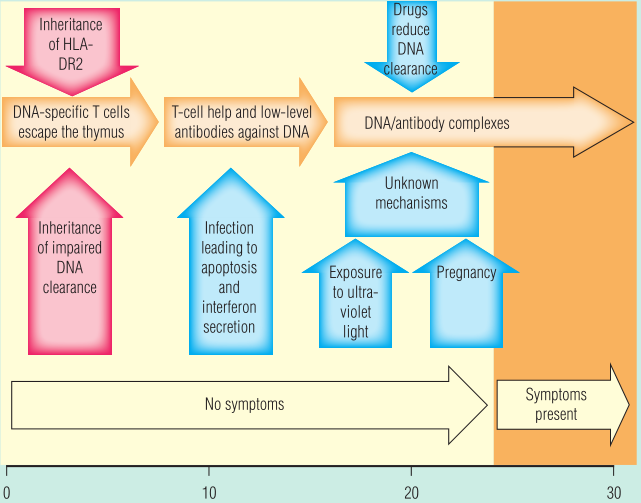
Fig 28.16 触发系统性红斑狼疮需要多种因素。
在许多健康的个体中,ANCA的水平都很低。已知ANCA水平可在SLE症状出现前几年升高。此外,针对双链DNA的特异性抗体也会开始产生。目前,将患者从无症状的SLE转变为有症状的SLE的因素还没有完全研究清楚,但可能包括感染、暴露于紫外线和雌激素等。
— THE END —
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
肿瘤免疫学-第6章:调节性T细胞的作用、作用机制以及对癌症的影响(下)
肿瘤免疫学-第6章:调节性T细胞的作用、作用机制以及对癌症的影响(上)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(下)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(上)
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA-I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡-OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频-中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程-中西医结合基础研究中心
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图-OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
中医中药系列

关注本号~

加入读者交流群~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏