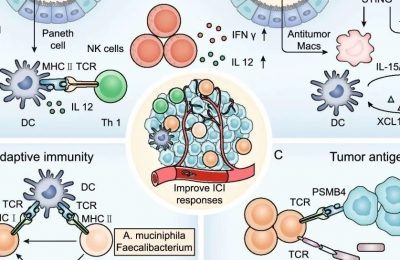
34.1 细胞因子在黑色素瘤中的作用
34.1.1 α-干扰素 (IFN-α)
干扰素-α是美国食品药品监督管理局(FDA)批准的首个用于治疗黑色素瘤的细胞因子。虽然对于晚期黑色素瘤来说,干扰素-α的效果有限,随机对照试验显示,对于这一阶段的患者,即使增加化疗也未能显著提高生存率。1996年,干扰素-α被批准作为IIIB-III期高风险黑色素瘤术后的辅助治疗。在后续的辅助免疫治疗章节中,将进一步讨论干扰素-α的使用细节。
34.1.2 白介素-2 (IL-2)
Rosenberg及其团队在白细胞介素-2(IL-2)的应用研究中取得了开创性成果。他们首先探索了IL-2单独使用,随后与淋巴因子激活的杀伤细胞(LAK)及肿瘤浸润淋巴细胞(TIL)的组合使用。这些研究最终证实了IL-2在治疗晚期黑色素瘤中的有效性,1998年,IL-2因此被批准为治疗晚期黑色素瘤的首个免疫疗法。Rosenberg及其团队还开展了一系列采用过继细胞疗法(ACT)的癌症治疗项目,尤其是针对黑色素瘤,多年的研究在理论和实践上取得了显著进展。在特定患者群体中,结合化疗清除淋巴细胞,有时配合全身照射,随后进行肿瘤来源的T细胞克隆及IL-2治疗,可以达到50-70%的缓解率,其中完全缓解(CR)率为10-20%。目前,使用基因工程改造的自体细胞表达T细胞受体是一个有希望的方法,但这些技术仍主要限于少数专业中心进行。
34.1.3 肿瘤坏死因子-α (TNF-α)
由于剂量相关的毒性,尤其是低血压的问题,全身性应用肿瘤坏死因子-α(TNF-α)的治疗发展受到限制,低剂量时效果不佳。然而,在孤立肢体灌注(ILP)技术中,可以在局部达到有效浓度,显示出较好的治疗效果。在此技术应用下,与melphalan(一种化疗药物)联用,可在多发性转移性黑色素瘤患者中产生显著的协同效应。1998年,针对危及肢体的软组织肉瘤,肿瘤坏死因子-α获得欧洲药品管理局(EMA)的批准,主要用于治疗软组织肉瘤和黑色素瘤的多发性转移。目前全球约有50个专业中心运行肢体保留治疗项目,取得了良好的长期成效。
34.1.4 使用免疫检查点抑制剂打破耐受性
目前,黑色素瘤治疗的重大进展主要集中在免疫治疗和突变驱动的药物开发上。克服肿瘤耐药性是治疗黑色素瘤的一大突破,我们已进入一个新时代,由于首批免疫检查点抑制剂——抗CTLA-4(细胞毒性T淋巴细胞抗原-4)和抗PD-1/抗PD-L1(程序性死亡-1及其配体)的使用,这些治疗方式的效果前所未有。短短五年内,晚期黑色素瘤从一种几乎无法治愈的疾病转变为有望治愈的疾病,我们正在开始认识到这些治疗在整个实体瘤领域的潜在影响(Table 34.1)
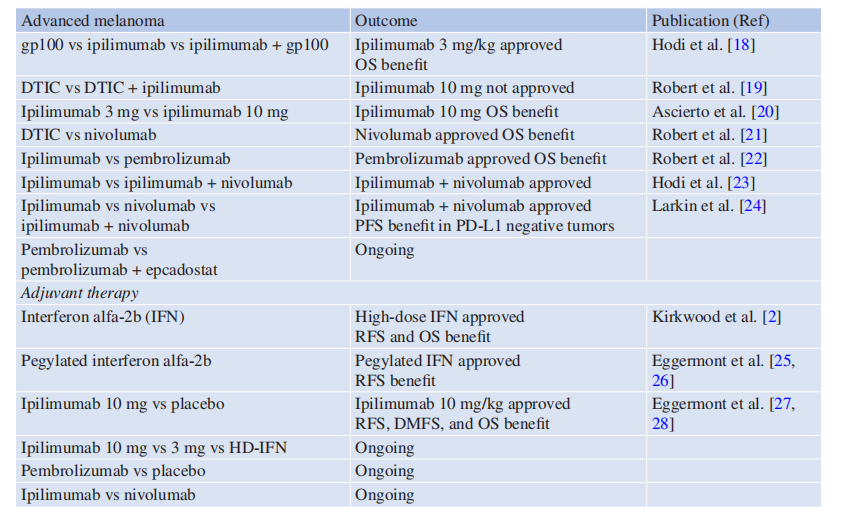
Table 34.1 干扰素、伊匹单抗、纳武单抗和派姆单抗的关键III期免疫治疗试验
34.2 抗CTLA-4治疗
34.2.1 晚期黑色素瘤患者的治疗效果
阻断细胞毒性T淋巴细胞抗原-4 (CTLA-4)的单克隆抗体可以打破免疫耐受,促进肿瘤缩小。全人源化的单克隆抗CTLA-4抗体,伊匹单抗(ipilimumab),于2011年在美国被批准用于晚期黑色素瘤患者的一线和二线治疗。根据随机对照试验(RCT)的结果,伊匹单抗在欧洲被批准用于二线治疗,剂量为3 mg/kg,显示与单独接种疫苗相比,伊匹单抗单独使用或与肽疫苗联合使用能显著提高生存效益约33%。在一线治疗中,10 mg/kg剂量的伊匹单抗联合达卡巴嗪虽然在统计上显著,但提供的治疗效果有限,因此不推荐联合用药。长期随访数据证实了这一点,表明达卡巴嗪和伊匹单抗联合治疗的5年生存率约为20%,与单独使用伊匹单抗的情况相似。此外,另一种单克隆抗体西木单抗(tremelimumab)单药治疗的长期生存率同样为20%,且其对脑转移患者的疗效也已得到证实。
因为治疗可能导致最初的肿瘤进展或新病变出现,已经制定了免疫相关反应标准(irRC)以避免过早中断治疗。在3 mg/kg剂量下,40%的患者会出现不良事件,大多数与免疫相关(irAE),例如皮疹、结肠炎、肝炎和垂体炎。大约20%的患者会出现3-4级不良事件,极少数情况可能致命。内分泌衰竭通常需要永久性激素替代,但这些事件通常会在类固醇治疗后自行缓解或消退。对于严重的irAE,通常使用大剂量类固醇治疗,有时还需使用其他免疫抑制剂,如抗TNF-α抗体。
关于伊匹单抗的剂量有效性,一项比较0.3、3和10 mg/kg的随机II期试验显示,10 mg/kg剂量更为有效,但伴随更高的毒性。2016年的随机III期试验结果明确指出,对于晚期黑色素瘤患者,10 mg/kg的剂量较3 mg/kg更为有效,总体生存效果显著(HR 0.84; P < 0.04),3年生存率的绝对差异为8%(31%对23%)。这些疗效的提高是以增加的毒性为代价的(3-5级事件率分别为34%与19%,30%与14%)。目前还未确定4次3周间隔的给药(诱导期)与之后的维持治疗的具体价值。
34.2.2 生物标志物
目前尚未确立对伊匹单抗治疗反应的可靠生物标志物。与更高应答率相关的因素包括免疫相关的不良事件、淋巴细胞计数增加、嗜酸性粒细胞计数增加、NY-ESO-1抗原的表达,以及体外对调节性T细胞(Treg)功能的抑制。此外,近年来的研究表明,血清中可溶性CD25的高水平,尤其是当与乳酸脱氢酶(LDH)的高水平同时出现时,可能预示着较差的预后。总体而言,目前我们主要拥有的是预后生物标志物,而缺乏临床上有重要预测价值的生物标志物。
34.2.3 黑色素瘤的辅助治疗及伊匹单抗的近期批准
目前,为III期黑色素瘤患者批准的辅助治疗药物包括重组干扰素α-2b(在美国和欧盟),此药物的批准基于ECOG 1684试验结果;以及聚乙二醇化干扰素α-2b(在美国),其批准则基于EORTC 18991试验。对辅助干扰素治疗的分析显示,治疗的剂量和持续时间似乎对治疗效果没有显著影响,且只观察到对生存率约3%的改善。因此,干扰素的辅助治疗并未被广泛接受或成为治疗标准。
34.2.3.1 伊匹单抗单抗延长无复发期和总生存期
在EORTC 18071试验中,951例III期黑色素瘤患者,在接受完全区域淋巴结切除术后,被随机分配接受伊匹单抗10 mg/kg或安慰剂,每3周一次静脉输注共4次(诱导期),随后每3个月一次,持续3年(维持期),或直至疾病复发或出现不可接受的毒性为止。研究的主要终点是无复发生存期(RFS)。2015年的结果显示,伊匹单抗显著改善了RFS(风险比0.75, p=0.0013),并因此获得了FDA的批准。到2016年,中位随访时间达到5.3年,数据显示,与安慰剂相比,伊匹单抗显著提高了总生存率(OS)(死亡风险比0.72; 95.1% CI, 0.58-0.88; p=0.001)和无远处转移生存期(DMFS)(死亡或远处转移的风险比0.76; 95.8% CI, 0.64-0.92; p=0.002)。伊匹单抗组的5年OS率为65.4%,安慰剂组为54.4%;伊匹单抗组的5年DMFS率为48.3%,安慰剂组为38.9%。先前观察到的无复发生存获益得到了维持(死亡或复发的风险比0.76; 95% CI, 0.64-0.89; p<0.001)。治疗效果在各亚组中总体一致,IIIC期患者似乎比IIIB期和IIIA期患者获益更多,这是唯一一个没有明显获益的亚组(HR 0.98)。
34.2.4 溃疡性黑色素瘤患者获益最显著
事后分析显示,在前哨淋巴结阳性和可触及淋巴结阳性的黑色素瘤患者中,伊匹单抗的治疗效果都有显著提升。这与EORTC的辅助试验18952和18991中,使用干扰素(IFN)和聚乙二醇化IFN治疗的前哨阳性疾病患者获得更大益处的结果一致。同样,溃疡性原发肿瘤的患者从治疗中获得的益处最大,这突显了溃疡性黑色素瘤作为一个独立的生物实体的特性。然而,与EORTC 18952和18991试验中干扰素治疗的结果相反,非溃疡性黑色素瘤患者在接受伊匹单抗的辅助治疗时也显示出了治疗益处。这与干扰素治疗未显示任何益处形成鲜明对比,最近对所有干扰素辅助治疗与观察试验的个体患者数据(IPD)分析也证实了这一点。
34.2.4.1 毒性和生活质量
在EORTC 18071伊匹单抗辅助试验中,尽管发生了较高比例的严重不良事件,全球健康生活质量评分在治疗组间并无显著差异。这一点有些出乎意料,因为只有42%的患者能接受超过4剂的伊匹单抗,而只有28.9%的患者接受了超过1年的治疗。在接受伊匹单抗的患者中,有41.6%发生了3-4级免疫相关不良事件(irAE),而在安慰剂组中这一比例为2.7%。其中最常见的严重irAE包括腹泻/结肠炎(17.2%)、肝炎(15.2%)、内分泌疾病(7.8%)、垂体炎(4.4%)和神经系统事件(1.1%)。此外,有5例患者因药物相关原因死亡,包括3例结肠炎、1例心肌炎和1例因格林-巴利综合症导致的多器官衰竭。大多数严重irAE发生在治疗的诱导期。在停用伊匹单抗并开始皮质类固醇治疗后,除内分泌治疗外(中位缓解时间为31周),其他不良事件的中位缓解时间为6周。
尽管伊匹单抗在无复发生存期(RFS)、无远处转移生存期(DMFS)和总生存期(OS)方面提供了持续改善,但它也带来了不小的免疫相关不良事件(irAE),这要求医疗团队具备专业知识和经验,以便能够及时识别和按照已建立的治疗方案进行处理。因此,这种治疗应由经验丰富的中心执行。
此外,试验结果并未显示在完成诱导期四次给药后需要进行维持治疗。对于复发风险较低的IIIA期患者,伊匹单抗未显示出显著效果,因此对这一剂量的伊匹单抗使用及其相关毒性的合理性值得进一步探讨。
34.3 与伊匹单抗联合治疗
伊匹单抗与其他免疫调节剂、抗血管生成药物、化疗药物或靶向药物的不同组合方式正在被广泛研究。这些联合治疗的设计原则往往基于选用能够诱导免疫原性细胞死亡的药物。鉴于放疗也能引发免疫原性细胞死亡,关于放疗联合伊匹单抗增强体外抗肿瘤效果的报道激发了多项临床研究,以进一步探讨这一现象。
34.4 化疗
目前已发布的关于化疗联合伊匹单抗治疗黑色素瘤的研究包括:
1. 达卡巴嗪(DTIC): 一项III期试验比较了达卡巴嗪与伊匹单抗(10mg/kg)联合一线治疗晚期黑色素瘤患者的效果,显示联合治疗提高了生存率。然而,中位生存获益仅为2.1个月,这一结果令人失望,并且联合用药的效果并不被认为优于单独使用伊匹单抗。长期生存率为20%,表明联合治疗并无优势,而且这种非免疫原性化疗与伊匹单抗的联合使用在临床上并未广泛采用。
2. 福莫司汀(Fotemustine): 在一项开放标签单组II期试验中,86名晚期黑素瘤患者,包括20名无症状脑转移患者,接受了诱导治疗,每3周静脉注射10mg/kg伊匹木单抗,共4个剂量,同时每周注射100mg/m2福莫司汀,持续3周。从第9周到第24周,每3周注射一次福莫司汀。证实临床反应的患者从第24周开始进行维持治疗,每12周使用伊匹单抗,每3周使用福莫司汀。在研究人群中,46.5%的患者实现了疾病控制,50%的脑转移患者实现了疾病控制。但由于其较大的毒性,55%的患者出现3级或4级治疗相关不良事件。由于抗PD1单药治疗的出现,这种联合疗法很少使用。
3. 卡铂/紫杉醇: 一项随机II期试验比较了卡铂+紫杉醇和伊匹单抗(4次剂量,3mg/kg)与这些药物的顺序治疗。参与研究的黑色素瘤类型包括皮肤、粘膜、眼部及未知原发部位的黑色素瘤患者。根据免疫相关反应标准(irRC),14名可评估患者在24周的缓解率(RR)为35.7%,疾病控制率(DCR)为64.3%,63%的患者出现3-4级不良事件。目前,由于抗PD1单药治疗及抗CTLA4和抗PD1联合治疗的高效性,整体化疗-免疫联合治疗的使用在黑色素瘤治疗中已被限制。
34.5 抗血管生成剂
在一项II期研究中,46例转移性黑色素瘤患者接受了伊匹单抗(剂量为3或10 mg/kg)和贝伐单抗(一种针对VEGF的单克隆抗体,剂量为7.5或15 mg/kg)的联合治疗。治疗方案包括初始的4个剂量,每3周一次,间隔4周,之后每12周维持一次治疗。整体疾病控制率达到了67.4%,其中包括8例部分缓解和22例病情稳定。中位生存期为25.1个月。免疫相关不良事件(irAEs)包括1例巨细胞动脉炎、2例肝炎和2例葡萄膜炎。在治疗期间进行的肿瘤活检中,观察到了广泛的CD8(+) T细胞和巨噬细胞浸润。初步经验表明,贝伐单抗与伊匹单抗的联合治疗在安全性方面表现良好,这进一步指出了VEGF-A阻断在炎症反应、淋巴细胞迁移和免疫调节方面的潜在作用,需要进一步的研究来探索和理解这些机制。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 廖媛
图文排版 | 吕思贤 蔡倩薇
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏