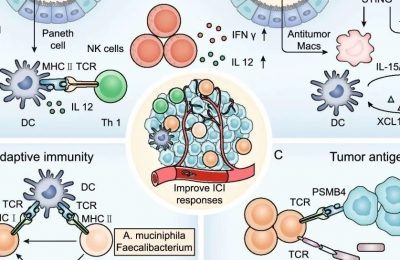
13.5 作为肿瘤疫苗靶点的肿瘤特异性基因改变
与免疫普遍激活的疗法(如免疫检查点抑制剂或干扰素)不同,接种疫苗可诱导针对不同肿瘤表位的更特异性的定向免疫反应。
Table 13.1列举了目前肿瘤疫苗开发的一些方式:包括主动接种,即接种主动免疫细胞,如树突状细胞、CAR T细胞或新抗原表位特异性T细胞,或使用多肽进行被动免疫,或使用针对一个或多个肿瘤特异性表位的RNA/DNA(Table 13.1)。
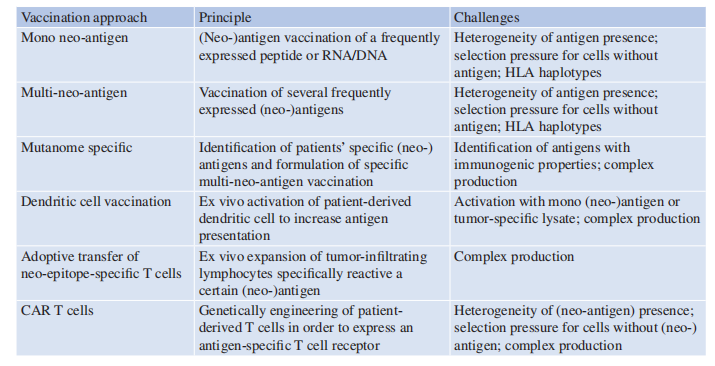
Table 13.1 疫苗开发方式
主动免疫治疗使用患者来源的细胞,在体外激活和扩增它们,并将它们回输到患者体内。这种个性化的免疫疗法需要非常苛刻和复杂的技术支撑,使得大型III期临床试验的商业化和实施更加复杂。
树突状细胞疫苗是一种已经被批准的安全的且能产生疗效的疫苗,例如对黑色素瘤、胶质母细胞瘤和前列腺癌均有疗效。
简而言之,这种方法就是先从患者身上提取外周血单核细胞和树突状前体细胞并进行体外扩增。再使用促炎细胞因子、CD40L或TLR激动剂使单核细胞成熟。然后,成熟的树突状细胞通过接触多肽、蛋白质、已知的肿瘤新抗原或患者特定的肿瘤裂解物来装载肿瘤抗原。
这些激活的、成熟的树突状细胞被重新注入患者体内,随后可以通过向T细胞递呈抗原以及维持B细胞记忆功能和自然杀伤细胞的激活来诱导特异性的免疫反应。
到目前为止,树突状细胞疫苗疗法仅在一项转移性去势耐受前列腺癌的前瞻性III期临床研究中显示出疗效。
过继转移新抗原特异性T细胞是目前正在进行临床试验研究的另一种免疫治疗方法,其已被证明在免疫调节治疗通常效果不好的实体肿瘤中也能产生免疫反应,如结直肠癌和胆管癌。
在这里,二代全基因组测序被用来揭示可能作为新抗原表位发挥作用的非同义突变。从患者上提取树突状细胞,树突状细胞可以将这些新表位呈递给从肿瘤组织中分离出来的T细胞(肿瘤浸润性T淋巴细胞)。然后将对呈递的新抗原有特异性反应的T细胞在体外扩增,再注入患者体内。
新抗原特异性T细胞可以启动肿瘤特异性免疫反应,这使得这些抗原特异性T细胞持续存在并控制肿瘤的发展。
另一种免疫治疗方法是应用具有嵌合抗原受体(CAR)的T细胞。
为了产生抗原特异的CAR T细胞类型,需要从患者身上获取外周T细胞。接下来,通过病毒或非病毒方法将所需的抗原特异性CAR引入T细胞,从而产生具有抗原特异性T细胞受体的T细胞。CAR T细胞在体外扩增,并重新注入患者体内。
CAR T细胞是可以靶向表达抗原的细胞,以不依赖于MHC的方式增强T细胞效应功能。因此,人类白细胞抗原单倍型可能不会影响CAR T细胞治疗的疗效。
目前实体癌症中CAR T疗法的潜在靶点有人表皮生长因子受体2(HER2)、表皮生长因子受体(EGFR)、间皮蛋白和癌胚抗原(CEA)等新抗原。
除了对恶性血液病已经有实质性的临床疗效外,第一批病例报告也显示出对实体癌有疗效,目前有几项研究正在招募研究对象。
除了使用体外培养患者特定细胞的治疗方法外,还设计了几种基于多肽或RNA/DNA的疫苗接种方法,以通过增加(新)抗原的可用性来增强宿主的免疫反应。
单一新表位疫苗仅针对特定肿瘤的一种特定抗原。因此该靶表位必须在大多数癌细胞中表达,以确保启动的T细胞反应是有效的。
目前已经进行了一些临床试验研究,例如针对HER2过表达乳腺癌的HER2特异性疫苗接种或针对黑色素瘤的gp100疫苗。
然而,单表位导向的免疫反应导致抗原阳性癌细胞的选择压力大,并为阴性细胞提供生存优势,造成了潜在的免疫逃逸。
此外,多肽因HLA单倍型的不同而与MHC的亲和力不同,这限制了某些多肽疫苗对表达特定人类白细胞抗原单倍型的患者的疗效。
与单表位疫苗相比,使用肿瘤的几个频繁出现的表位的多表位疫苗被认为可以产生更广泛的免疫反应,并更有效地防止免疫逃逸。
在疫苗接种中含有一组预定义的表位,这些表位已被鉴定为在某种肿瘤类型中频繁表达。然而如前所述,尽管特定肿瘤的组织学和位置可能具有可比性,但特定患者的特异性抗原特征是非常独特的。
突变特异性疫苗接种提供了一种更加个性化的疫苗接种方法:可以在特定的患者中识别出特定的多个新表位,并促进个性化疫苗的制造。
这些新表位可以通过基因组测序和新抗原预测或直接通过质谱仪识别。因此,肿瘤的异质性的问题得到了更充分的解决,也更有可能应用于临床,因此诸如特定抗原或人类白细胞抗原单倍型的存在的限制减少了。
然而,并不是所有的基因突变都会导致转录蛋白和免疫原性表位的产生。只有大约20%-40%的(新)抗原被免疫系统识别并导致肿瘤特异性T细胞反应的产生。
因此,一个关键的问题是如何以个性化的方式识别相关的免疫原性癌症突变并进行治疗探索。在这里,野生型多肽和突变新抗原之间的数值差异以及MHC I和多肽相互作用的构象稳定性对于定义新抗原的免疫原性至关重要。
目前,一些临床试验正在测试各种新表位疫苗方法,要么是单一疗法,要么是联合疗法。
像免疫检查点抑制剂的应用一样,疫苗疗法需要讨论的一个重要问题是确定哪些患者最有可能从这些特定的方法中受益。在这里应该考虑到疾病的范围。
接种疫苗虽然会产生肿瘤特异性免疫反应,但很可能不会导致肿瘤缩小,而是控制现有的肿瘤大小。因此,仅有肿瘤微小病灶残留的患者可能受益最大。
因此,严谨的试验设计对于确定从疫苗的治疗方法中受益最大的患者群体也是至关重要的。
13.6 作为免疫检查点抑制剂免疫反应预测生物标记物的肿瘤基因改变
除了在接受靶向CTLA4和PD1免疫检查点的抑制剂治疗的患者中观察到高应答率外,还有很大一部分患者没有反应。
因此,迫切需要准确和精确的预测生物标志物来充分选择应答可能性最高的患者(Table 13.2 )。
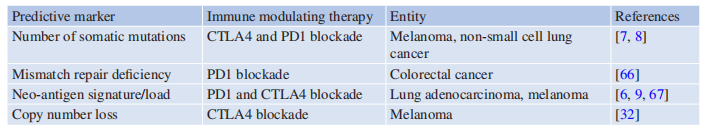
Table 13.2 肿瘤的基因改变可作为免疫检查点抑制物治疗的预测生物标志物
事实上,更确切地说,总的突变负荷而不是特定变化与免疫应答和对免疫检查点抑制剂应答的可能性增加相关(Fig.13.4)。
同样,与突变频率较低的肿瘤(如乳腺癌)相比,黑色素瘤或肺腺癌等突变负荷高的癌症类型对免疫调节疗法更敏感。
由暴露于高致癌物质导致的癌症类型,如紫外线辐射引起的黑色素瘤或吸烟者的肺癌,或病毒诱导的癌症类型,如头颈部鳞状细胞癌,呈现出特别高的突变负荷。
有趣的是,突变负荷在不同癌症之间差异很大,尽管其他特征,如组织学、位置和驱动突变的因素都非常相似。一些突变负荷相当低的癌症类型,如结直肠癌或胶质母细胞瘤,存在某些特定的遗传亚型如微卫星不稳定或错配修复缺陷时,可能会有出乎意料的反应。
然而,体细胞突变数量中位数较低的癌症类型也表现出令人印象深刻和持久的反应,如肾细胞癌。他们认为,除了原始突变数量外,突变的免疫学质量可能会影响癌症免疫监测。
更准确地说,突变负荷与给定肿瘤的免疫原性相关,因为每增加一个突变,就会增加产生相关患者特异性癌症新抗原的几率。
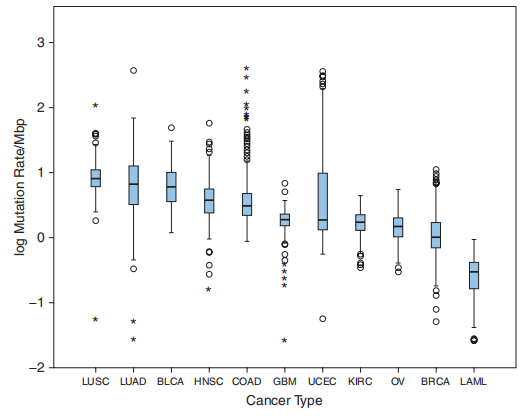
Fig.13.4 不同原发肿瘤类型的突变负荷;(LUSC肺鳞状细胞癌、LUAD肺腺癌、BLCA膀胱尿路上皮癌、hNSC头颈部鳞状细胞癌、COAD结肠腺癌、GBM胶质母细胞瘤、UCEC子宫体子宫内膜癌、KIRC肾透明细胞癌、卵巢浆液性囊腺癌、BRCA乳腺浸润性癌、LAML急性髓系白血病)
事实上,大量的突变和高负荷的新抗原与CD8+肿瘤浸润淋巴细胞的增加和预后的改善有关。
根据与MHC复合物的亲和力、与野生型多肽的不同以及肿瘤内新抗原的异质性,这种新抗原的免疫原性可能会有所不同。
在黑色素瘤和其他高突变负荷的肿瘤中发现的大多数突变都是与细胞转化过程无关的“伴随突变”。因此,这些癌症中绝大多数潜在的新表位都是患者特有的。
在对CTLA4抑制剂有反应的黑色素瘤患者中,发现了与许多病毒和细菌抗原同源的新表位特定新抗原特征。这种特殊的新抗原标记是否在其他实体瘤中也具有预测潜力,以及能否定义具有高突变负荷的肿瘤的最终截断值,目前尚不清楚。
此外,突变载量的丢失与对CTLA4抑制的反应的可能性相关。这里突变载量的丢失与黑色素瘤的进展有关,可能是免疫逃逸的原因之一,因为发现了突变载量的丢失与免疫相关基因表达下调的相关性。有趣的是,低突变载量的丢失和高突变负载的效应对临床反应具有非冗余效应,表明几个预测标记物的组合可能可以提供更准确的反应预测。一些截断编码干扰素受体相关的JAK1和JAK2的基因改变被证明与对抗PD1免疫检查点抑制剂的获得性抵抗有关。
13.7 个性化免疫治疗:免疫调节疗法的联合
虽然免疫调节疗法已经观察到令人鼓舞的应答率,但大多数患者仍然不能从目前可用的治疗中长期受益。这可能是由于除了宿主特异性因素外,肿瘤同时具有几个活跃的免疫逃逸因素。
免疫调节疗法相互结合或与其他已建立的治疗方案相结合,可以通过改善癌症-免疫循环的不同步骤来增强宿主和癌症的相互作用。
缺乏可用的抗原可以通过接种肿瘤特异性抗原来克服。
目前临床前研究表明,疫苗接种与检查点抑制具有协同效应,尽管CTLA4抑制和gp100疫苗联合的临床研究并未显示出具有临床意义的额外疗效。然而,最近关于肽疫苗疗法的发现,包括建立突变体特异性疫苗,被认为可能成为免疫检查点抑制剂的一个更好的搭配。
所谓的非局部性效应主张放射治疗和免疫检查点抑制剂的合理结合。
从理论上讲,放射治疗首先通过肿瘤细胞凋亡诱导肿瘤特异性T细胞反应来增加抗原的可获得性。此外,放疗对炎性微环境有多个局部影响,并诱导肿瘤与抗原提呈细胞、巨噬细胞和细胞毒性T细胞的浸润。
因此,疫苗接种和放射治疗以及其他导致抗原呈递增加的治疗方法的联合可以克服抗原呈递不足的问题,而抗原呈递和免疫检查点抑制剂的联合使用可能具有协同作用。
然而,目前人们对如何识别抗原提呈不足的患者知之甚少,因为还没有可靠的标记物来量化抗原提呈的有效性。
如上所述,肿瘤特异性免疫反应受到高度调控,因为几个TCR辅助受体通过增强或抑制信号来控制由此产生的T细胞反应。
PD1和CTLA4都是抑制T细胞反应的途径,实际上减少了T细胞的激活。同样,这种抑制导致肿瘤特异性T细胞反应的“释放”。
然而,PD1检查点抑制会导致其他免疫抑制性的免疫检查点通路的上调,如TIM3。因此,两种检查点抑制剂联合使用可能会克服这种免疫逃逸机制。
尽管考虑到较高的毒副作用,CTLA4和PD1阻滞剂联合使用仍比单独使用检查点抑制剂在临床上更有效。
此外,CTLA4治疗被证明增加了肿瘤中存在的TCR克隆性,从而提高了对PD1定向治疗的应答的可能性。
目前有几项研究正在研究靶向TIM3、LAG3、OX40等的第二代检查点抑制剂与第一代检查点抑制剂联合使用的临床疗效。
除了免疫检查点抑制剂外,进一步的组合旨在增加肿瘤内T细胞的密度。
PI3K和MEK通路被证明影响肿瘤组织内T细胞的密度。因此,在免疫检查点抑制剂中添加MEK酪氨酸激酶抑制剂可能会增加肿瘤浸润性淋巴细胞的密度,将“冷”肿瘤转变为“热”肿瘤,从而对免疫检查点抑制剂的治疗更敏感。
另一个有前景的组合是在标准化疗方案中添加免疫检查点抑制剂,因为许多标准化疗已被证明具有免疫调节功能。
以铂为基础的标准化疗和PD1抑制剂的组合显著提高了有效率和生存率。
最后,为了产生持久的适应性免疫反应,还必须考虑先天免疫系统。人们早就知道巨噬细胞和中性粒细胞以一种临床相关的方式调节T细胞的活动。
最近,有研究表明巨噬细胞复极化可以导致非免疫原性肿瘤中的淋巴细胞对肿瘤的反应增强。目前,利用这些调控轴的临床试验正在进行中。
综上所述,癌症免疫治疗正迅速从单剂疗法向联合疗法转变,以解决患者免疫系统和给定癌症之间的特定相互作用。
免疫调节疗法的结合肯定会产生另一层复杂性,这必须通过临床前研究来更好地了解产生潜在复杂性的生物学原理,以及发现相应的的生物标记物来解决。
在这里,潜在的预测算法必须结合肿瘤本身的几个遗传特性,以及由特定宿主和肿瘤的相互作用引起的宿主特异性因素和动态因素。
在对炎性肿瘤微环境的深入了解中,必须评估和进一步分析肿瘤和宿主的遗传特征,以开发预测性生物标记物信号。
我们必须监测连续肿瘤活检的即时治疗效果,以便更好地理解反应机制,更重要的是了解个体患者的耐药机制。这些数据对我们的预测算法非常重要。
最终,我们可以设想临床试验策略,每个患者都接受不同的药物组合,甚至可能按顺序改变。肿瘤治疗效果的实时评估将有助于不断修改个别患者的治疗策略。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab学术星球现已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~

加入知识星球~
用于OncoLab读者交流互助永久免费
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏