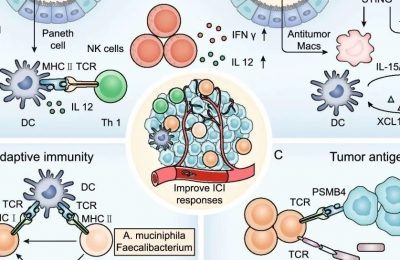
14.1 引言
自从发现MHC呈递的蛋白质片段(多肽)是T细胞识别抗原的基础后,人们对利用多肽诱导T细胞反应的治疗方法就产生了极大的兴趣。
CD8+ T细胞(Tc)可以识别由MHC-l类分子(人类的HLA l类)提呈的氨基酸短肽。这些短肽由8-11个氨基酸组成,且可以在所有有核细胞上表达。
而CD4+ T细胞(Th)可以识别由MHC-II类分子(人类的HLA ll类)提呈的长度为12-15个氨基酸的多肽,这些MHC-II类分子主要在免疫细胞上表达,如树突状细胞(DC)、巨噬细胞和B细胞。
由于T细胞只能识别由HLA提呈的抗原片段(表位),所以当这些表位被HLA提呈到细胞膜上时,T细胞不会被体液中游离的抗原激活,而会专门识别与T细胞受体结合的HLA-抗原肽复合物。
重要的是,T细胞可以识别在细胞内任意位置表达的蛋白质片段,这为我们提供了一个理想的监测系统,这个系统甚至可以检测细胞最偏远位置(如细胞核)的蛋白质片段。因此,T细胞反应可以看作是对抗病原体和癌细胞的特异性适应性细胞介导的免疫反应。
由于诱导免疫耐受的机制并不是万无一失的,所以T细胞治疗也可以针对过度表达的自身抗原或分化抗原,但通过免疫耐受来削弱与这些抗原有关的T细胞谱系可能也会带来新的问题。
14.2 治疗性肿瘤疫苗的作用模式
肿瘤治疗性疫苗需要诱导强大细胞毒性T细胞反应(CD8+ T细胞反应),这可以通过皮下、皮内或肌肉注射不同的疫苗来实现:DNA、RNA、合成的长肽(SLP)或包含肿瘤相关抗原序列的重组病毒。
注射到体内的疫苗抗原会被DC提呈(例如,表皮或真皮树突状细胞)。然后,DC通过传入淋巴管迁移到疫苗引流淋巴结,并定居在这些淋巴结的T细胞区,通过与CD4+ T细胞和CD8+ T细胞适当的接触来启动T细胞反应。
正常激活的T细胞会通过淋巴管离开淋巴结,最终通过胸腔导管到达血流。在血液中,它们有一定概率会渗入携带抗原的肿瘤部位。
通常那里的T细胞必须应对恶劣的微环境,包括调节性T细胞(Treg)、T细胞检查点配体(如PD-L1)、髓系抑制细胞(MDSC)以及由T细胞释放的因子,如免疫抑制细胞因子、趋化因子和吲哚胺2,3-双加氧酶(IDO)。而这些因子会损害T细胞的迁移、增殖及功能(Fig 14.1)。
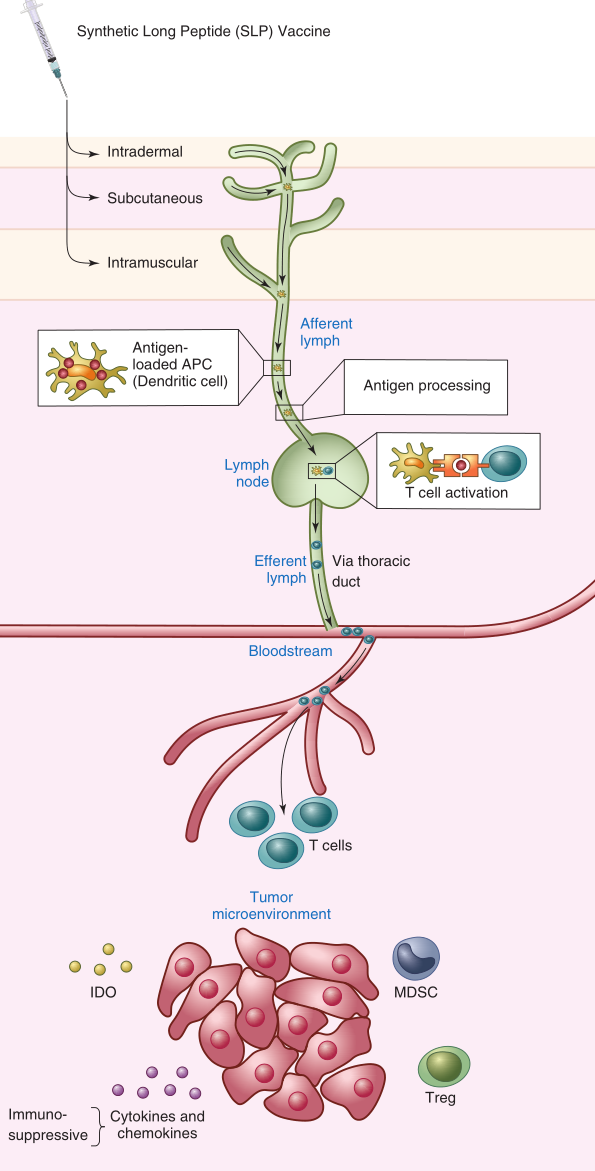
Fig. 14.1 人工合成长肽(SLP)疫苗的作用方式
SLP能有效地运送肿瘤相关抗原,并且在疫苗注射区很容易接触到DC。携带抗原的DC通过传入淋巴管迁移到疫苗引流淋巴结,进入皮质旁T细胞区域,在那里继续对摄入SLP的抗原进行处理,之后它们将抗原呈递给CD4+和CD8+ T细胞,激活T细胞。
活化的T细胞通过传出淋巴管离开淋巴结,部分迁移到肿瘤中肿瘤抗原表达的部位。在那里激活的T细胞会面临恶劣的肿瘤环境,其中包括对T细胞不利的细胞成分,如髓系来源的抑制细胞(MDSC)和Treg,以及免疫抑制趋化因子和细胞因子,IDO酶的表达,以及抑制T细胞检查点的配体,如PD-1和LAG-3。这些情况共同损害T细胞的迁移、功能和扩增。
14.3 什么才是一种好的肿瘤治疗性疫苗?
我们回顾了决定肿瘤疫苗成败的因素。总结出成功的肿瘤疫苗必须满足下列四个要求:
(1)选择正确的肿瘤抗原,
(2)选择有效的疫苗平台,
(3)使用适当的疫苗佐剂,
(4)结合适当的联合治疗使用。
Table14.1列出了肿瘤疫苗成功的关键因素和相应的选择。
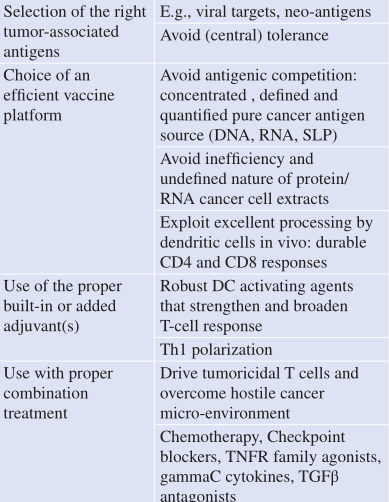
Table 14.1 治疗性癌症疫苗成功开发的关键因素
在抗原的选择上,优先选择不受胸腺内免疫耐受机制影响的相关肿瘤抗原,尤其是由人类乳头瘤病毒(HPV)、爱泼斯坦-巴尔病毒(Epstein-Barr Virus)、人类嗜T细胞病毒I(HTLV-I)、乙肝病毒、丙型肝炎病毒、卡波西肉瘤病毒(KSV)和默克尔细胞癌病毒等癌症病毒编码的抗原。
全世界大约20%的癌症是由病毒引起的。而在引起人类癌症的原因中占比更大的是的一种新的、非常重要的抗原类别,它们包括在香烟烟雾中的化学致癌物(肺癌、H&N鳞状细胞癌、膀胱癌)、紫外线(黑色素瘤和皮肤基底细胞癌)或DNA修复缺陷(例如微卫星不稳定的结直肠癌)引起的癌细胞突变产生的新抗原。
这些新抗原是癌症特异性T细胞的高效靶点,发现其重要性源于人们观察到针对CTLA-4或PD-1的检查点阻断单抗的临床疗效与个体患者癌症突变数量之间有显著相关性。在一名患者中,针对紫外线诱导突变的CD8+ T细胞增殖与使用抗CTLA-4抗体的治疗成功有关。
在小鼠模型中,已经预测并验证有可能发生突变的新抗原,并将小鼠成功地接种了含有新抗原的SLP或RNA疫苗。目前较受欢迎的肿瘤疫苗成分是病毒的非自身抗原和突变衍生的新抗原片段,但针对许多过表达的肿瘤-睾丸抗原、分化抗原、Survivin、Wilms Tumor 1(WT1)、野生型或突变型P53和间硫蛋白的T细胞谱系可能也具有诱导强大的CD8+ T细胞反应的能力。
14.4 基于T细胞表位的疫苗接种
经典的预防性疫苗由热灭活或减毒的微生物组成,这些微生物表达的折叠蛋白,可以诱导机体产生针对特定表位的保护性抗体。
然而,治疗性疫苗需要诱导由HLA II或 I类分子提呈且具有特定T细胞识别的表位,从而激活CD4+ T和CD8+ T细胞反应。该表位只有在与HLA II或 I类分子结合时才具有正确的构象。因此,用于诱导T细胞反应的多肽疫苗的组成表位包括具有准确长度的肽(短肽),或包含一个或多个表位的较长的肽(合成长肽,SLP),但这些肽还需要DC进一步处理,以便将精确的表位正确地结合到HLA分子上。
完全匹配的短肽和SLP都已用于治疗性疫苗,但相比之下,SLP更受欢迎。基于T细胞表位疫苗的一个优点是只需要表达该表位丰富区域的氨基酸序列,而可以忽略大量不包含的T细胞表位的蛋白质片段。
除了免疫沉默的序列外,DC对蛋白质的处理效果也很差,差到不足以将其呈递给T细胞(特别是CD8+ T细胞)。而SLP能被DC有效地处理,并分别呈递给CD4+ T和CD8+ T细胞。
在合成SLP疫苗时,关键是要包括能够与最常见的HLA I和II类分子结合的表位。为此,在多肽疫苗中还需要有足够长度的氨基酸序列来容纳最常见的HLA I和II类分子的结合基序列,这与胞浆中的蛋白酶体处理多肽疫苗的能力相关,胞浆中经过处理后的多肽疫苗可以通过抗原处理转运体(TAP)(HLA I类处理途径)进行转运,或者通过DC内体中的组织蛋白酶(HLA II类处理途径)进行处理。
14.5 短肽与长肽在肿瘤疫苗中的比较
多肽疫苗的最初尝试只涉及小鼠体内单一的MHC I类结合表位+佐剂。尽管这种疫苗在几个实例中都显示出抗病毒或抗肿瘤活性,但这种短肽疫苗(<15个氨基酸)显然不是最优选择,其中的原因有很多。首先,短肽可以直接与所有有核细胞的HLA I类分子结合,而不需要进行抗原处理。
因此,在缺乏共刺激分子的情况下,疫苗短肽在非专业抗原提呈细胞(APC)的HLA I类分子中浓度较高,会导致短暂的CD8+T细胞反应甚至CD8+T细胞耐受。
短肽疫苗的第二个缺点是缺乏激活CD4+T细胞的 II类表位。而CD4+T细胞在诱导和维持最佳的CD8+T细胞反应以及促进CD8+T记忆细胞的产生中是必不可少的,并且CD4+T细胞本身可以发挥重要的抗病毒或抗肿瘤功能。
此外,接种用不完全弗氏佐剂(IFA)配制的短肽疫苗会导致T细胞反应减弱,产生这种现象的原因一部分是上述的两点,另一部分是由于用IFA配制的短肽会使T细胞移动到接种疫苗部位而不是肿瘤部位。
相反,用SLP(>20个氨基酸长度)接种,而不是用IFA或相关佐剂Montanide ISA-51配制的短肽接种,会诱导持续的CD8+T细胞反应和强大的抗肿瘤免疫反应。
事实上,接种用IFA或Montanide配制的SLP疫苗也能使癌症病变前或癌症患者体内维持强大而持续的CD8+T细胞反应和记忆T细胞反应。
使用成熟的DC免疫注射前,在体外负载一定程度的短肽或用抗CD40的激动型抗体以替代CD4+T细胞信号,再加上或不加TLR3配体PolyI:C,可以在一定程度上克服短肽诱导的耐受。
在皮下或体外注射SLP后,DC能够有效地处理SLP,从而高效地将SLP呈递给MHC I类和II类分子。此外,DC对被MHC I或II类分子提呈的SLP的处理比对蛋白质的处理更高效。SLP能够在临床前和临床环境中诱导强大的CD4+和CD8+T细胞反应,而接种完整蛋白疫苗与显著的CD4+T细胞反应有关,但与CD8+T细胞反应无关。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab学术星球现已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
用于OncoLab读者交流互助永久免费
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏