1.通过靶向galectin-糖基相互作用重编程肿瘤免疫微环境
Gabriel A. Rabinovich – 生物学和实验医学研究所,阿根廷布宜诺斯艾利斯市
Gabriel Rabinovich在“来自赤道以南的甜蜜冒险”中展示了他对Galectin-1(Gal-1)的几十年研究。Gal-1在大多数人类肿瘤中上调,并与预后不良相关。它由癌细胞、成纤维细胞和一些免疫细胞表达和分泌,并具有两个结合糖基N-乙酰-乳糖胺(LacNac)的位点,LacNac存在于复杂的N-糖基和核心1/2 O-糖基中。Gal-1作为一个糖基检查点,促进肿瘤免疫逃逸和血管生成。
Gal-1-糖基相互作用通过诱导Th1、Th17和CD8+ T细胞的选择性死亡,同时保留携带α(2,6)-唾液酸化细胞表面糖蛋白的Th2和Treg细胞,通过IL-27和IL-10驱动的回路促进耐受性树突状细胞和M2巨噬细胞极化,以及在髓样抑制细胞(MDSCs)中激活免疫抑制和促血管生成的程序。Gal-1还将肿瘤微环境中的免疫抑制和血管生成联系起来。在缺氧条件下,癌细胞分泌Gal-1,它可以与内皮细胞上的VEGFR2结合,模仿VEGF,并促进血管生成。
在AVAST-M 3期试验中,接受贝伐单抗(抗VEGF mAb)治疗的黑色素瘤患者,循环Gal-1水平升高与复发和死亡风险增加相关,且非应答患者的血浆样本可以通过Gal-1-VEGFR2途径重新编程内皮细胞。总之,Gal-1和其他galectin网络控制肿瘤微环境中的免疫和血管景观,影响癌症的多个标志。
癌症中的galectin驱动回路可以通过小分子碳水化合物抑制剂、天然多糖及其衍生物、肽和肽模拟物、中和单克隆抗体以及截短型galectin来靶向。许多这些方法目前正在各个临床试验阶段进行研究。Rabinovich开发的Gal-1特异性中和mAb在小鼠模型中抑制肿瘤生长和血管生成,并抵消抗VEGF治疗的抗性。它还增加了免疫细胞(尤其是CD8+ T细胞)进入肿瘤的浸润,并诱导MDSCs的重编程。
2.基于白介素-8、中性粒细胞和NETs的抗癌免疫疗法策略
Ignacio Melero – Clínica Universidad de Navarra, Pamplona, Spain
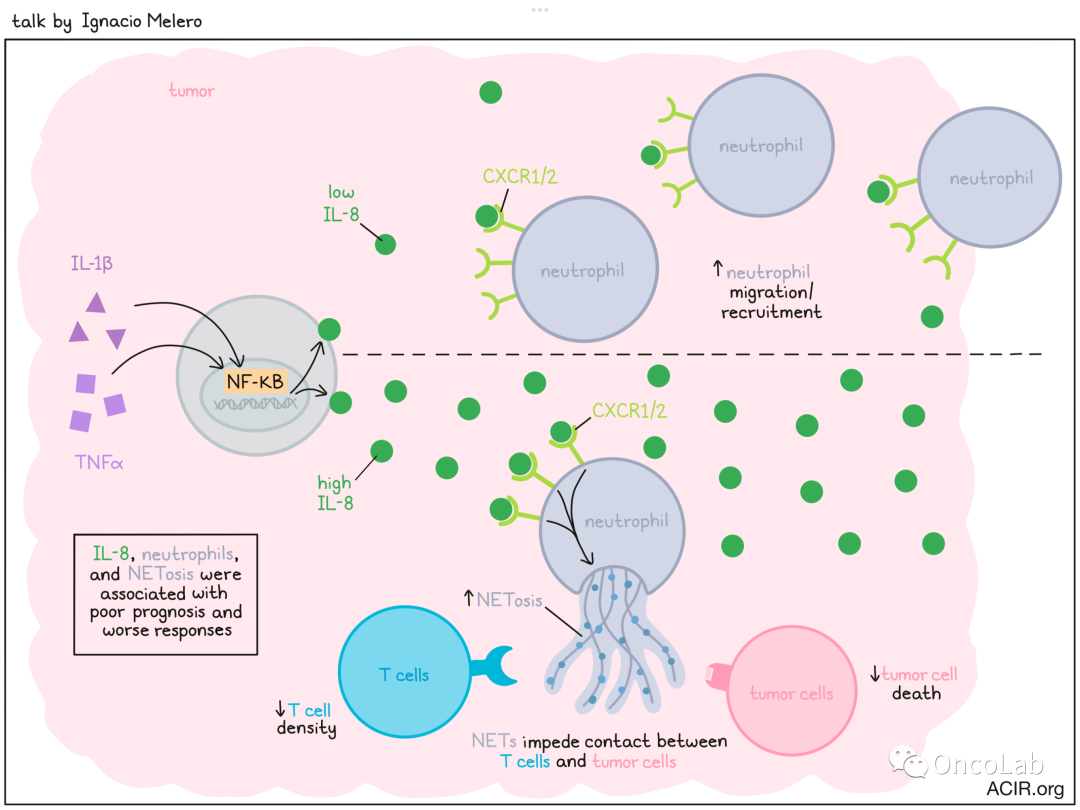
癌症中免疫系统的作用是复杂且常常矛盾的,因为一些免疫细胞努力对抗癌症,而其他细胞则保护它。正如Ignacio Melero所说,这要求免疫治疗师同时扮演纵火犯和消防员的角色。为了抑制不良的免疫反应,Melero专注于中性粒细胞,它们可以发挥多种作用,但通常被认为是促癌的,与预后不良相关。
中性粒细胞能够进行脱颗粒作用、吞噬/内质泡吞作用、产生活性氧物质以及一个称为NETosis的过程,在这个过程中,它们释放包裹着蛋白质和多肽的DNA,形成一个粘性的网状结构,能捕获并杀死微生物,这个网状结构即为中性粒细胞细胞外陷阱(NETs)。在癌症环境中,已知NETs在支持转移和抑制免疫反应中起到了关键的作用。Melero和他的同事发现,这些NETs可能通过阻止T细胞与靶细胞的物理接触,来帮助恶性细胞存活,从而保护癌症。
研究IL-8是因为已知它能吸引中性粒细胞,研究人员发现,在多个临床试验的数据中,癌症患者中高IL-8表达与免疫检查点阻断的反应较差相关,甚至可以作为独立于PD-L1和肿瘤突变负荷的反应生物标志物。IL-8还与肿瘤中中性粒细胞、NETosis和单核细胞的存在呈正相关,与T细胞和IFNγ呈负相关。在更仔细地研究IL-8的浓度时,研究人员发现,低浓度的IL-8诱导中性粒细胞的迁移和招募,而高浓度的IL-8则负责诱导NETosis。
鉴于IL-8与CXCR1和CXCR2受体相互作用,Melero等人证明,阻断CXCR1/2或阻断CXCR1/2下游信号分子可以减少肿瘤类器官、携带小鼠肿瘤的小鼠和携带人肿瘤的人源化小鼠中的NETosis。更重要的是,这种阻断还改善了CD8+ T细胞和NK细胞介导的肿瘤杀伤。与此相一致,不同肿瘤中NET表达与IL-8产生呈正相关,与CD8+ T细胞密度呈负相关;通过血清中的NET测量也可以得到类似的相关性。
接下来,为了研究肿瘤中IL-8产生的增加是由什么驱动的,Melero将注意力转向了由TNFɑ和IL-1β诱导的NF-κB。观察这些细胞因子(IL-8,TNFɑ和IL-1β)在血清中的相关性,小鼠中也观察到了类似的效应(使用CXCL1和CXCL2作为IL-8的同源物)。此外,阻断或注射TNFɑ和IL-1β可以有效地阻止或促进IL-8的产生。从接受抗TNFɑ抗体治疗的患者样本中证明了这一点,治疗后24小时,IL-8血清水平降低。目前正在进行阻断CXCR1/2或IL-8的临床试验,尽管需要高剂量才能完全中和IL-8,但到目前为止,治疗已被证明是安全的,即使与nivolumab和ipilimumab联合使用。此外,研究人员还观察到治疗肿瘤中中性粒细胞的减少。
3.嗜酸性粒细胞与适应性免疫细胞之间的相互作用:乳腺癌免疫检查点阻断治疗新进展
Karin E. de Visser – 荷兰癌症研究所,阿姆斯特丹,荷兰
免疫检查点阻断(ICB)已被证明对实体瘤有效,但在晚期乳腺癌患者中的应答率令人失望,仅有5-10%的患者有应答。尽管PD-L1阳性三阴性乳腺癌(TNBC)患者在ICB加化疗方案下应答率有所改善,但大多数患者仍无法对ICB产生应答。尽管大多数关于ICB应答的研究都集中在T细胞上,但先天和适应性免疫细胞之间的相互作用对有效免疫应答至关重要。
Karin de Visser及其同事对TONIC临床试验中接受ICB治疗的TNBC患者的血液和转移病灶中免疫细胞动态进行了无偏倚的分析。通过与小鼠研究相结合,这使他们能够研究与应答相关的免疫参数。在接受ICB治疗的应答患者中,观察到嗜酸性粒细胞在全身和肿瘤内的增加,而在非应答患者中则没有观察到这种情况。在TONIC临床试验中,全身嗜酸性粒细胞水平增加2倍以上与更好的总生存相关。
在基因工程的KEP(K14-cre;Cdh1f/f;Trp53f/f)小鼠中,自发性侵袭性乳腺癌对ICB单独治疗没有反应,但对ICB和顺铂的联合治疗以T细胞依赖的方式有反应,这与TNBC患者中观察到的情况类似。在这个小鼠模型中,ICB和顺铂的联合导致嗜酸性粒细胞在全身和肿瘤内增加。用抗SiglecF抗体耗竭嗜酸性粒细胞使ICB联合顺铂的治疗效果消失。在另一个基于KEP的多器官转移性疾病模型中,ICB联合顺铂以嗜酸性粒细胞依赖的方式诱导出持久的应答。
为了了解治疗如何调动嗜酸性粒细胞,de Visser及其团队分析了血浆中的细胞因子,发现在ICB治疗的小鼠中IL-5水平上调,而IL-5中和作用消除了ICB的治疗效果。由于CD4+ T细胞是IL-5的主要产生者,研究者通过流式细胞术分选了TNBC患者接受ICB治疗的CD4+ T细胞,并在这些细胞中发现IL-5mRNA上调。消耗CD4+ T细胞导致小鼠模型中嗜酸性粒细胞特征的丢失,这表明ICB治疗诱导CD4+ T细胞产生IL-5,从而增加骨髓中嗜酸性粒细胞的产生,并导致全身嗜酸性粒细胞的积累和激活。
为了确定导致嗜酸性粒细胞进入肿瘤的因素,研究人员分析了顺铂加ICB治疗患者血浆中的细胞因子,发现嗜酸性粒细胞已知的趋化剂IL-33仅在顺铂治疗时上调。IL-33中和作用消除了肿瘤内嗜酸性粒细胞的积累,并降低了对小鼠肿瘤生长的控制。同样,IL-33水平与ICB应答患者(而非非应答患者)的肿瘤样本中嗜酸性粒细胞基因特征相关。用重组IL-33全身治疗小鼠以模拟顺铂的作用,增加肿瘤内嗜酸性粒细胞,但需要与ICB联合以激活CD8+ T细胞。在另一种策略中,Treg消耗导致肿瘤内嗜酸性粒细胞的积累,同样,与ICB治疗的联合是在转移性KEP基础肿瘤模型中改善生存的必要条件。
总之,ICB联合顺铂治疗诱导CD4+ T细胞产生IL-5,这增加了骨髓中嗜酸性粒细胞的产生,导致全身嗜酸性粒细胞的积累和激活,这些细胞被产生IL-33的肿瘤吸引,从而改善乳腺癌的ICB应答。
4.免疫治疗中肠道和肿瘤微生物介导免疫应答的机制
Florencia McAllister – UT MD安德森癌症中心,休斯顿,TX
许多类型的微生物,尤其是细菌,在所有具有粘膜组织的身体屏障或身体屏障可能被病原体破坏的地方都非常丰富,因此可能对各种类型的癌症产生重要影响。关于肠道菌群对抗肿瘤免疫应答的影响的研究引领了这个领域的发展。
Florencia McAllister首先简要回顾了她的团队和其他团队发表的研究,重点强调了条件控制(地理范围内的队列、收集方法等)的重要性,并且应用了多种现有和正在开发的工具来提升可信度,以及寻找功能和机制信息以便将来采用更有针对性的方法。重点关注肿瘤内微生物(TRMs),重要的新工具包括评估微生物与肿瘤和免疫细胞之间的空间关系,以及定量和定性的物种鉴定新核酸方法。
McAllister还提供了一些关于微生物与药物治疗之间的相互作用、免疫激活或抑制微生物对胰腺癌生存的影响,以及微生物与原发性和转移性肿瘤之间关系的开创性例子。在她的新工作中,McAllister开发了一种量化微生物/宿主DNA比例的工具,以广泛测量整体肿瘤内的微生物负荷(ITMB)。有趣的是,将该工具应用于4种肿瘤类型(胃、结直肠、乳腺和子宫)的TCGA数据,发现在与肠道相关的胃和结直肠肿瘤中高ITMB与多种免疫途径相关。
此外,高ITMB与激活的肥大细胞增加和静止肥大细胞减少相关。这些结果通过16S测序和IHC实验得到了验证。通过将抗生素直接注入MC38肿瘤中来调节肿瘤内细菌,降低了肥大细胞水平,而相反地,通过局部抗体阻断肥大细胞导致微生物数量显著增加,表明宿主与侵入性微生物之间存在相互作用。通过研究这些变化是否影响ICB疗法,两种免疫治疗敏感肿瘤(MC-38和E0771)中抗生素的直接肿瘤内注射(主要在肿瘤边缘)降低了ICB反应,表明肿瘤内微生物对ICB反应具有重要意义。
此外,在一种本身对免疫治疗不敏感的胰腺肿瘤(KPC)中,通过消耗肥大细胞来增加微生物负荷,导致了免疫治疗应答的增强,而这种应答又被抗生素治疗所消除,表明由肥大细胞耗竭所增加的肿瘤内微生物是驱动这种应答的关键因素。总之,这项工作强调了肿瘤内微生物与免疫治疗结果的直接相关性。
5.肿瘤微环境代谢物塑造了癌症中T细胞的命运和功能
Greg M. Delgoffe – 匹兹堡大学,匹兹堡,宾夕法尼亚州
这是偏离讲者原计划的讲座,Greg Delgoffe介绍了一些关于肿瘤微环境(TME)的代谢特征及其与免疫抑制关系的新颖且令人兴奋的工作。肿瘤细胞改变其代谢方式,这反过来影响其直接环境,即TME的间质液的代谢组成。
长期以来人们所熟知的例子包括较高的氧气消耗,导致缺氧和活性氧物质的积累,以及较高的糖酵解速率,导致低血糖和乳酸积累。多位研究者已经证明,这些变化会影响局部T细胞生物学 – CD8+ T细胞因缺氧而耗竭,CD4+ T细胞因葡萄糖减少而向调节性细胞分化。然而,尚缺乏直接将特定代谢物变化与TME中T细胞变化联系起来的研究。
Delgoffe和他的合作者通过对小鼠KPC(KrasG12Dp53f/fPdx1cre)肿瘤的肿瘤间质液(TIF)的代谢组成进行定量表征,生成基于TIF的化学定义培养基(可以非常特异性地进行配方的修改),并直接分析T细胞对这种变化的表型反应来解决这个问题。初步实验表明,在正常培养基(反映正常外周)中活化的T细胞,转移到TIF培养基(反映肿瘤)后,如果在转移后不久重新刺激,仅显示出轻微的抑制。然而,在TIF培养基中长时间暴露后,重新刺激前,PD-1逐渐上调,多细胞因子产生减少,细胞生长速度显著减缓,即使在正常培养基中重新刺激T细胞,也表现出稳定的抑制性变化。
为了确定TIF培养基中可能缺失的物质,将TIF培养基与血浆进行定量比较,发现多种被耗尽的代谢物。补充实验确定了精氨酸是能够挽救T细胞PD-1和增殖表型的关键代谢物,但不能恢复多细胞因子产生。接下来,研究人员将重点放在了相对于血浆在TIF培养基中积累的物质上,他们确定了多个有趣的候选物质,但将研究重点放在了磷酸乙醇胺(pEtn)上,这是一种从乙醇胺到磷脂酰乙醇胺(PE)的途径上的代谢物,PE是细胞膜的丰富脂质成分。肿瘤细胞经常降低ECT/Pcyt2酶的表达,该酶是将pEtn最终转化为PE所需的。
令人惊讶的是,将pEtn加入正常培养基中的T细胞可重现T细胞功能障碍状态。进一步的分析将T细胞的代谢影响追溯到T细胞代谢的重编程,使其对pEtn产生依赖性。将从乙醇胺到PE的途径中的其他代谢物加入正常培养基中也重现了T细胞功能障碍,这表明在这些细胞中过量产生的PE是功能障碍的根本原因。最终,代谢重编程的T细胞用尽了二酰甘油(DAG)将pEtn代谢为PE,因此耗尽了T细胞受体信号通路所需的这一关键的第二信使,导致T细胞功能障碍。
恢复肿瘤细胞中pyct2的表达(以消除培养基中pEtn的积累)恢复了完全的T细胞功能,并导致肿瘤大小减小。作为一种更易处理的治疗方法,使用肝脏酶PEMT将T细胞中的多余PE转化为磷脂酰胆碱同样挽救了T细胞功能。作为一个附带的和一般的警示,PMA经常用于刺激T细胞,包含DAG类似物,因此使用PMA刺激可能掩盖代谢诱导的T细胞功能障碍。

加入读者交流群~
(添加请备注单位姓名)

关注本公众号~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏