1.个性化癌症疫苗mRNA-4157与帕博利珠单抗(pembrolizumab)联合应用于切除后高风险黑色素瘤患者的疗效与安全性:来自随机开放标签的II期临床试验mRNA-4157-P201/Keynote-942
Jeffrey S. Weber – 纽约大学朗格尼医学中心,纽约
过去十年,新抗原作为真正的肿瘤特异性、免疫原性且安全的疫苗靶点的出现,为癌症疫苗领域注入了新的活力,尤其是在利用肿瘤相关抗原的大型试验令人失望之后。基于新抗原的疫苗能激发强烈、持久的T细胞应答,甚至引发表位扩散,这是疫苗活性的关键标志。意识到检查点阻断抗体现已成为多种疾病(如高风险黑色素瘤)的标准治疗,但仍需在应答率和耐久性方面进行改进,Jeffrey Weber描述了一项随机II期临床试验的非常鼓舞人心的结果,该试验将单独的检查点治疗(帕博利珠单抗)与个性化新抗原mRNA基因癌症疫苗(mRNA-4157)在切除后高风险黑色素瘤患者中的应用进行了比较。
利用患者肿瘤和正常样本的核酸测序来识别患者特异性突变,采用先进的算法选择有前景的新抗原靶点,以及一个集成的制造过程来为每个患者准备编码(主要是)34个个性化新抗原靶点的mRNA,157名患者被随机分为(2:1)接受疫苗加检查点联合治疗或单独检查点治疗每三周一次。联合治疗安全性高,与单独使用帕博利珠单抗相比,轻度AEs增加,表现为“典型的COVID疫苗”反应。
值得注意的是,联合治疗在无复发生存期(RFS)上显著提高(单侧p=0.026),风险比为0.56,随着时间推移,复发风险降低了44%。RFS曲线在约9个月时开始分离,18个月的RFS在联合治疗组为79%,对照组为62%。在PD-L1状态的患者中,联合治疗组的改善独立于PD-L1状态,有迹象表明在PD-L1较低的患者中效果更大。Ryan Sullivan提供的独立数据表明,这也独立于肿瘤突变负荷。根据这些结果,计划于2023年启动III期研究,并扩展到其他免疫治疗响应组织学类型,如非小细胞肺癌(NSCLC)。
2.个性化mRNA新抗原疫苗治疗胰腺癌
Vinod P. Balachandran – 纽约纪念斯隆凯特琳癌症中心
Vinod Balachandran研究胰腺导管腺癌(PDAC),这是典型的免疫学冷肿瘤,具有低突变负荷、最小的T细胞浸润和对免疫治疗的抵抗。然而,约9%的PDAC肿瘤是热的,这类肿瘤的患者生存期较长。为了确定能最有效地引发初次应答、扩增预先存在的应答或两者兼而有之的新抗原,Balachandran及其同事开发了一种评估新抗原质量的模型,通过预测MHC结合、潜在TCR反应和已知病毒抗原肽相似性来估算“自体”和“非自体”。有趣的是,新抗原质量比新抗原数量更能预测患者生存期,而且在胰腺癌长期生存者的血液中,即使在10年后仍能发现针对高质量新抗原的特异性T细胞。
研究团队还发现,在长期生存者复发肿瘤中,高质量新抗原可能被编辑,自发产生高质量新抗原可能导致新抗原特异性T细胞增多,从而延迟肿瘤复发。考虑到几乎所有PDAC都携带有不同预测免疫原性的新抗原库,Balachandran及其同事想知道RNA疫苗是否可以用来激发初次应答。在一项合作研究中,他们为胰腺癌开发了个性化的mRNA疫苗。在I期试验中,患者接受手术治疗,然后在第6周开始接受阿特珠单抗治疗,第9周开始接受8次连续的个性化癌症疫苗治疗,第21周开始接受标准化疗,最后在第46周进行晚期补充。尽管这项试验受到了COVID-19大流行的影响,但在接受阿特珠单抗治疗的19名患者中有16名继续接受疫苗治疗,证明了在手术后生成和给予定制疫苗的可行性。
通过使用主要的ELISpot分析和确认性TCR测序CloneTrack测试来监测疫苗诱导的T细胞应答,结果显示疫苗接种后的应答强烈且持久,即使在化疗后也能维持。根据疫苗诱导的外周血克隆轨迹对克隆进行聚类,表明mRNA疫苗扩增的多克隆T细胞库包括在疫苗接种前无法检测到的克隆,且与抗PD-L1扩增的库有所不同。特别是在疫苗增强剂后,疫苗诱导的克隆扩增得到进一步加强,而PD-L1诱导的克隆则没有。
此外,研究人员发现,疫苗扩增的克隆在接种前收集的肿瘤中没有发现,这表明疫苗可能在引发初次应答。进一步分析发现,许多在外周血扩增的T细胞克隆实际上是新抗原特异性的,即使在总克隆扩增较少的患者中也是如此。对于显示出初次ELISpot活性和确认性克隆扩增的患者,将其归类为mRNA新抗原疫苗应答者。
总体而言,mRNA疫苗在50%的PDAC患者中诱导了T细胞应答,其中许多应答都是显著且持久的。在中位随访18个月后,应答者尚未达到中位无复发生存期,而非应答者的中位无复发生存期为13.4个月。阿特珠单抗治疗、标准预后变量差异(淋巴结状态或切除边缘)、化疗周期或原发肿瘤中的T细胞密度与复发之间没有类似的相关性。
考虑到非应答者可能对mRNA疫苗的适应性较低,研究人员将患者对COVID-19疫苗的应答进行了比较,发现癌症疫苗应答者和非应答者对COVID-19疫苗的应答相似,排除了基线免疫适应性作为影响因素。然而,他们发现,应答者具有更多的克隆突变和更高质量的新抗原。
在一个临床案例中,Balachandran描述了一位患者,他似乎有转移的证据,还有一个可疑的肝脏病变,后来证实是疫苗扩增的T细胞克隆的淋巴样聚集体,在后续的影像检查中消失了。这一结果可能表明疫苗诱导的免疫对微转移的控制。展望未来,Balachandran及其同事将进行该疫苗策略的二期临床试验,并正在考虑将此治疗扩展至其他对检查点阻断剂不敏感的癌症。
3.T细胞特异性、表型和动态:对癌症疫苗的影响
Catherine J. Wu – Dana-Farber癌症研究所,波士顿,MA
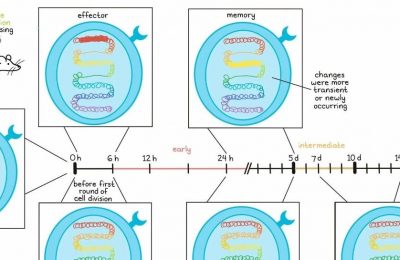
在来自四名黑色素瘤患者的数据中评估TIL景观时,Wu及其同事使用聚类分析绘制了不同的CD8+T细胞表型,并关注了两个最大的种群:耗竭效应细胞和非耗竭记忆细胞。从这些组中的主导克隆型中重建TCR,研究人员观察到耗竭的T细胞比非耗竭的记忆细胞具有更高的肿瘤特异性,而非耗竭的记忆细胞则更倾向于病毒特异性。CD4+T细胞也可以划分为不同的表型,分为耗竭、非耗竭记忆或Tregs。有趣的是,Tregs中观察到最高的肿瘤特异性。四名评估患者中的每一名都显示出非常不同的抗原特异性剖面,显示了对黑色素瘤相关抗原(MAA)、新抗原和病毒抗原的多种特异性,其中新抗原特异性TCR与MAA特异性TCR相比具有更高的亲和力。除黑色素瘤外,研究人员在肾细胞癌(RCC)和头颈鳞状细胞癌(HNSCC)的数据中观察到类似的聚类结果。
作为2023年AACR学院新任研究员的Catherine Wu在讲话开始时讨论了癌症疫苗如何有潜力应对抗肿瘤免疫面临的一系列挑战,从肿瘤异质性和进化到免疫不应答,因为癌症疫苗既可以利用已存在的肿瘤免疫,也可以诱导新的应答。癌症疫苗开发中一个重要的障碍是识别肿瘤特异性TCR,它们在原生态环境中相对稀少,并与肿瘤微环境中的旁观者T细胞混合。对于Wu及其团队,识别相关肿瘤特异性T细胞涉及综合考虑TCR序列和T细胞表型,这基于单细胞测序技术的进步以及通过质谱和其他技术提高潜在靶抗原识别。这种联系是通过使用组合染料标记系统实现的,该系统允许对大量TCR候选者进行高通量筛选,以确保对肿瘤和靶抗原的特异性。
从不同角度评估肿瘤反应性T细胞,Wu及其同事利用基于Slide-seq的技术研究了肿瘤微环境中细胞之间的空间关系,该技术可以在组织切片中分析RNA、DNA和TCR。使用这个系统,研究人员能够确定与肿瘤边缘相比在肿瘤内被耗竭或富集的TCR。通过将Slide-seq与人类黑色素瘤中的TCRseq结合,研究人员可以分析样本的多个区域,并识别出第三级淋巴结构。一个有趣的样本由两个叶子组成,显示出一个仅限于一个叶子的TCR,表现出空间偏见。观察其环境关系,这与趋化因子CXCL10呈正相关,与先前与免疫治疗反应相关的MGST1呈负相关。
总体而言,从黑色素瘤的TIL景观来看,Wu认为对免疫治疗最有益的T细胞特异性不幸已经耗尽。为了寻找恢复或替代它们的方法,Wu转向了识别个性化新抗原和制备个性化癌症疫苗。在2017年两个独立小组的临床研究中,针对个性化新抗原的肽疫苗和RNA疫苗在与检查点阻断剂联合使用时都显示出安全性、可行性、免疫原性和令人鼓舞的疗效。
总体而言,从黑色素瘤的TIL景观来看,Wu认为对免疫治疗最有益的T细胞特异性不幸已经耗尽。为了寻找恢复或替代它们的方法,Wu转向了识别个性化新抗原和制备个性化癌症疫苗。在2017年两个独立小组的临床研究中,针对个性化新抗原的肽疫苗和RNA疫苗在与检查点阻断剂联合使用时都显示出安全性、可行性、免疫原性和令人鼓舞的疗效。

加入读者交流群~
(添加请备注单位姓名)

关注本号~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏