OncoLab实验室 文献阅读 Hepatology:ALDOB/KAT2A相互作用通过表观遗传调控TGF-β表达和T细胞功能促进肝细胞癌发生
杂志名称:Hepatology 发表日期:2023.12.05 DOI:10.1097/HEP.0000000…
杂志名称:Hepatology
发表日期:2023.12.05
DOI:10.1097/HEP.0000000000000704.
PubMed:https://pubmed.ncbi.nlm.nih.gov/38051951
影响因子:13.5
肿瘤细胞与免疫细胞之间的相互作用使肿瘤细胞能够逃避免疫监视,并影响免疫疗法的反应。先前的研究发现,在肿瘤细胞中,糖解酶果糖-1,6-二磷酸醛缩酶B(ALDOB)的表达下调,通过影响代谢编程促进了肝细胞癌(HCC)的发生。然而,肿瘤细胞中ALDOB的表达如何影响HCC肿瘤微环境仍不清楚。
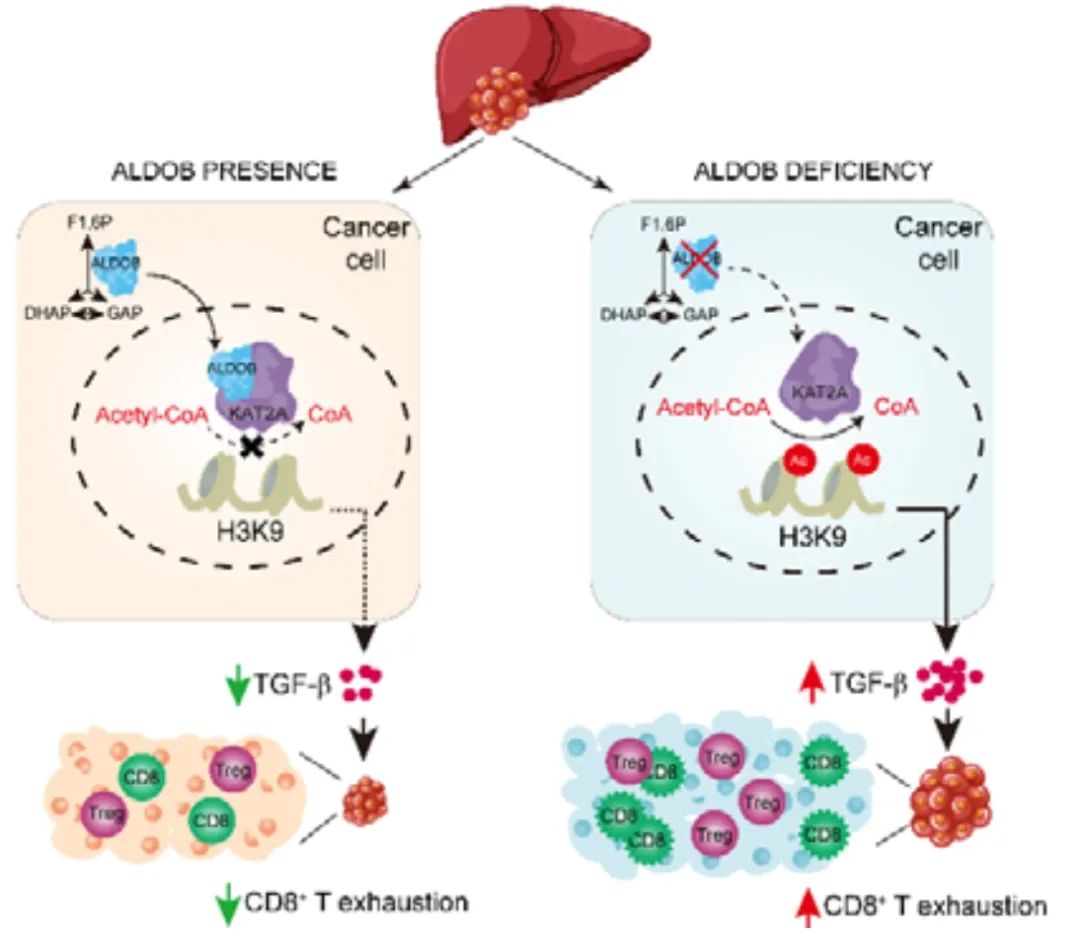
作者发现,在人类HCC肿瘤组织中,ALDOB的表达下调与CD8+ T细胞的浸润呈负相关,但这些细胞呈现耗竭状态。在特定敲除肝脏ALDOB的小鼠或敲低ALDOB的皮下肿瘤模型中观察到了类似的现象。此外,肿瘤细胞中ALDOB的缺失上调了TGF-β的表达,从而增加了调节性T细胞的数量,并削弱了CD8+ T细胞的活性。一致地,ALDOB表达低和TGF-β表达高的HCC患者总体生存率最差。更重要的是,同时阻断TGF-β和PD-1的抗体可以叠加抑制小鼠中由ALDOB缺失引起的肿瘤发生。进一步的机制实验表明,ALDOB进入细胞核并与赖氨酸乙酰转移酶2A(KAT2A)相互作用,导致抑制H3K9乙酰化,从而抑制TGFB1转录。同样,通过小分子抑制剂抑制KAT2A活性,能够抑制TGF-β和HCC。
该研究揭示了一种新的机制,通过这种机制,肿瘤细胞中的代谢酶通过表观遗传调节TGF-β信号传导,从而使癌细胞能够逃避免疫监视并影响其对免疫疗法的反应。
本研究围绕肝细胞癌(HCC)中肿瘤细胞与免疫系统的复杂相互作用,揭示了糖解酶ALDOB在肿瘤微环境中的新作用及其对T细胞功能的影响。研究表明,肿瘤细胞中ALDOB的下调与CD8+ T细胞的功能耗竭密切相关。ALDOB缺失还上调了促肿瘤因子TGF-β的表达,进一步抑制免疫细胞的活性,并提高了免疫抑制性Treg细胞的数量。
该研究的创新之处在于它揭示了ALDOB与KAT2A相互作用的分子机制,这一发现对于理解T细胞如何在肿瘤微环境中被调节具有重大意义。ALDOB通过进入细胞核与KAT2A相互作用,进而影响了H3K9的乙酰化状态,对TGFB1的转录产生抑制作用,这一过程对肝细胞癌的发生和发展具有关键影响。此外,研究还发现低ALDOB和高TGF-β表达的HCC患者总体生存率最差,为临床提供了新的生物标志物。
总体而言,这项研究不仅为我们提供了肝细胞癌发生的新的表观遗传机制,而且还为开发针对这种机制的潜在治疗策略提供了科学依据。通过这些发现,我们能够更好地理解肝细胞癌中的代谢重编程如何影响肿瘤免疫微环境,为免疫治疗提供了新的靶点,有望推动肝癌治疗策略的进步。
OncoLab公众号已增加期刊查询功能,SCI期刊可查询期刊名称缩写、ISSN刊号、近五年影响因子、最新WOS的JCR分区、最新中科院分区以及中科院期刊预警信息;
中文期刊可检索CSCD核心、北大中文核心、科技核心收录情况;
在公众号对话框发送杂志名称即可快速检索,支持模糊检索,欢迎使用!

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab