29.1 引言
29.1.1 小鼠和人源(鼠源和人源)Treg细胞的特征
调节性T细胞(Treg)在维持自身免疫耐受和免疫系统的动态平衡中起着至关重要的作用。这类细胞通过多种机制抑制抗肿瘤免疫反应,助推肿瘤逃避免疫监视,从而有利于肿瘤的生长和扩散。
Treg的关键标志是转录因子FoxP3的表达,它对Treg的发育和功能至关重要。在小鼠中,Treg细胞会持续表达FoxP3,而在人类中,Treg的FoxP3表达则不必然,且激活的传统T细胞(Tconv)在某些条件下也可能暂时表达中等水平的FoxP3。因此,人类Treg的识别更为复杂,涉及多种标志物的组合。通常情况下,人类Treg可通过流式细胞术被识别为CD3+、CD4+、高表达CD25且低表达CD127的细胞。
此外,无论是在小鼠还是人类中,Treg均能表达多种抑制性受体,如CTLA-4、PD-1和Lag-3。它们还表达一些共刺激受体,如糖皮质激素诱导的肿瘤坏死因子相关蛋白(GITR)和OX40(也称CD134),以及其他重要的表面标记物,如可诱导共刺激分子(ICOS)、胞外核苷酸酶CD39和CD79。这些表面分子的表达赋予Treg其独特的调控功能,使其在免疫系统中发挥关键作用。
29.1.2 Treg的免疫抑制活性
调节性T细胞(Treg)的免疫抑制活性是其关键功能,主要通过以下四种机制实现:
1. 细胞因子的释放:Treg能够分泌多种具有免疫抑制作用的细胞因子,包括白细胞介素-10(IL-10)、转化生长因子β(TGF-β)和IL-35。这些因子能有效抑制炎症反应和促进免疫耐受。
2. 细胞毒性作用:Treg也可以通过释放细胞毒性分子如颗粒酶A、颗粒酶B和穿孔素,直接杀伤靶细胞,这一机制主要针对激活的免疫细胞,以减少免疫反应。
3. 代谢干预:Treg通过表面分子如CD25(高亲和力的IL-2受体α链)、CD39和CD73等外切核苷酸酶,干预其他T细胞的代谢过程。这些分子的作用主要是降低IL-2的可用性和增加细胞外腺苷的浓度,从而抑制T细胞的活化和增殖。
4. 调节树突状细胞功能:通过共抑制受体如CTLA-4或LAG-3,Treg能够抑制树突状细胞(DC)的活性。这种作用不仅减弱了树突状细胞对效应T细胞的激活能力,还增强了免疫耐受环境的建立。
这些机制的协同作用使得Treg在调控免疫反应、维护机体免疫稳定中发挥着不可或缺的作用。
29.1.3 外周血和肿瘤微环境中Treg的表达水平对肿瘤预后的影响
调节性T细胞(Treg)在维护自身耐受性、预防自身免疫病和控制慢性炎症中发挥关键作用。然而,在肿瘤疾病的背景下,Treg的作用较为复杂,其在不同类型的肿瘤中的表达与预后之间的关系各异。
研究显示,Treg在多种肿瘤中的高表达与不良预后相关,包括胰腺癌、肝癌、肺癌、乳腺癌和卵巢癌。在这些情况下,Treg可能通过抑制有效的抗肿瘤免疫反应,帮助肿瘤细胞逃避免疫系统的监控,从而促进肿瘤生长和扩散。
另一方面,一些证据表明,Treg在某些癌症类型如滤泡性淋巴瘤和头颈癌中可能发挥保护作用,这可能与这些肿瘤的特定免疫环境有关。然而,对于肛门鳞状细胞癌,目前的研究表明Treg的表达水平似乎对患者的存活率没有显著影响。
这些发现强调了在不同肿瘤微环境中,针对Treg的潜在治疗策略需要因肿瘤类型而异,以优化治疗效果和预后。
29.1.4 Treg在肿瘤微环境中的募集
在肿瘤微环境中,Treg的招募是一个复杂而关键的过程。通常,Tregs被吸引到肿瘤部位,以参与调节肿瘤周围的免疫反应。这一过程主要由恶性细胞和先天免疫细胞分泌的趋化因子驱动。在此过程中,一些关键的趋化因子-趋化因子受体通路起着核心作用,包括CCL17/CCL22与其受体CCR4,以及CXCL12与其受体CXCR4。
此外,相比于源自外周血或健康组织的Treg,肿瘤浸润性(TI)Treg在肿瘤微环境(TME)中表现出更强的免疫抑制功能。这种增强的抑制能力可能是由于它们在肿瘤微环境中的特定激活状态。在这种环境下,Treg可能接受到额外的刺激信号,如局部细胞因子的浓度变化或与其他细胞类型的相互作用,这进一步强化了它们的功能并加剧了免疫抑制效果。
因此,了解Treg在肿瘤微环境中的募集和功能机制对于开发针对Treg的新型癌症治疗策略具有重要意义。这不仅可以帮助我们更好地控制肿瘤的免疫逃逸机制,还可能为免疫治疗提供新的靶点。
29.1.5 靶向Treg的肿瘤治疗方法
由于Treg细胞在促进肿瘤生长、发展及免疫逃逸中扮演关键角色,它们成为癌症治疗中潜在的靶点。针对Treg的治疗策略主要集中在两大方向:耗竭Treg以及抑制其功能。
首先,使用针对CD25的特异性抗体是一种常见的靶向Treg的策略,因为CD25是Treg表面的主要标记物之一。然而,这种方法的局限性在于,激活的CD4+ 和CD8+ T细胞同样表达CD25,因此这类治疗可能会影响到这些具有重要免疫功能的细胞。
为了更加精确地靶向Treg而不影响其他免疫细胞,当前研究正在探索新的疗法。这包括开发新的药物,以特定地抑制Treg的免疫抑制活性,或通过靶向与Treg迁移至肿瘤微环境相关的趋化因子及其受体途径来限制其在肿瘤中的集聚。
此外,一些原本用于治疗其他疾病的药物,如抗血管生成药物和酪氨酸激酶抑制剂,也正在被研究是否能有效抑制Treg的功能。这些药物的重新评估可能为癌症治疗带来新的方向。
在本章中,我们将详细介绍这些策略的研究进展,包括在小鼠肿瘤模型和人类临床试验中的应用情况。这些信息将为未来癌症治疗提供重要的科学基础和临床指导。
29.2 小剂量化疗所致的Treg耗竭
近年来,传统的观念认为抗癌化疗主要通过直接杀死肿瘤细胞来发挥作用,并通常会抑制免疫系统。然而,新的研究数据显示,某些化疗药物也能够引发免疫介导的抗癌反应。
自21世纪初以来,环磷酰胺(CTX)、紫杉醇(PTX)和氟达拉滨(FDB)等常规化疗药物开始被用于晚期耐药癌症患者的低剂量长期给药计划中。这种所谓的节律化疗旨在通过最小的毒副作用减少肿瘤血管生成。
在这一过程中,研究表明这些化疗药物能够耗竭肿瘤微环境(TME)及外周血中的调节性T细胞(Treg),从而损害这些免疫抑制细胞的功能。因此,节律化疗不仅有助于抑制肿瘤生长,还能恢复肿瘤浸润性淋巴细胞(TIL)的抗肿瘤功能。
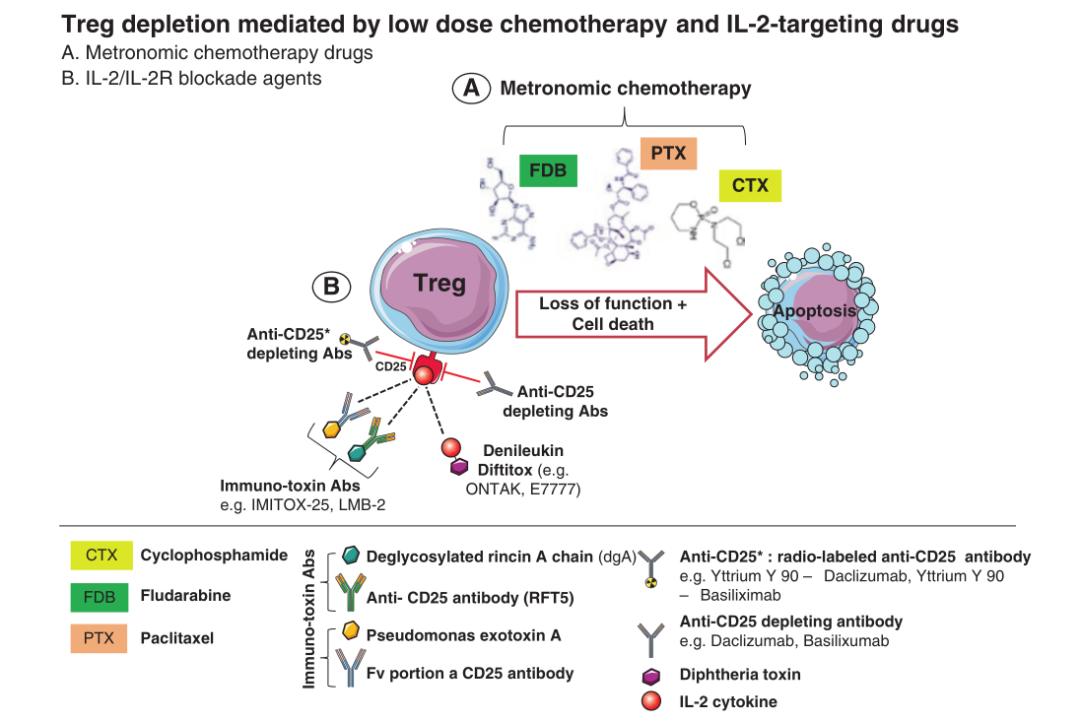
Fig 29.1 描述了小剂量化疗和IL-2/IL-2R靶向药物如何介导调节性T细胞(Treg)的耗竭:(A) 小剂量口服节律化疗:使用环磷酰胺(CTX)、紫杉醇(PTX)和氟达拉滨(FDB)等药物,在周期性低剂量给药的方案中,可以显著降低Treg的数量。这种策略最小化了毒副作用,同时有效地抑制了Treg的免疫调节功能,促进了免疫系统对肿瘤的攻击。(B) IL-2/IL-2受体阻断剂:抗CD25抗体Daclizumab和Basiliximab通过介导抗体依赖性细胞介导的细胞毒性(ADCC)或补体依赖性细胞毒性(CDC)机制,能够引发Treg细胞的死亡。此外,还有两种基于CD25的免疫毒素抗体正在人类癌症治疗中进行测试:IMITOX-25(RFT5-DGA),这是一种将脱糖化蓖麻毒素A与CD25抗体RFT5相连的药物;以及LMB-2,一个将CD25抗体的Fv部分与假单胞菌外毒素A片段结合的融合蛋白。另一药物,Denileukin diftitox(Ontak),因含有IL-2成分,能够与高亲和力的IL-2受体(CD25)结合,促使Treg的快速内吞和细胞凋亡。
Ghiringhelli及其同事首次证明,与未经治疗的动物相比,单剂量的环磷酰胺(CTX)能显著耗竭荷瘤大鼠体内的Tregs。这一发现在晚期实体瘤患者中的临床前研究中得到进一步证实,研究结果显示外周血中的免疫抑制Tregs数量的选择性急剧减少,有助于改善肿瘤的发生和进展。此外,这些研究将节律化疗法,特别是使用CTX,在抗癌免疫治疗前,作为降低肿瘤诱导的免疫耐受性的有效方法。
在对难治性和转移性晚期乳腺癌患者进行的研究中,葛英子等人监测了每天50毫克口服CTX(为期三个月)对循环中Treg数量和功能的影响,以及其对肿瘤特异性T细胞反应的免疫学效应。研究发现,乳腺癌患者中Treg的短暂耗竭与T细胞的活性增强相关,并与良好的临床结果有关。
在许多小鼠和人类癌症研究中,疫苗接种前通过低剂量化疗耗竭Treg显著提高了患者的总生存期(OS),并诱发了有效的抗肿瘤免疫反应。例如,在一项针对肾癌的随机II期研究中,单剂量CTX的使用降低了Tregs的数量并诱导了特异的免疫反应,这与较长的生存期相关。
然而,不是所有研究都报告了正面结果。在一项I/II期临床试验中,转移性去势抵抗前列腺癌(MCRPC)患者接受了DC疫苗和长期的化疗药物(节律化环磷酰胺、多西紫杉醇和泼尼松)治疗。虽然观察到外周血中Tregs显著下降,但目前还没有证据显示这与较好的生存期有显著关联。
值得注意的是,在一项I期临床试验中,49名转移性癌症患者(包括乳腺癌、肺癌、肾癌、胃癌、膀胱癌和前列腺癌)接受了BCG和CTX的联合治疗后,外周Tregs数量意外地增加。这种与预期相反的结果可能与给药方式的不同有关,例如在此研究中CTX是静脉滴注给药,而其他研究中通常是口服。
此外,Koumarianou及其同事的研究表明,即使是口服的节律化疗药物也能诱导Treg数量增加和免疫活性的抑制,这些影响在节律化疗中比在标准化疗中更为显著。
此外,Koumarianou及其同事的研究表明,即使是口服的节律化疗药物也能诱导Treg数量增加和免疫活性的抑制,这些影响在节律化疗中比在标准化疗中更为显著。
29.3 IL-2受体(IL-2R)诱导的Treg耗竭
T调节性T细胞(Treg)特征性表达高亲和力的IL-2受体α链(CD25)。这些高亲和力的IL-2受体使Treg能够捕获环境中的IL-2,限制传统T细胞(Tconv)的可用IL-2,从而阻碍它们的扩张和活化。在癌症治疗中,利用IL-2/IL-2R轴来耗竭Treg,有助于恢复抗肿瘤免疫反应。
29.3.1 抗CD25抗体治疗(如达利珠单抗和巴利昔单抗)
Daclizumab是一种人源化的针对人CD25 IgG1-κ的单抗。给药时耐受性良好,不会引起严重的副作用。它最初于1997年被食品和药物管理局(FDA)批准用于预防肾移植排斥反应,现在在几个癌症临床试验中用于进行Tregs耗竭测试(Fig 29.1b)(Table 29.1)。
在第一组研究中,研究人员探讨了在转移性黑色素瘤患者接受DC疫苗接种前,Daclizumab用于耗竭癌症Treg的效果。研究使用了Daclizumab的单一低剂量(0.5 mg/kg),发现该药物能有效耗尽患者外周血中表达CD4+、高表达CD25和FoxP3的T细胞。然而,约30天后,随着Daclizumab的清除,观察到Tregs的再次出现。值得注意的是,接受Daclizumab预处理的患者相较于仅接种疫苗的患者,其疫苗诱导的效应性T细胞特异性反应效果较差。
在另一项关于转移性乳腺癌的试验中,Rech等研究人员评估了Daclizumab与多肽疫苗联合使用的疗效。结果表明,Daclizumab能显著并持续地耗尽外周血中的Tregs,并有效增强了疫苗诱导的特异性T细胞反应。这些发现强调了在癌症治疗中,通过靶向Treg来调节免疫响应的潜力,尽管其效果可能受多种因素的影响。
这些研究表明,抗CD25单克隆抗体Daclizumab能有效诱导癌症患者中Treg的耗竭。Treg的减少可能导致体内表达CD25的T细胞被激活,而剩余在体内的Daclizumab抗体可能对这些新激活的CD25+ T细胞产生不利影响。实际上,Daclizumab的半衰期超过四周,这可能解释了Jacobs等人观察到接种疫苗后患者T细胞特异性反应较低的现象。
另一种抗CD25单克隆抗体,嵌合抗体Basiliximab,也在癌症治疗中评估其对Treg的耗竭效果(Fig 29.1b)。Basiliximab目前正在针对胶质母细胞瘤、急性髓系白血病、霍奇金淋巴瘤和非霍奇金淋巴瘤患者的多个I期临床试验中进行测试。这些试验旨在探索Basiliximab在不同类型癌症治疗中的潜在效用和安全性(Table 29.1)。

Table 29.1 CD25-癌症临床试验中的靶向药物
29.3.2 Denileukin Diftitox (ONTAK®)
Denileukin diftitox(DD)/Ontak 是一种由白喉毒素的结构域和IL-2构成的基因工程重组融合蛋白。这种蛋白质包含IL-2成分,使其能够与高亲和力的IL-2受体(IL-2R)结合,促使细胞迅速内吞并在40-72小时内引发细胞凋亡(Fig 29.1b)。自1999年起,Ontak获得美国食品和药物管理局(FDA)的批准,用于治疗表达IL-2Rα链CD25的持续性或复发性皮肤T细胞淋巴瘤患者。自那时起,Ontak也被用于靶向表达CD25的Treg细胞的癌症治疗,以耗尽CD25+细胞群。到目前为止,Ontak已经用于治疗不同癌症、不同剂量和不同方案的Treg耗竭的许多临床试验,结果各不相同(Table 29.2)。
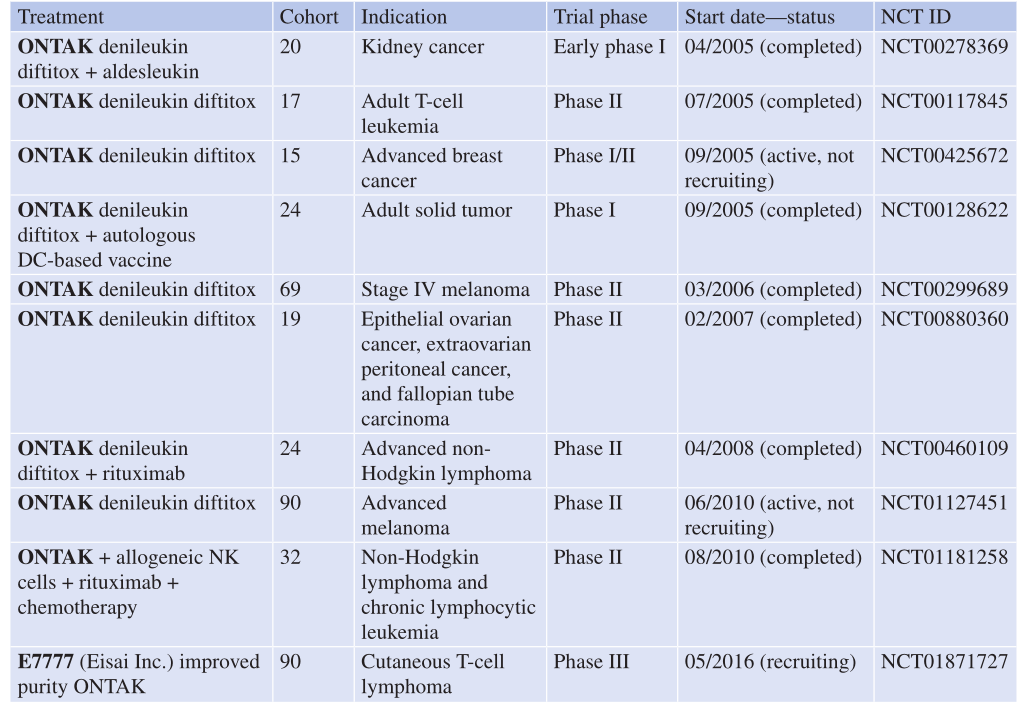
Table 29.2 癌症临床试验中的Ontak(代尼罗金地夫妥)
Ontak已经在多项临床试验中被用于治疗不同的癌症类型,试验中采用了不同的剂量和治疗方案,结果表现各异。在这些研究中,Ontak通常以单剂18μg/kg的剂量与树突状细胞(DC)或多肽疫苗联合使用。这些试验涵盖了治疗癌胚抗原(CEA)阳性的恶性肿瘤、转移性肾细胞癌(RCC)和转移性黑色素瘤。在这三项研究中,有两项报告指出在使用该剂量时CD4+CD25+FoxP3+ T细胞的数量未发生变化。然而,在肾癌的试验中,观察到高表达CD4+和CD25的Treg暂时耗尽,但对低表达CD25的T细胞和其他细胞群没有显著影响。
在针对转移性黑色素瘤使用Ontak进行Treg耗竭的几项试验中,有四项研究已被发表。这些研究显示,Ontak在一定条件下可以有效耗竭Treg。具体地,当以12μg/kg/d的剂量连续给药4天,或以5和18μg/kg/d的剂量连续给药3天时,Ontak能够瞬时耗竭Treg。然而,以单次注射18μg/kg的剂量或连续5天给药9和18μg/kg时,效果不佳。这表明,在黑色素瘤和其他类型的癌症治疗中,选择合适的Ontak剂量对有效耗竭Treg至关重要。
尽管在一些研究中观察到了Treg细胞的耗竭,但Ontak的临床效果并不总是如预期那样显著,有时甚至无明显治疗效果。这引发了关于Ontak可能对患者免疫系统有其他未被发现的不良影响的担忧。例如,在一项针对黑色素瘤患者的临床试验中,使用Ontak预处理来耗竭Tregs,随后接种DC疫苗。结果显示,Ontak预处理未能有效诱导针对肿瘤抗原的CD4+和CD8+ T细胞反应,从而未达到预期的临床疗效。研究还发现,Ontak的作用可能超出单纯的树突状细胞耗竭,它还可能作为一种强大的免疫调节剂,导致生成耐受性DC细胞。此外,Ontak未能有效诱导Treg的凋亡,也未提高患者的存活率。
最近,还启动了一项第三阶段试验,目的是评估改进纯度的Ontak(E7777)治疗持续性或复发性皮肤T细胞淋巴瘤(CTCL)的安全性和有效性,试验编号为NCT01871727。这项试验旨在进一步验证E7777在临床应用中的潜力和改进的疗效。
29.3.3 抗CD25免疫毒素抗体
在靶向CD25的免疫毒素抗体领域,存在两种主要的疗法:IMITOX-25(RFT5-DGA)和LMB-2。IMITOX-25是一种将脱糖基化蓖麻毒素A与CD25抗体RFT5结合的产品,该融合蛋白在细胞内化后通过抑制蛋白质合成诱导细胞死亡。而LMB-2则是一种将CD25抗体的Fv片段与假单胞菌外毒素A片段结合的融合蛋白,已知能够诱导caspase介导的细胞凋亡(Fig 29.1b)。这些免疫毒素能够在体内迅速(少于4小时)清除抗CD25抗体,并已在临床试验中进行了评估(Table 29.1)。然而,尽管CD25+ Treg细胞可被短暂耗尽,CD25− Treg亚群却得以存活,导致仅耗尽CD25+ Treg细胞并不足以显著增强对多肽疫苗的免疫应答。
综合考虑,Daclizumab、Ontak以及其他CD25+细胞耗尽剂在某些情况下已显示出在癌症患者中耗尽CD25+ Tregs的潜力。然而,这些疗法的效果有时受限于CD25并非只由Tregs特有表达这一事实。在一些试验中,这些疗法未能增强疫苗诱导的特异性免疫反应,可能与此相关。此外,CD25+ Treg在这些研究中的持续存在提示我们,开发更具Treg特异性的治疗策略或将这些疗法与其他Treg耗尽药物结合使用,可能会提供更加有效的治疗方案。
29.3.4 新兴的抗CD25抗体疗法
另一个关于针对CD25的治疗策略的缺陷是,全身性耗尽Tregs可能破坏外周的免疫平衡,并导致严重的副作用。为此,一种令人兴奋的新一代抗CD25抗体已被开发,能够选择性地耗尽肿瘤内的Treg。
近期,佐藤等人开发了一种创新的方法,他们将抗CD25 F(ab‘)2片段与光激活硅酞菁染料(IRDye 700DX)结合。这种结合物被设计用于在荷瘤小鼠中选择性地消耗肿瘤内(TI)Tregs。通过注射这种光活化抗体后,将肿瘤局部暴露于近红外光,激活IRDye 700DX,从而实现肿瘤微环境(TME)内的Tregs耗尽,而不影响周围细胞或系统中未暴露于近红外光的CD25+ Tregs。实验结果显示,肿瘤部位的85% CD4+CD25+ Tregs在30分钟内被耗尽。此外,研究还观察到,近红外治疗后,CD8+ T细胞、NK细胞以及抗原提呈细胞迅速激活。这种针对局部Treg的耗尽策略不仅促进了肿瘤的消退,还显著延长了小鼠在仅一次治疗后的存活时间。
此外,已经有FDA批准使用的人源化CD25抗体,如daclizumab和basiliximab,减少了将这种新疗法转化为人类临床试验的障碍。并且,目前正在进行一项与IRDye 700DX结合的抗表皮生长因子受体(EGFR)的I期人体研究,针对无法手术的头颈癌患者(NCT02422679)。这些进展使得近红外光免疫疗法策略有望在临床试验中为癌症患者提供治疗新方向。
29.4 干扰Treg细胞向肿瘤的迁移
29.4.1 CCL22-CCR4通路阻断
CCR4-CCL22途径是肿瘤内Treg招募的主要机制。实际上,Treg的运输和渗透到不同类型的肿瘤中,似乎与肿瘤细胞或浸润性巨噬细胞产生的CCR4配体(CCL17和CCL22)的表达水平有关(Fig 29.2a)。此外,CCR4主要在高表达FoxP3和CD25、CD45RA−的细胞上表达,这些被称为效应型Tregs(ETregs),在肿瘤浸润性(TI)FoxP3+ T细胞中占据主导地位。
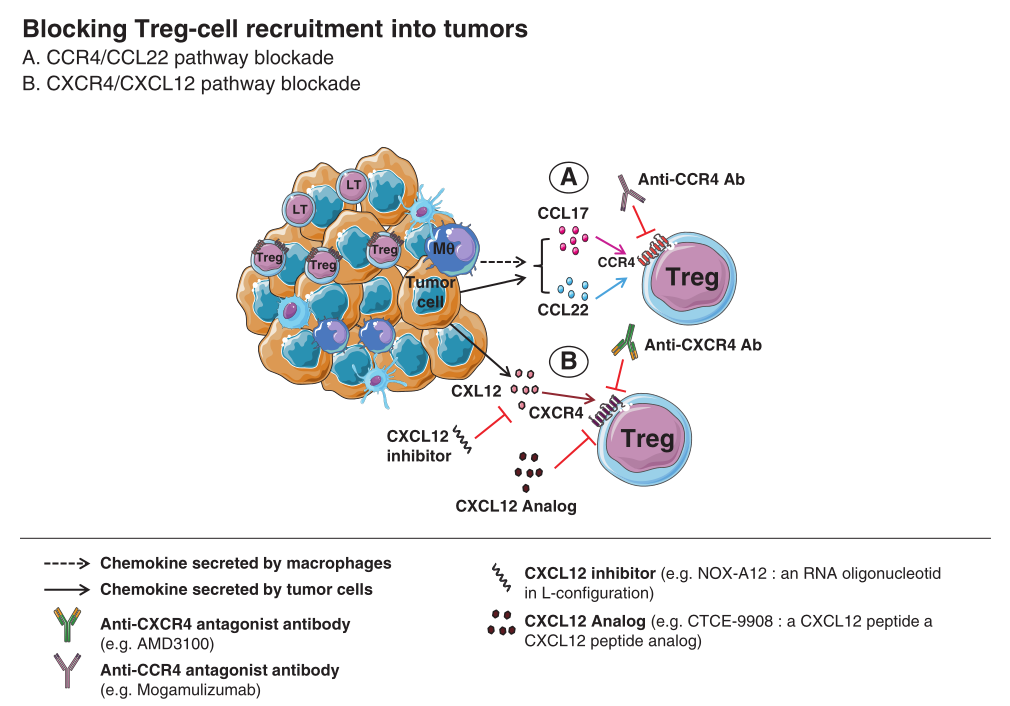
Fig 29.2 描述了如何阻断Treg细胞向肿瘤的募集。在肿瘤微环境中,恶性肿瘤细胞和免疫细胞(例如巨噬细胞)分泌的趋化因子会吸引大量的Tregs到肿瘤区域。特别是CCL17/CCL22-CCR4(A)和CXCL12-CXCR4(B)这两条关键的趋化因子-趋化因子受体通路,是目标化疗的关键点,包括使用特异性拮抗剂单抗、趋化因子抑制剂及其类似物(这些治疗手段与趋化因子受体竞争性结合)。通过阻断这些关键的信号通路,可以有效地阻止Tregs向肿瘤大量迁移,从而可能促进肿瘤的消退。
在皮肤T细胞淋巴瘤(CTCL)的小鼠模型中,Ito等人使用了抗CCR4拮抗剂的单克隆抗体,并展示了通过自然杀伤(NK)细胞诱导的抗体依赖性细胞介导的细胞毒性(ADCC)可以显著耗尽TI Tregs。其他研究小组还表明,通过CCR4拮抗剂抑制表达Treg的CCR4群体足以打破对自发性乳腺肿瘤的免疫耐受,这突显了CCR4在Treg的免疫抑制功能中的重要作用。总体来说,这些研究结果为CCR4和CCL22拮抗剂的临床试验发展提供了理论基础,以阻断Treg细胞向肿瘤的迁移。
到目前为止,CCR4拮抗剂主要用于治疗表达CCR4的T细胞淋巴瘤,包括成人T细胞白血病-淋巴瘤(ATLL)、外周T细胞淋巴瘤(PTCL)和CTCL(Table 29.3)。
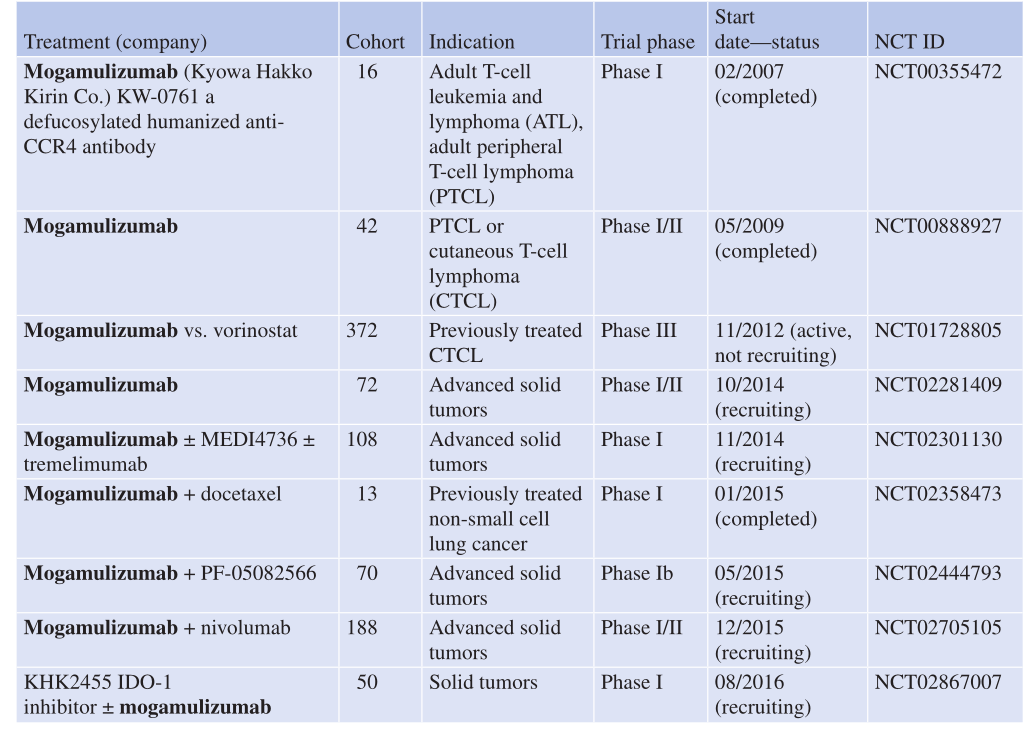
Table 29.3 CCR4-靶向抗体临床应用
Mogamulizumab(KW-0761)是一种针对CCR4(图29.2a)的脱糖人源化IgG1单抗,其设计目的是发挥强大的ADCC作用。它在I期和II期临床试验中显示出良好的治疗效果,尤其是在治疗预后不佳的CTCL中表现突出。
最初的I/II期多中心研究对莫伽慕珠单抗(Mogamulizumab)进行了剂量递增试验,以评估其作为单药治疗在已经接受过预治疗的外周T细胞淋巴瘤(PTCL)或皮肤T细胞淋巴瘤(CTCL)患者中的疗效。研究发现,即使在最低剂量0.1 mg/kg时,抗CCR4单克隆抗体也能有效耗尽循环中的CCR4+效应型调节T细胞(eTregs),并恢复抗原特异性细胞毒性T淋巴细胞(CTL)的反应。基于这些积极的初步结果,该研究组最近启动了一项III期试验,比较莫伽慕珠单抗和伏立诺(一种组蛋白去乙酰化酶抑制剂)在治疗CTCL中的无进展生存期(NCT01728805)。
此外,Sun等人的研究指出,与其他CCR4结合配体相比,在头颈部鳞状细胞癌(HNSCC)患者中,单核细胞的MCP-1是一种内源性CCR4结合配体,并特异性高表达。研究通过使用CCR4拮抗剂阻断MCP-1/CCR4信号,抑制Treg细胞的募集,发现这种方法可以抑制肿瘤生长并延长生存期。
自2014年以来,莫伽慕珠单抗已在晚期或转移性实体癌患者中进行了疗效评估。这些试验大多采用莫伽慕珠单抗与其他免疫治疗药物联合使用,包括抗PD-1、抗PD-L1、抗CTLA-4、抗4-1BB抗体以及吲哚胺2,3-双加氧酶(IDO)抑制剂,以探索其协同治疗效果(Table 29.3)。
29.4.2 阻断CXCR4-CXCL12通路
CXCL12(也称为基质细胞衍生因子-1,SDF-1)是一种主要由骨髓、淋巴结和炎症细胞分泌的趋化因子,负责引导表达CXCR4的Treg细胞迁移至特定组织。
CXCL12-CXCR4通路在许多人类癌症中扮演着关键角色,参与肿瘤细胞的进展、血管生成和转移过程,如黑色素瘤、卵巢癌、乳腺癌、小细胞肺癌和胃癌。因此,由于其与癌症转移和不良临床结果的关联,阻断CXCL12与CXCR4的相互作用或抑制其下游信号传导的治疗策略成为了研究的热点。
目前,多种针对CXCL12通路的药物正在开发中,包括AMD3100(也称为plerixafor),这是一种高度特异的CXCR4拮抗剂;CTCE-9908,一种能够与CXCR4竞争性结合的CXCL12类似物;以及Spiegelmer/NOX-A12,一种CXCL12抑制剂(Fig. 29.2B)。在这些药物中,AMD3100和CTCE-9908已被批准用于治疗白血病和骨肉瘤患者。
最近的研究还揭示了CXCL12-CXCR4通路在肿瘤对常规化疗和抗血管生成治疗发展耐药性中的潜在作用。为了克服这些耐药性,目前正在探索涉及阻断CXCL12通路的综合治疗策略。
尽管如此,目前针对CXCL12-CXCR4通路阻断对人类Treg细胞群体影响的研究尚不充分,需要进一步的科学探索来验证这些治疗策略的效果及其机制。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 罗佳佳
图文排版 | 潘君君 郭震远
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏