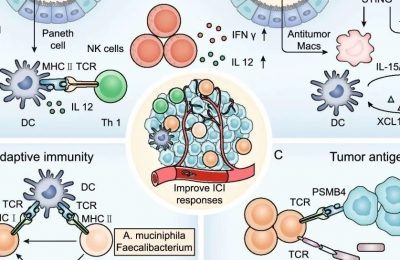
实体瘤往往会出现缺氧区域,这会触发肿瘤微环境 (TME) 中的细胞释放 ATP 和腺苷。ATP 通过其对 P2 嘌呤受体 (P2R) 的作用来发出促炎信号,进而抑制肿瘤细胞的生长。相比之下,腺苷对 P1 嘌呤受体 (P1R) 的激活往往会起到促肿瘤和抗炎的功能。
在已知的 P2 受体中,人们对P2X7R 进行了广泛的临床前和临床研究。P2X7R 表现出双向的功能表型;依赖于细胞外 ATP 的浓度和细胞类型,它可以促进或抑制肿瘤生长。
已知腺苷受体 A2AR 和 A2BR 的激活通过不同的免疫和非免疫细胞机制促进肿瘤生长和转移。在 TME 中,A2AR 的促肿瘤作用主要通过其对免疫细胞的激活来介导,而 A2BR 在肿瘤细胞上的表达被证明对肿瘤进展和转移至关重要。
外核苷酸酶(CD39 和 CD73)是 TME 中细胞外腺苷的主要来源。CD39 和 CD73 表达增加与癌症患者预后不良有关。它们在肿瘤和免疫细胞上普遍表达,并且已被确定通过作用于这两种细胞中的相关通路介导免疫抑制作用。
7.1 引言
自从1955年汤姆林森和格雷发现肿瘤缺氧以来,这一直是肿瘤学家非常感兴趣的话题。在他们的研究中,作者观察到来自人类肺癌患者的肿瘤具有放射抗性,并且根据组织学分析,表现出不均匀的氧分布。1977年,Reinhold等人拓展了这些初步发现,并得出结论:包裹肿瘤的血管系统结构紊乱,随后导致氧气水平的波动。
目前,我们知道缺氧肿瘤微环境(TME)在遗传上是不稳定的,并经历不断的代谢重组。这种缺氧环境触发TME中的细胞释放促炎性三磷酸腺苷(ATP),随后被外核苷酸酶(CD39和CD73)去磷酸化为免疫抑制性腺苷。Geoffrey Burnstock的实验有助于证明细胞外ATP和腺苷能够以自分泌/旁分泌方式与质膜上的嘌呤受体结合。1978年,他的团队将嘌呤受体分为两个亚组,一个是选择性ATP/二磷酸腺苷(ADP)受体(称为P2受体),另一个是选择性腺苷受体(称为P1受体)。
在过去的十年中,已经证明P2和P1嘌呤受体(P2R,P1R)通过多种非冗余、免疫和非免疫介导的机制影响肿瘤的进展。目前,开创性的研究已经明确证明,免疫细胞和肿瘤上的几种嘌呤受体的激活可以促进肿瘤生长和转移。特别是缺氧和腺苷可以下调抗原呈递细胞(APC)上主要组织相容性复合体(MHC)II类分子和其他共刺激分子的表达。这个过程会损害T细胞的激活和效应功能,而T细胞是许多癌症免疫控制的核心。笔者研究小组和其他研究小组进一步证明,某些嘌呤受体的表达可能直接或间接抑制T细胞和自然杀伤(NK)细胞的效应功能,从而抑制对原发性肿瘤及其转移的免疫反应。
腺苷还可以促进调节性T细胞(Tregs)和髓样细胞群的增殖和免疫抑制功能。除了在免疫细胞中的作用外,其中一些ATP和腺苷受体在人类癌症中过度表达,它们的激活能够促进肿瘤细胞增殖、侵袭、迁移和血管生成。目前,其中两种嘌呤受体(CD73和A2AR)作为实体癌治疗的阻断靶点正在进行临床试验,这也突出了该途径在肿瘤进展中的重要性。
本章描述了ATP和腺苷改变TME动态影响肿瘤生长和发展的机制。此外,我们概述了针对嘌呤能途径中各种受体的治疗方法,并且还证明了与当前批准的免疫检查点抑制剂(如抗PD-1/PD-L1和抗CTLA-4)组合的协同效应。总的来说,从小鼠和人类研究的证据表明,开发能够特异性靶向嘌呤能途径的各个方面的药物作为癌症治疗新策略是非常有前景的。
7.2 细胞外ATP和腺苷在肿瘤中的作用
氧气是一种微环境因子,在调节细胞代谢以及维持正常组织内稳态方面至关重要。氧气从血管扩散到组织中,与这些血管的接近程度决定了该组织中的氧合水平。通常,氧气的扩散极限约为100–200μm,超过此半径的组织被归类为缺氧组织。
在实体肿瘤中,肿瘤血管系统的异常结构加上转化细胞的不可控增殖通常会导致氧气供应不均匀。因此,无论是急性发生还是慢性发生,大多数实体瘤都存在缺氧区域。例如,在鳞状细胞癌患者中,高达30%的肿瘤区域被确定为缺氧的状态。肿瘤通过启动一系列有利于肿瘤细胞血管生成、侵袭和代谢重编程的反应机制来适应缺氧。
缺氧性肿瘤在遗传上不稳定,DNA断裂和DNA复制错误的频率增加。此外,缺氧调节多药耐药基因1(MDR1)和多药耐药相关蛋白1(MRP1)等基因的表达。这使得这些肿瘤对放疗和化疗产生耐受,因此在临床上,缺氧是一个不利的预后因素。
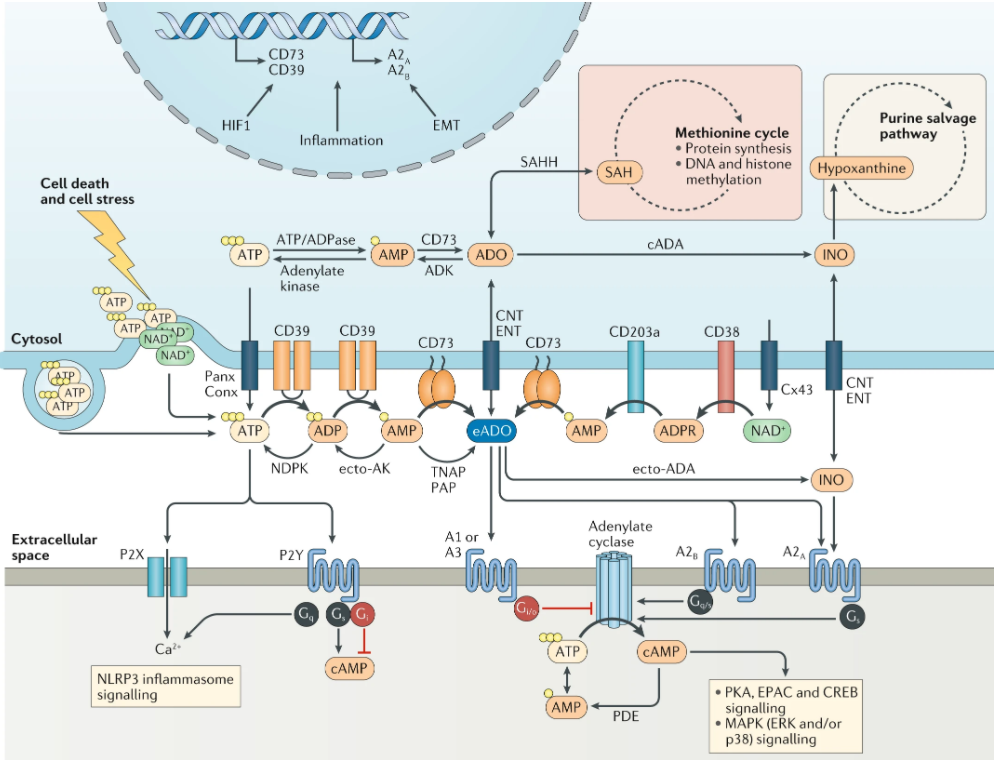
缺氧可激活缺氧诱导因子-1α(HIF-1α),进而诱导能量(ATP)生成所需的几种生物合成中间产物的上调。在肿瘤中,细胞外的ATP可以由坏死或炎性细胞释放,也可以通过与ATP结合转运蛋白、膜联蛋白或缝隙连接蛋白有关的机制从癌细胞释放(见Fig 7.1)。高度不稳定的ATP迅速分解为ADP或单磷酸腺苷(AMP),最后分解为腺苷(Fig 7.1)。
因此,缺氧水平的增加可导致TME中腺苷水平的升高。Busse和Vaupel于1996年首次报告了这一观察结果,发现TME中的腺苷水平与肿瘤质量相关。此后,几项研究证实许多小鼠和人类肿瘤中腺苷水平均有升高。例如,Zhang等人的研究表明,缺氧通过激活信号分子细胞外信号调节激酶(ERK)促使M2型巨噬细胞的发育来促进肿瘤的发展。这导致小鼠肺癌内的血管增加,并促进了小鼠肺癌生长的进程。同样,与周围正常组织相比,在各种人类实体腺癌中,如人类结肠癌(T-84和HT-29)和肺癌(A549)以及小鼠MC38结肠癌中,细胞外腺苷水平也被发现增加了许多倍。
在肿瘤形成过程中,细胞外腺苷主要通过两种外核苷酸酶的顺序激活产生。其中包括将ATP和ADP水解为AMP的CD39,以及将AMP进一步去磷酸化为腺苷的CD73(Fig 7.1)。转录因子Sp-1和HIF-1α介导CD39和CD73表达的上调。除CD39和CD73外,碱性磷酸酶(ALP)、核苷酸焦磷酸酶以及磷酸二酯家族的几个成员,包括NPP1/CD203a,也可促进细胞外腺苷的产生。
然而,尽管有报道称该通路在神经胶质瘤、黑色素瘤、前列腺癌和多发性骨髓瘤中被激活,但对该通路在癌症中的作用却知之甚少。重要的是,通过腺苷脱氨酶(ADA)与CD26的结合,腺苷可以进一步降解为肌苷(Fig 7.1)。然而,Tan等人的一项研究表明,腺苷自身水平的升高可以有效抑制HT-29结直肠癌细胞上ADA和CD26的活性。ADA在癌症发展过程中是否起关键作用尚待进一步确定。
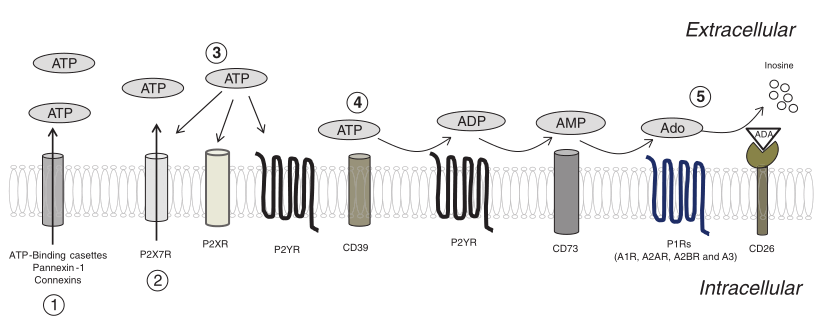
Fig. 7.1 肿瘤微环境(TME)中细胞外ATP和腺苷的生成。(1)作为对缺氧的响应,TME中的细胞通过ATP结合盒、Pannexin-1或连接蛋白释放ATP。(2)嘌呤受体P2X7R也参与TME内ATP的分泌。(3)环境中ATP的积累可兴奋P2嘌呤受体P2XR和P2YR。(4)CD39和CD73的顺序作用使ATP分别降解为ADP/AMP和腺苷(Ado),从而导致免疫抑制性TME的产生。(3)部分P2YR包括P2Y1R、P2Y12R和P2Y13R能够与ADP结合并触发下游信号转导。ADO通过P1受体、A1R、A2AR、A2BR和A3R调节肿瘤生长。(5)在腺苷脱氨酶(ADA)及其受体CD26存在下,积累的腺苷可随后分解为肌苷。三磷酸腺苷、二磷酸腺苷、一磷酸腺苷。
7.3 嘌呤受体在免疫和癌症中的作用
ATP 和腺苷的生物学作用依赖于在肿瘤和浸润性免疫细胞以及非免疫细胞上大量表达的嘌呤受体的激活。ATP结合P2Rs,而腺苷结合P1Rs。P2R可进一步分为七个P2X(P2X1-P2X7)和八个P2Y(P2Y1-2、P2Y4、P2Y6、P2Y11-14)受体亚型。P1R结合腺苷,由四个G蛋白偶联受体(GPCR)组成,即A1R、A2AR、A2BR和A3R。重要的是,两种胞外核苷酸酶CD39和CD73的协同作用构成了TME细胞外腺苷的主要来源。因此,在本节中,我们将讨论肿瘤细胞和免疫细胞上嘌呤受体和外核苷酸酶的激活如何影响肿瘤的生长和转移。
7.3.1 对肿瘤细胞的影响
7.3.1.1 感应ATP的P2受体:P2XR和P2YR
TME中高浓度的ATP可直接影响肿瘤发生过程中P2Rs的表达和功能。这一点通过几种人类和小鼠的肿瘤细胞系的P2R差异表达得到了证实(总结见Table 7.1)。通常,肿瘤细胞上P2XRs的表达与抗肿瘤功能相关(见Table 7.1)。然而,P2X7R对肿瘤细胞的生长和存活的影响似乎有着相反的作用。
例如,P2X7R的激活促进了PC9肺癌和T47D乳腺癌细胞的迁移,而这些细胞中P2X7R的siRNA的敲除逆转了它们迁移的能力。相反,在P2X7R过表达的急性髓系白血病(AML)细胞中加入外源性ATP会抑制其表达,并导致细胞周期基因、迁移和粘附分子的抑制。同样,B16F10黑色素瘤细胞上P2X7R的激活导致这些细胞的增殖和存活率降低。
导致这些差异的一个可能原因是这些研究中用于体外刺激的ATP的水平。这一观点得到了Giannuzzo等人的支持,他们发现ATP的浓度可能对P2X7R活性产生截然相反的影响。具体而言,高水平的ATP可激活人胰腺导管腺癌细胞(PDAC)上的P2X7R,导致其增殖和存活率降低。相反,低水平或基础水平的ATP促进了它们的细胞迁移和侵袭特性。
在癌症患者中也发现了这种相反的P2X7R效应,即P2X7R的表达与胶质瘤、非小细胞肺癌(NSCLC)和肝细胞癌(HCC)患者的总体生存率有良好的相关性。然而,肾细胞癌(RCC)患者的情况则相反(Table 7.2)。
P2YRs在肿瘤上的表达在很大程度上有利于肿瘤的生长、迁移和存活(Table 7.1)。在人乳腺癌细胞系MCF-7上检测到P2Y2Rs,其激活增强了肿瘤细胞的迁移和增殖能力。同样,MDA-MB-231细胞上P2Y2R的激活增加了粘附分子-细胞间粘附分子-1(ICAM-1)和血管细胞粘附分子(VCAM)的表达。这随后导致肿瘤细胞与内皮细胞的粘附增加,从而促进肿瘤细胞的迁移和侵袭。相比之下,AML细胞对趋化因子CXCL12的反应在经过P2Y2R和P2Y6R激动剂孵育后减弱。
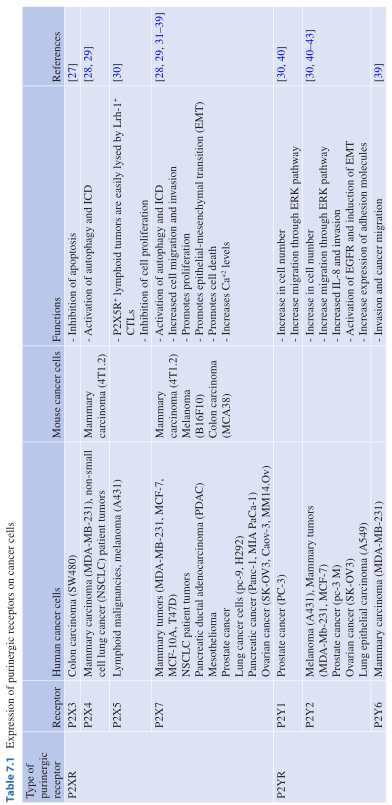
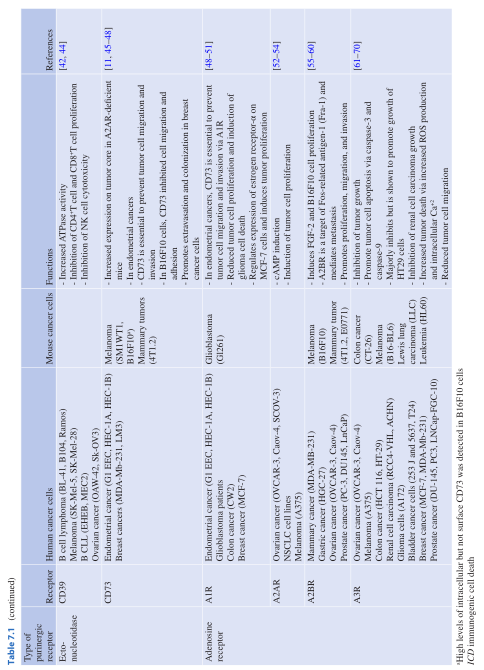
Table 7.1 嘌呤受体在癌细胞上的表达
7.3.1.2 促使腺苷产生的外核苷酸酶:CD39和CD73
如Table 7.1所示,CD39和CD73的共同或差异表达在许多来源于实体和血液的人类癌症中已有报道。越来越多的证据表明,肿瘤细胞上CD39和CD73的表达可促进肿瘤细胞的生长和存活。因此,CD39或CD73高表达的癌症患者在几种癌症类型中表现出较差的生存和无复发生存期的结果也就不足为奇了(Table 7.2)。
在临床前实验中,人CD39+CD73+SK-MEL5黑色素瘤细胞与人外周血单个核细胞(PBMC)的共培养抑制了CD4+和CD8+T细胞的增殖,并降低了CD8+T细胞的细胞溶解活性。用CD39抑制剂对癌细胞进行预处理逆转了这种抑制表型,并增强了CD8+T细胞和NK细胞的效应功能。同样,据报道,人类卵巢癌细胞上的CD39表达可抑制T细胞和NK细胞的效应功能。表达CD73的ID8小鼠卵巢癌细胞也可抑制CD8+和CD4+T细胞的增殖以及效应细胞因子IFN-γ的产生。从间皮瘤患者分离的外泌体也发现了CD39和CD73的表达,它们表现出强大的酶活性,导致局部腺苷的产生。在功能上,这些外显体抑制人类CD4+和CD8+T细胞的增殖和细胞因子释放。
虽然CD73具有促肿瘤作用,但有趣的是,最近一个研究小组发现CD73对人类子宫内膜癌具有抗肿瘤作用。在这项研究中,这些肿瘤上CD73的缺失阻碍了肌动蛋白聚合,从而阻碍了细胞间粘附和子宫内膜上皮细胞完整性的丧失。结果,这些肿瘤变得高度迁移和侵袭。
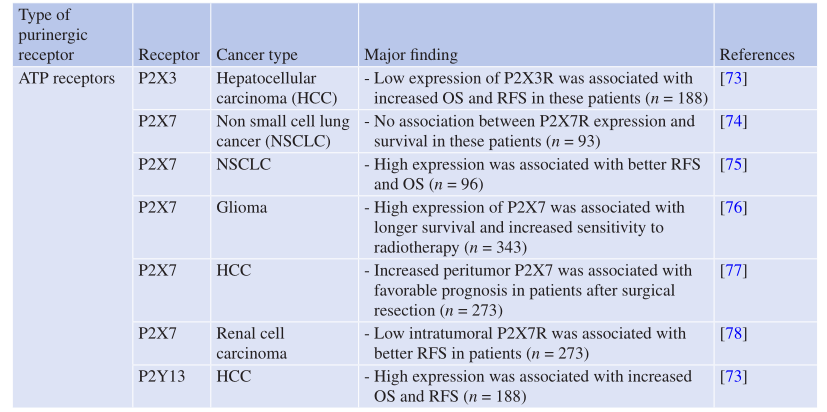
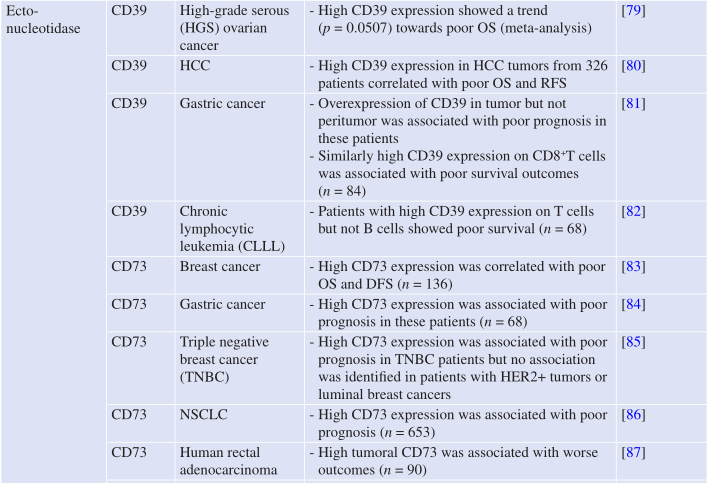
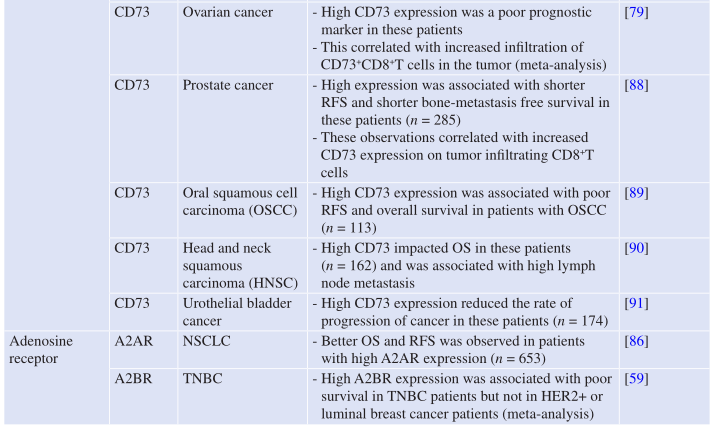
Table 7.2 嘌呤受体在人类癌症中的作用
7.3.1.3 腺苷结合受体P1:A1、A2a、A2b和A3
P1Rs类似于P2YRs,在小鼠和人类的肿瘤细胞中广泛表达(Table 7.1)。在生理条件下,腺苷激活高亲和力A1、A2A和A3受体。相反,A2BR(一种低亲和力受体)的激活发生在腺苷浓度高的情况下,这在TME等病理条件下很常见。通过A1R和A3R发出的信号抑制细胞内环腺苷酸(cAMP),而A2AR和A2BR激活腺苷酸环化酶和蛋白激酶A,导致细胞内环腺苷酸(cAMP)水平升高。高水平的cAMP通常与严重的免疫抑制相关,因此A2AR和A2BR被视为促肿瘤的腺苷能受体。
A2AR的抑制功能已在TME内的免疫细胞中进行了大量研究,但对肿瘤上A2AR的表达如何影响肿瘤细胞功能的理解仍有限。最近的一项研究显示,腺癌患者的A2AR肿瘤活检的高表达与生存率有良好的相关性。与此观察结果相反的是,在人类A375黑色素瘤细胞中抑制A2AR会降低这些肿瘤中的细胞存活率和增殖率。然而,这些相反结果背后的确切原因目前尚不清楚。
另一方面,A2BR主要对肿瘤而非免疫细胞发挥抑制作用。该受体在人和小鼠三阴性乳腺癌(TNBC)细胞中检测到,其表达增加了这些细胞的存活率。与这些发现一致的是,A2BR的过度表达与TNBC、多发性骨髓瘤、AML和脂肪肉瘤患者的低生存率相关。Wang等人最近发现microRNA-128b抑制A2BR的表达。在胃癌患者中,microRNA-128b下调导致A2BR表达增加,从而促进了肿瘤细胞的增殖、迁移和存活。
激活的A1R可增加乳腺癌细胞上雌激素受体-α(ER-α)的表达,进而促进癌症生长。A3R在肿瘤细胞上的表达具有反差效应。A3R存在于人原发性胶质母细胞瘤和前列腺癌中,体外刺激可抑制PC3前列腺癌、HCT-116结肠癌和MIA-PaCa胰腺癌细胞的增殖。而矛盾的是,A3R在HT29和CaCo2结肠癌细胞上的激活可诱导肿瘤细胞增殖。与之类似,A3R激动剂CI-IB-MECA对人A375黑色素瘤细胞的处理会诱导血管生成因子Angiopoeitin-2(Ang-2)的分泌。
7.3.2 对免疫细胞的影响
7.3.2.1 ATP/ADP结合性P2受体
P2XRs介导Na+、K+和Ca2+离子跨质膜的转运。因此,推测这些受体不参与抗肿瘤免疫的调节。所以,尽管P2XR和P2YR在同一时间被发现,但P2XRs在免疫调节中的作用直到现在才变得明显起来。各个P2XRs在不同免疫细胞类型上的表达如Table 7.3所示。在已知的P2XRs中,P2X7R在免疫细胞和肿瘤细胞中的表达和功能得到了最全面的研究。Cockcroft和Gomperts首次在大鼠肥大细胞中发现P2X7R的表达。他们最初将P2X7R称为“ATP4− 受体”,因为它与完全解离的ATP(ATP4−)结合。1996年,这一“ATP 4− 受体”由Surprenant等人克隆,由于其与其他P2XR的同源性,随后被重新命名为P2X7R。相比之下,P2YRs是G蛋白偶联受体,对ATP/ADP甚至5′-磷酸尿苷(UTP)产生反应,并影响cAMP的激活,cAMP既有促炎功能,也有抗炎功能,与P2XRs类似,P2YRs也在小鼠和人类免疫细胞中表达,P2Y6R亚型的研究比其他亚型更加深入(Table 7.3)。
与对肿瘤的作用类似,P2受体的活性在很大程度上受细胞外ATP水平的调节(Table 7.3)(Fig. 7.2)。例如,低至中等水平的ATP通过激活P2Y11R触发小鼠树突状细胞(DC)成熟和诱导T辅助细胞2(TH2)细胞。相反,高水平的ATP激活了人肺泡巨噬细胞上的P2X7R,这种相互作用导致炎症细胞因子IL-1β的释放。Vishva Dixit的研究小组后来证明炎症小体的激活是因为P2X7R介导的IL-1β的分泌。通过P2X7R发出的信号还可以激活几个关键的巨噬细胞功能,包括产生活性氧(ROS)、一氧化氮(NO)、诱导吞噬和形成多核巨细胞。
有报道称,人和小鼠中性粒细胞上的P2Y2R、P2Y11R和P2Y14R信号传导以及人单核细胞、小鼠巨噬细胞和DC上的P2Y2R和P2Y6R信号传导具有类似的迁移和趋化功能。在人类NK细胞上,P2Y11R的参与通过消除其迁移和细胞毒性功能来抑制NK细胞对趋化因子CX3CL1的反应性。T细胞受体(TCR)的刺激也可触发T细胞释放ATP,然后介导P2X1R、P2X7R和P2X4R的自分泌激活来增强T细胞增殖和信号传导。此外,人内皮细胞上P2YR的信号传导是通过血管内皮生长因子受体-2(VEGFR-2)的反式激活来促进血管生成的。
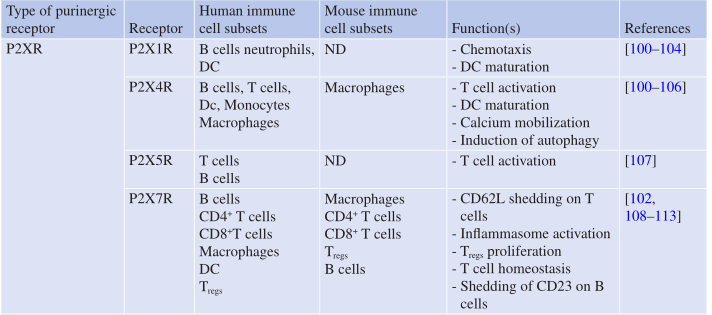
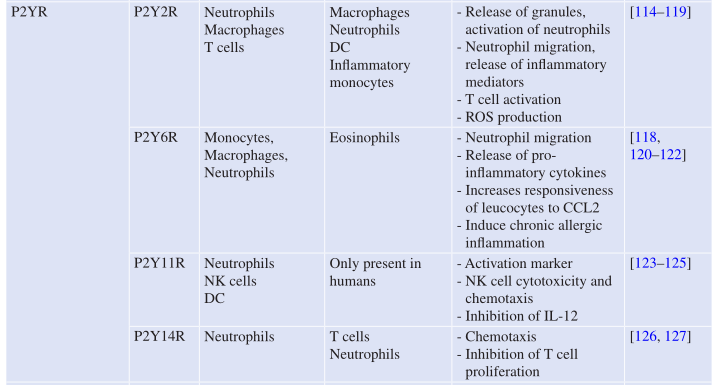
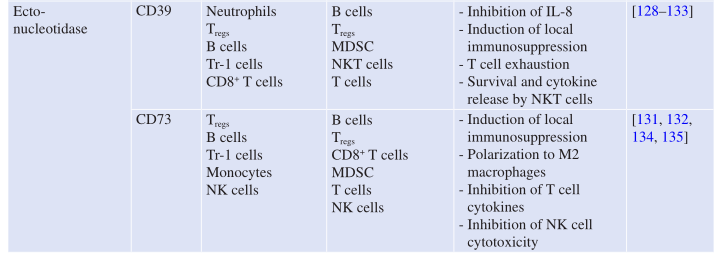
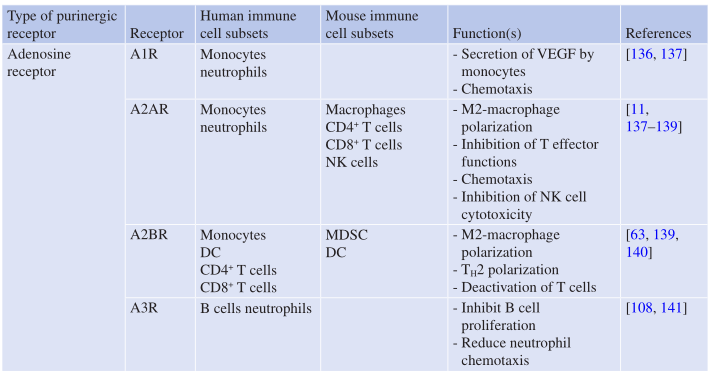
Table 7.3 嘌呤受体在人和小鼠免疫细胞上的表达
7.3.2.2 促使腺苷产生的外核苷酸酶:CD39和CD73
Gregory等人首先描述了CD39在B细胞上的表达。在他们的研究中,CD39被确定为伯基特淋巴瘤患者扁桃体B细胞的激活标志物。此后,发现CD39在脾脏、胸腺、肺以及原发性肿瘤中呈组成性表达(Table 7.3)。细胞因子、氧化应激和缺氧诱导的转录因子,如Sp-1、STAT3和锌指蛋白生长因子非依赖性转录因子(Gfi1),都可以上调CD39的表达。免疫细胞和组织上的其他外核苷酸酶CD73的表达模式也与CD39的表达模式非常相似(Table 7.3)。
CD39和CD73的免疫抑制作用可归因于这些受体在抗炎细胞上的相对高表达,包括肿瘤相关巨噬细胞(TAM)、Tregs、1型调节(Tr-1)细胞和抑制性骨髓细胞群(Table 7.3)。在TME中,CD39和CD73的主要功能在于触发ATP快速分解代谢为免疫抑制性腺苷,防止P2受体脱敏,进而促进肿瘤发展。事实上,当与CD4+T细胞共培养时,CD73+CD39+TAM通过产生腺苷显著抑制了T细胞的增殖。阻断TAM上CD39或CD73的活性足以挽救这种T细胞效应。同样,CD39+Tr-1细胞与CD73+CD4+T细胞的共培养进一步抑制了这些细胞的活性。CD39/CD73轴对中性粒细胞的有效激活、粘附和趋化性也至关重要,据报道,它们还具有促肿瘤功能。大多数人类Tregs是CD39+而不是CD73−, 然而这些细胞中的CD73大量存在于胞质内颗粒中。TCR参与后,Tregs上CD73的表达和活性得到增强。
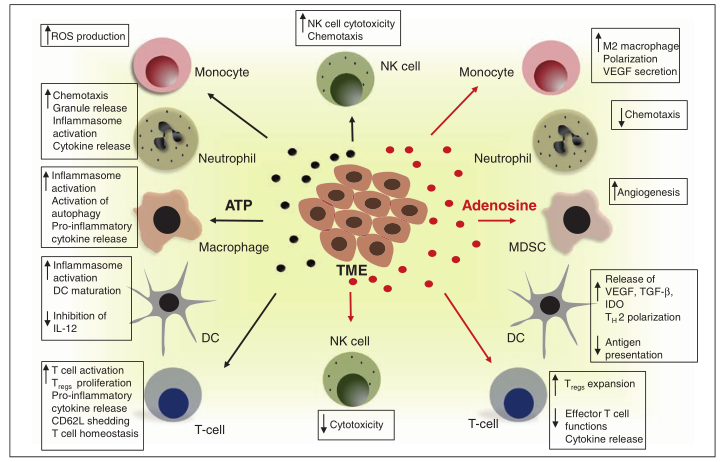
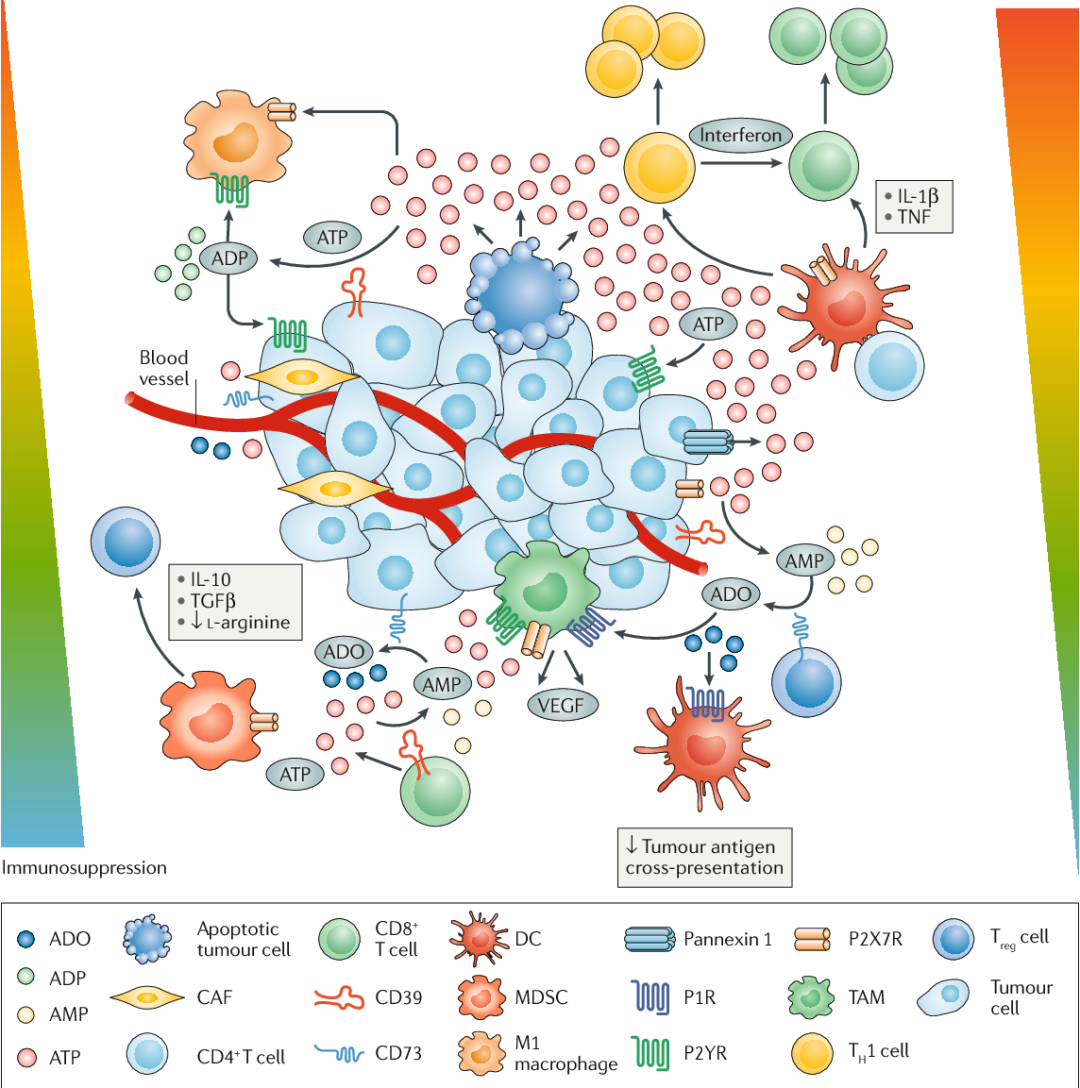
Fig. 7.2 CD39和CD73的外核苷酸酶活性促使肿瘤从ATP驱动的炎症状态转变为富含腺苷的免疫抑制性TME。
肿瘤和肿瘤浸润细胞释放的ATP激活P2嘌呤受体。这主要通过激活炎症小体、自噬、增加细胞因子释放和激活免疫原性细胞死亡来诱导抗肿瘤作用(如左图所示)。
相反,通过CD39-CD73轴产生腺苷会对TME产生负面影响,并通过血管生成增加、免疫抑制性免疫群体(MDSC和Tregs)扩张以及NK细胞和CD8+T细胞的细胞毒性功能受损等机制促进肿瘤生长和转移(如右图所示)。
7.3.2.3 腺苷结合性P1受体:A1、A2a、A2b和A3
P1R在小鼠和人类的髓系淋巴系免疫细胞中广泛表达(Table 7.3)。在P1受体中,A1R和A2BR的表达更局限于髓系细胞,而A2AR和A3R在髓系和淋巴细胞群体中的表达更为普遍。
免疫细胞上A1R和A3R的表达主要激活抗肿瘤免疫反应。例如,使用CPA(一种A1R激动剂)对小鼠进行预处理,可促进脾脏CD4+T细胞的增殖,并增加IL-2的产生。类似地,使用激动剂Cl-IB-MECA激活A3R,能增强NK细胞功能,并提高小鼠的抗肿瘤免疫。
2001年,Sitkovky的研究小组首次证明了A2AR的抗炎作用。在他们的研究中,与野生型(WT)小鼠相比,A2AR缺陷小鼠表现出更严重的肝炎和更严重的组织损伤。目前,我们了解到髓细胞和淋巴细胞中的A2AR信号可以参与介导TME中的局部免疫抑制(Fig 7.2)。A2AR信号可抑制巨噬细胞分化、成熟和活化。此外,Cekic等人证明,髓样细胞上A2AR的表达可增加TME中TAM和肿瘤相关DC(TADC)产生的抗炎IL-10细胞因子。此外,髓系细胞上A2AR的条件性缺失显著增强了肿瘤中CD8+T细胞和NK细胞的浸润、激活和效应功能。同样,NK细胞上A2AR的激活抑制了其产生IFN-γ的能力,而A2AR激动剂CGS21680的激活增加了混合培养的淋巴细胞中Tregs的比例。
A2BR的刺激也可促进免疫抑制,但主要作用于髓系细胞。具体而言,A2BR抑制造血祖细胞向成熟髓系细胞的分化,并导致未成熟细胞的积累增加。这些细胞通过产生血管内皮生长因子(VEGF)、IL-8、TGF-β和吲哚胺2,3-双加氧酶(IDO)表现出免疫抑制功能。类似地,用A2BR激动剂Bay60-6583治疗小鼠可增加髓系来源的抑制细胞(MDSC)在B16F10原发黑色素瘤中的浸润,而这些抑制细胞的缺失可促进这些小鼠的抗肿瘤作用,这也暗示了MDSC的A2BR信号传导可促进肿瘤的生长。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 往期文章目录
基础免疫学系列
肿瘤免疫学系列
肿瘤免疫学-第6章:调节性T细胞的作用、作用机制以及对癌症的影响(下)
肿瘤免疫学-第6章:调节性T细胞的作用、作用机制以及对癌症的影响(上)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(下)
肿瘤免疫学-第3章:CD8+ T细胞在免疫治疗、放疗和化疗中的作用(上)
文献分享系列
年度巨献:神刊CA发布最新癌症数据:全球1000万人死于癌症,中国占比超3成
HLA-I分子加工和递呈抗原功能受损是免疫检查点抑制剂耐药的重要原因
生信入门学习笔记系列
基础实验技术系列
Annexin V/PI染色检测细胞凋亡-OncoLab实验室
仪器操作系列
蔡司LSM800激光共聚焦显微镜操作视频-中西医结合基础研究中心
IN Cell Analyzer2200高内涵细胞成像分析系统操作教程-中西医结合基础研究中心
作图投稿选刊系列
GraphPad+AI制作可发表级别的柱状图-OncoLab实验室
PubMed中如何按影响因子筛选检索结果并显示影响因子及分区?
如何使用EndNote软件插入参考文献(附6813种杂志参考文献格式文件)
中医中药系列

关注本号~

加入读者交流群~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏