节
日
DRAGON BOAT
FESTIVAL

DRAGON BOAT
FESTIVAL
2021/06/14
祝大家端午安康!
上期内容链接:肿瘤免疫学-第9章:自然杀伤细胞以及其它固有淋巴细胞对肿瘤的免疫监视作用(上)
,今天我们继续学习后面的内容。
9.3 激活ILC的细胞因子和可溶性因子
除了细胞间的相互作用外,ILC(先天淋巴细胞)还整合了由可溶性介质提供的多种信号,如上皮细胞、间质细胞或髓样细胞产生的细胞因子、警报素、脂质或由上皮细胞、基质细胞或骨髓细胞产生的激素 (Fig 9.3)。
肿瘤的生长可能会扰乱周围组织的动态平衡,导致细胞因子和危险信号的释放,这可能会造成ILC介导的免疫监视。NK细胞和辅助性ILC1对IL-12、IL-15和IL-18均有反应,而ILC2主要对IL-25、IL-33和TSLP有反应,ILC3则由IL-23和IL-1β激活。
几乎没有直接证据可以证明生理分泌的细胞因子对癌症中ILC的作用,大多数研究更多的是关注外源性细胞因子的作用,或者使用基因操纵的肿瘤或小鼠。
例如,一份报告描述了过度表达IL-15的转基因小鼠对皮下注射缺乏MHC-I的B16黑色素瘤细胞具有抵抗力。在这项研究中,在没有CD4+或CD8+T细胞的情况下,其抗肿瘤活性保持不变,但当NK细胞被抗asialo-GM1抗体耗尽时,其保护作用就丧失了。
此外,IL-2、IL-12和IL-18能促进NK细胞介导的小鼠实验性转移的调控,IL-12、IL-15和IL-18预激活的NK细胞显示持续的效应功能,并延缓MHC-I缺陷小鼠肿瘤的生长。有趣的是,最近的一项研究证实,IL-12诱导的对皮下B16黑色素瘤的抑制是由NKp46+NK1.1−ILC3群体介导的,该细胞群的分化受转录因子RORγt调控。
最后,NK细胞和ILC3s表达的Toll样受体可能使这些细胞能够检测肿瘤微环境中存在的危险相关分子模式(DAMP)。DAMP可直接或间接通过刺激辅助细胞诱导NK细胞激活。有趣的是,最近的一项研究证实,TLR3缺陷小鼠的NK细胞对细胞因子刺激反应迟钝,这一缺陷与这些小鼠在受到B16F10黑色素瘤细胞攻击时增加实验性肺转移有关。
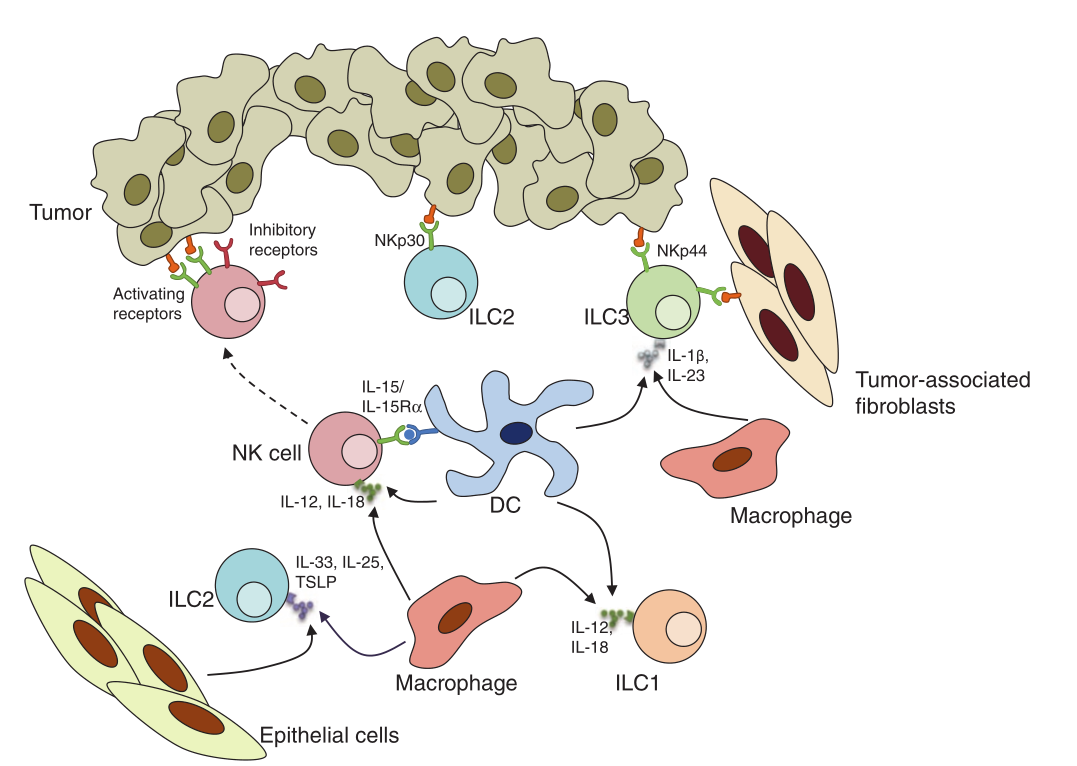
Fig 9.3 细胞因子和膜结合配体参与ILC的活化。树突状细胞和巨噬细胞产生的IL-12、IL-15和IL-18等细胞因子在激活受体的作用下增加了它们的能力。IL-12和IL-18也可刺激ILC1产生干扰素-γ。ILC2对IL-25、IL-33和TSLP有反应。此外,人类ILC2在NKp30参与时被激活,而人类ILC3对NKp44刺激有反应,ILC3被细胞因子IL-1β和IL-23激活。
值得注意的是,辅助性ILC主要通过可溶性介质激活,而NK细胞受体是NK细胞激活的主要途径。然而,相比于静止的NK细胞,细胞因子激活的NK细胞对NK细胞受体信号更敏感。
激活NK细胞的细胞因子通常由髓系细胞或树突状细胞(DC)分泌。事实上,有人认为,幼稚的NK细胞只有在与DC或巨噬细胞相互作用后才能发挥完整的杀伤效应,这一过程被称为“NK细胞启动”,这一过程受到共生微生物区系的影响。特别有趣的是,最近在NCR+ILC3s中描述了细胞因子介导的激活和NCR信号之间类似的协同作用。
9.4 ILC对癌细胞的直接清除作用
含有穿孔素和颗粒酶的细胞毒性颗粒的释放构成了NK细胞发挥杀伤活性的主要途径。穿孔素是一种成孔蛋白,它允许颗粒酶进入靶细胞,从而引发细胞凋亡。穿孔素保护小鼠免受自发性淋巴瘤的侵袭,在小鼠中的研究证实了穿孔素在NK细胞介导的缺乏MHC-I的肿瘤排斥反应中的主要作用,以及NK细胞介导的转移控制和对致癌物诱导的纤维肉瘤的保护作用。颗粒依赖性细胞毒性最初被认为是NK细胞区别于ILC1细胞的特征。
然而,最近的研究表明,一群明显不同于传统NK细胞的ILC1样细胞也能以穿孔素依赖的方式杀死肿瘤细胞。值得注意的是,这项研究使用自发性小鼠乳腺癌模型表明 ILC1 样细胞而非常规 NK 细胞有助于减少肿瘤生长。
Fas配体(FasL或CD95L)和肿瘤坏死因子相关的凋亡诱导配体(TRAIL)属于死亡受体途径,代表了NK细胞清除靶细胞的另一种机制。
FasL或TRAIL与其受体(分别为Fas和DR5或DR4)的结合可触发常见的死亡信号分子FADD、caspase8和caspase3的激活,并导致细胞凋亡。以Fas和TRAIL死亡受体通路为靶点,绕过癌症干细胞的难治性,从而进行常规治疗的相关性已经在小鼠身上得到证实。
最初,TRAIL阳性的NK细胞在幼稚小鼠的肝脏中被发现;在体外,肝脏的NK细胞的杀伤活性被证明是依赖TRAIL的。因此,TRAIL似乎对控制小鼠实验性肝转移是必要的。有趣的是,TRAIL在新生小鼠体内主要由未成熟的NK细胞表达,是胎儿NK细胞体外杀伤TRAIL敏感靶点所必需的。同样,TRAIL是人脐血NK细胞体外杀伤活性所必需的,而成熟的人NK细胞的细胞毒作用主要依赖于穿孔素和FasL途径。
虽然TRAIL+胎儿NK细胞的来源尚不清楚,但小鼠肝脏TRAIL+NKp46+细胞现已被归入ILC1谱系。在健康人的肝脏中,NK细胞不表达TRAIL,但其表达可被促炎细胞因子诱导。最近研究表明,TRAIL的上调仅限于表达CXCR6的特定人群的人肝内NK细胞,而外周缺乏。因此,在没有炎症刺激的情况下,TRAIL的表达可能仅限于I型ILC的组织驻留亚群。
事实上,在小鼠的唾液腺ILC1和肿瘤浸润性ILC1样细胞上也检测到TRAIL。然而,我们还观察到细胞因子刺激诱导小鼠脾脏中的CD3-NK1.1+细胞和人血液中的CD3–CD56+细胞上的TRAIL表达,这表明TRAIL在某些情况下也有助于常规NK细胞的功能。事实上,膜结合的TRAIL补充了穿孔素介导的从人外周血中分离的活化NK细胞对神经母细胞瘤和多发性骨髓瘤细胞系的杀伤作用。
进一步的研究应该会阐明血液循环中的常规NK细胞和组织驻留的ILC1在TRAIL介导的新生肿瘤控制中各自扮演的角色。与TRAIL的研究相反,支持FasL在NK细胞介导的体内肿瘤控制中的作用的数据非常有限。值得注意的是,最近的一项研究证明,IL-18诱导小鼠NK细胞表面FasL的快速表达,并发现NK细胞介导的FasL依赖的细胞毒作用可以控制MC38小鼠的肝转移。
I型ILCs的一个重要特征是分泌干扰素-γ和肿瘤坏死因子(TNF)。这两种细胞因子在肿瘤发生中起重要作用,它们不仅能调节免疫反应,还能直接影响肿瘤细胞的生命机理。事实上,在去除干扰素-γ对肿瘤的反应性后,已经观察到各种小鼠细胞系在体内的增殖加强。
对干扰素-γ的应答是由JAK-STAT信号通路诱导的。在癌细胞中,这一途径已被证明可以抑制细胞增殖和促进细胞凋亡。Schreiber和他的同事已经证明了内源性干扰素-γ在促进免疫介导的消除新生肿瘤细胞中所起的重要作用。
早期研究表明,穿孔素和干扰素-γ途径的结合可以解释小鼠NK细胞的抗转移活性。尽管如此,由于干扰素-γ可以由许多不同的天然和获得性免疫细胞类型产生,因此目前还缺乏正式的证据证明ILC在干扰素-γ介导的免疫监视中的作用。
至于肿瘤坏死因子,这种细胞因子在癌症生物学中的作用是相当模糊的。TNF的两个受体是TNFR1和TNFR2,TNFR1在所有类型的细胞上都有表达,而TNFR2仅限于免疫细胞和内皮细胞表达。
但矛盾的是,TNFR1既可以传递促生存信号,也可以传递促凋亡信号。因此,一些报告描述了TNF对肿瘤细胞的细胞抑制或细胞毒作用,而另一些报告则观察到了恶性细胞增殖的增强。肿瘤坏死因子缺陷小鼠的NK1.1+脾细胞对YAC-1的体外杀伤能力降低的现象表明,肿瘤坏死因子参与了NK细胞介导的杀伤。此外,NK细胞对化疗致敏的小鼠MC38肿瘤的杀伤作用被发现是肿瘤坏死因子依赖性的。
但总体而言,到目前为止还没有令人信服的证据表明TNF对天然细胞介导的细胞毒活性有重大贡献。事实上,来自肿瘤坏死因子缺陷小鼠的脾细胞在体外完全能够溶解MHC-I缺陷的RMA-S肿瘤细胞。然而,在肿瘤坏死因子缺乏的小鼠进行腹腔注射后,观察到RMA-S细胞的缺陷消除。这一现象可以由在缺乏TNF的情况下会减少NK细胞在腹膜中的积聚来解释。
此外,在抗CD319单抗(Elotuzumab)存在的情况下,TNF的中和可抑制NK细胞的激活,从而降低人NK细胞介导的对骨髓瘤细胞的细胞毒活性。综上所述,这些数据表明,NK细胞分泌的TNF虽然没有直接的细胞毒作用,但可能对肿瘤微环境起调节作用。
值得注意的是,虽然对肿瘤细胞的直接细胞毒活性被认为是I型ILC的特异性,但最近发现ILC2通过CXCR2途径也可直接诱导肿瘤细胞凋亡。
9.5 ILC与其他免疫细胞之间的相互作用
NK细胞的功能远远不止简单地杀死癌细胞。除了干扰素-γ和肿瘤坏死因子外,激活的NK细胞还释放多种细胞因子,包括GM-CSF、IL-6和IL-10,它们可能通过分泌趋化因子如单核细胞趋化蛋白-1(CCL2)、巨噬细胞炎性蛋白-1α(CCL3)、MIP-1β(CCL4)、RANTES(CCL5)、IL-8(CXCL8)和IP-10(CXCL10)来促进其他免疫细胞的招募。
已显示 NK 细胞产生的 IFN-γ 可促进巨噬细胞介导的小鼠致癌物诱导肿瘤的免疫编辑。此外,NK细胞以许多不同的方式影响T细胞反应的结果。例如,NK细胞通过清除髓系来源的抑制性细胞(MDSC)和激活DC来增强启动细胞毒性CD8+T细胞的反应。
NK细胞对肿瘤细胞的杀伤和随后抗原的释放进一步促进了T细胞的启动。此外,NK细胞被招募到发炎的淋巴结,这为干扰素-γ提供了早期来源,是CD4+T细胞Th1型极化所必需的。激活的调节性T细胞(Tregs)的直接细胞毒性是NK细胞增强效应T细胞反应的另一种机制。重要的是,在一些小鼠肿瘤模型中,NK细胞被发现有助于启动肿瘤特异性记忆T细胞,这是长期控制癌症所需的。
我们对辅助性ILC介导的抗肿瘤反应调节的理解还处于初级阶段。鉴于干扰素-γ在NK细胞介导的适应性免疫反应调节中的重要作用,很自然地设想ILC1产生的干扰素-γ也有类似的作用。然而,目前还没有研究支持这一说法。
事实上,由于这些细胞的高度表型相似性,NK细胞和ILC1细胞在抗肿瘤免疫中的相对贡献的评估变得复杂。值得注意的是,I型ILC的TRAIL+成员也可能抑制T细胞反应。
关于ILC2s,这些细胞产生的2型细胞因子通常抑制1型抗肿瘤反应,促进肿瘤生长。然而,在实验性转移的小鼠B16F10模型中,肺ILC2s细胞产生的IL-5已被证明能促进嗜酸性粒细胞的募集和肺部肿瘤的清除。
一项研究表明,ILC3s在抗肿瘤免疫中具有积极作用,化疗与肿瘤靶向抗体联合治疗可延缓B16皮下肿瘤的生长。在这种情况下,肿瘤清除依赖于CD90+NK1.1−RORγt+天然淋巴细胞,并与肿瘤组织内巨噬细胞浸润增加有关。
另一份报告显示,NKp46+ILC3能抑制皮下注射的分泌IL-12的B16F10肿瘤细胞的生长。在缺乏T细胞或常规NK细胞的情况下,分泌IL-12的肿瘤仍然受到抑制,表明NKp46+ILC3s通过上调肿瘤内皮细胞表面黏附分子来介导其抗肿瘤作用。
类似地,有研究发现人类非小细胞肺癌(NSCLC)组织中存在的NCR+ILC3产生的可溶性因子可以激活间充质干细胞和内皮细胞。在这项研究中,肿瘤组织中ILC3的数量与TLS三级淋巴结构(TLS)的密度相关,TLS是一种异位淋巴器官,与NSCLC患者的良好预后相关。非常有趣的是,晚期肿瘤中肿瘤浸润NCR+ILC3s的频率较低,提示NCR+ILC3s可能与NSCLC患者良好的预后相关。
总结
ILC起着哨兵的作用,一旦宿主体内平衡受到干扰,就会迅速做出反应。它们快速而有力的反应可以暂时控制危险,并提醒其他免疫细胞提供长期保护(Fig 9.4)。
长期以来,NK细胞一直被认为是抗癌症发展的最强大的先天守护者。然而,最近ILC家族的扩大可能会对这一观点提出挑战,并提出不同ILC亚群,特别是NK细胞和ILC1的相对贡献的问题。
值得注意的是,尽管NK细胞与ILC1有相当大的转录重叠,但NK细胞能表达更高的转录本,编码细胞毒性机制的蛋白,以及参与检测转化细胞的细胞表面受体。
此外,辅助性ILC是驻留在组织中的细胞,它只会感觉到它们所在的特定器官的变化,而常规的NK细胞在血液中循环,可以扫描全身是否存在受损细胞。因此,NK细胞可能是清除肿瘤的最有效的ILC亚群。
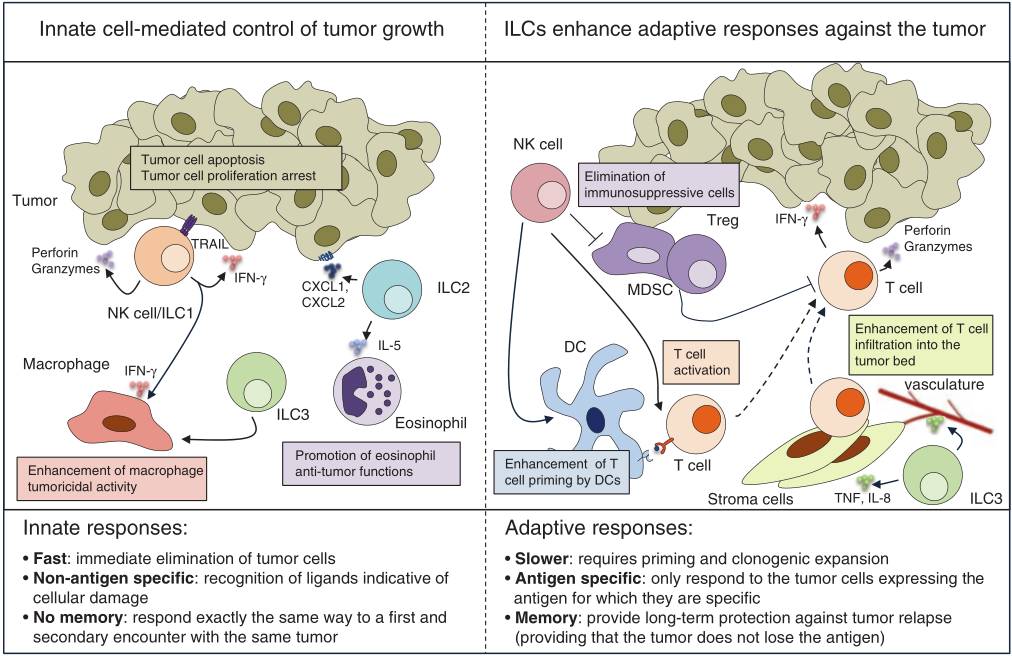
Fig 9.4 固有的和适应性的淋巴细胞有助于癌症的免疫监控。左图:ILC可直接诱导肿瘤细胞凋亡和/或生长停滞,也可刺激其他固有细胞以确保癌细胞的快速清除。I型ILCs通过细胞毒颗粒途径(穿孔素/颗粒酶)或死亡配体途径(TRAIL)对肿瘤细胞产生直接的细胞毒作用。值得注意的是,传统NK细胞和ILC1细胞都有这种细胞毒活性,但NK细胞目前被认为是更有效的杀手。I型ILC产生的干扰素-γ也可直接抑制肿瘤生长,并可能刺激巨噬细胞的杀瘤活性。ILC2可能通过分泌CXCL1和CXCL2直接诱导表达CXCR2的肿瘤细胞凋亡。ILC2还分泌IL-5,从而招募嗜酸性粒细胞。ILC3s可增加巨噬细胞对肿瘤的浸润。右图:ILC刺激T细胞反应,从而确保对癌细胞的长期保护。NK细胞能激活DC,增强抗肿瘤T细胞反应,还能杀伤免疫抑制细胞,如树突状细胞(Tregs)和髓系抑制细胞(MDSC)。ILC3激活基质和内皮细胞,从而促进免疫细胞向肿瘤区域的浸润。
ILC在功能性适应性免疫中的重要性最近受到质疑,因为在一组SCID患者中发现存在ILC缺陷似乎没有严重的临床后果。本研究对18例IL2RG或JAK3突变的患者进行了7-39年的随访,这些患者在不进行骨髓清除术的情况下接受了造血干细胞移植治疗。然而,这个队列太小,不能说明ILC在肿瘤免疫监测中的作用,这样的研究也可能需要更长的随访时间。
也许证明细胞毒性ILC对人类癌症免疫监测的重要性的最有说服力的证据来自一项前瞻性研究,该研究表明,外周血淋巴细胞自发细胞毒性活性高的个体患癌症的风险显著降低。在胃肠道肉瘤患者中,NK细胞浸润与确诊时无转移相关,而在肾癌中,肺转移中NK细胞密度高与生存期延长相关。
相反,NSCLC的一项研究表明NK细胞数量和临床结果之间没有相关性。对晚期癌症缺乏NK细胞活性可能是由于(1)肿瘤通过免疫编辑过程选择抗药性变异克隆而逃脱NK细胞免疫监视和/或(2)肿瘤微环境中NK细胞耗尽,其中多种机制导致NK细胞功能受阻。
腺苷和转化生长因子-β是两个被证实影响NK细胞抗肿瘤活性的可溶性因子。此外,NK细胞在人类肿瘤组织中的低浸润可以解释它们对实体瘤进展的影响有限。然而,NK细胞似乎对转移性疾病和血液恶性肿瘤特别有效。
辅助性ILC亚群参与人类癌症发生发展的证据有限。在人类结直肠癌、乳腺癌患者的原发肿瘤和非小细胞肺癌(NSCLC)组织中已经观察到ILC3的浸润。但重要的是,辅助类ILC在恶性疾病中的功能仍不清楚,可能取决于癌症的类型和分期。
本章的重点是ILC在检测和消除新生肿瘤中的保护作用,请读者参考其他综述,以完整讨论辅助性ILC促进或抑制肿瘤生长的相反的两种能力。
肿瘤微环境可能通过抑制ILC的抗肿瘤活性(如干扰素-γ的释放)或通过影响ILC的可塑性来操纵ILC。事实上,一些ILC亚群并不稳定,这取决于细胞因子所在的微环境,NK细胞可以获得ILC1表型,ILC2s可以转化为ILC1或ILC3s,ILC3s可以转化为ILC1。急性髓系白血病患者血液中ILC功能和亚型组成失调的报道支持了肿瘤可能通过调节ILC逃脱免疫监视的假设。
ILC是一个有趣的临床靶点,因为它们对刺激立即产生反应,并且它们的反应不是由抗原驱动的。它们产生的大量细胞因子可以改变肿瘤微环境,唤醒髓系细胞和适应性淋巴细胞的抗癌能力。
然而,在这些细胞能够有效地应用于临床之前,需要更好地了解辅助类ILC的功能、生物学特性和可塑性。另一方面,操纵NK细胞已经成为癌症患者非常有前景的治疗选择。利用NK细胞抗肿瘤活性的多种策略已经在其他章节有描述,并且是本卷的另一章的主题。
重要的是,目前开发的一些针对T细胞或NK细胞的策略,如抗PD1单抗、NKG2D双特异性结合分子或细胞因子输注也可能影响ILC的功能。随着我们对ILC家族知识的增加,这些细胞在癌症免疫治疗领域的作用可能也会有所提升。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab学术星球现已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。
关注本号~

加入读者交流群~

加入知识星球~
用于OncoLab读者交流互助永久免费
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏