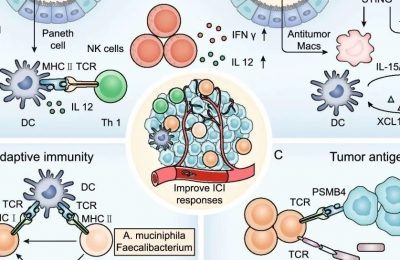
15.1 引言
在全球范围内,大约六分之一的新的癌症诊断可归因于一种特定的感染病原体(Fig. 15.1)。人类乳头瘤病毒(HPV)导致了大约30%癌症相关的感染,包括宫颈癌、阴道癌、外阴癌、肛门癌和口咽癌,占全球所有癌症的近5%。在女性群体中,大多数HPV诱发的癌症是宫颈癌;在男性群体中,大多数HPV相关的恶性肿瘤是口咽癌(Fig. 15.2)。尽管有预防性的HPV疫苗以及检测下生殖道中HPV的筛查方法,但在资源匮乏的环境中,宫颈癌是女性因癌症死亡的第二大常见原因。
接触HPV是在首次性行为发生时,基本上是地方性疾病。感染后通常是无症状的,虽然大多数感染是暂时的,但痊愈可能需要1-2年。年长的女性需要更长的时间来清除感染,吸烟者和患有潜在免疫抑制的女性也是如此。这些感染的临床沉默性质有助于维持大量可传播HPV的群体数量。此外,在符合条件的美国队列研究中,9-26岁的年轻人的预防性疫苗接种率一直处于次优水平。在2015年,有43%的女孩和28%的男孩完成了三联疫苗接种方案中的所有三种疫苗接种。现有的预防疫苗 Gardasil©和Cervarix©被批准用于预防宫颈癌、外阴癌、阴道癌和肛门癌。由于HPV是口咽鳞状细胞癌(OSCC)亚群的潜在病因,而在大多数年轻、不吸烟和不酗酒的男性中,它们仅限于腭扁桃体和舌根的上皮细胞,因此目前正在研究它们用于口咽癌的预防作用。
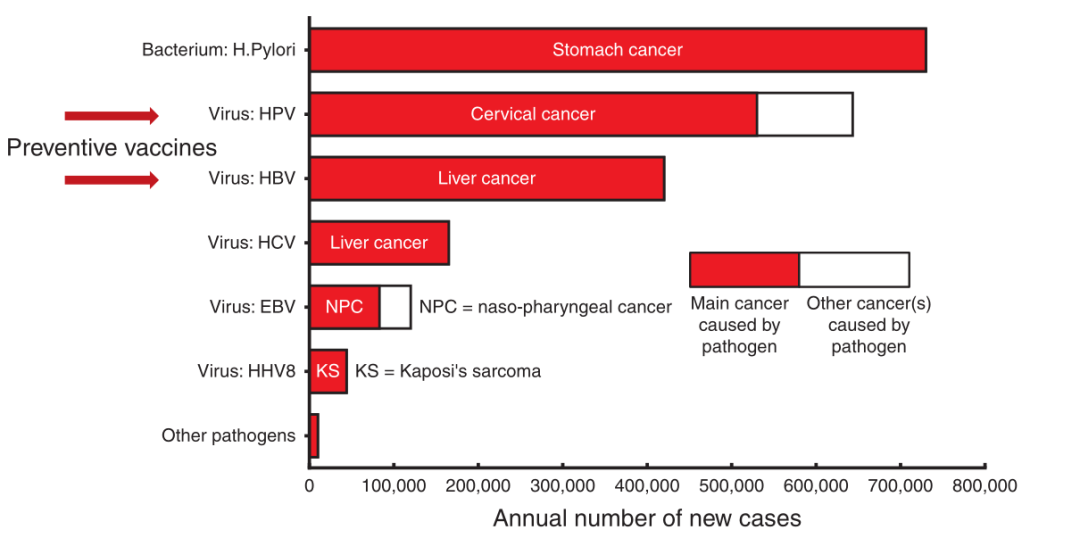
Fig 15.1 2012年全球病原体引起的人类恶性肿瘤发病率
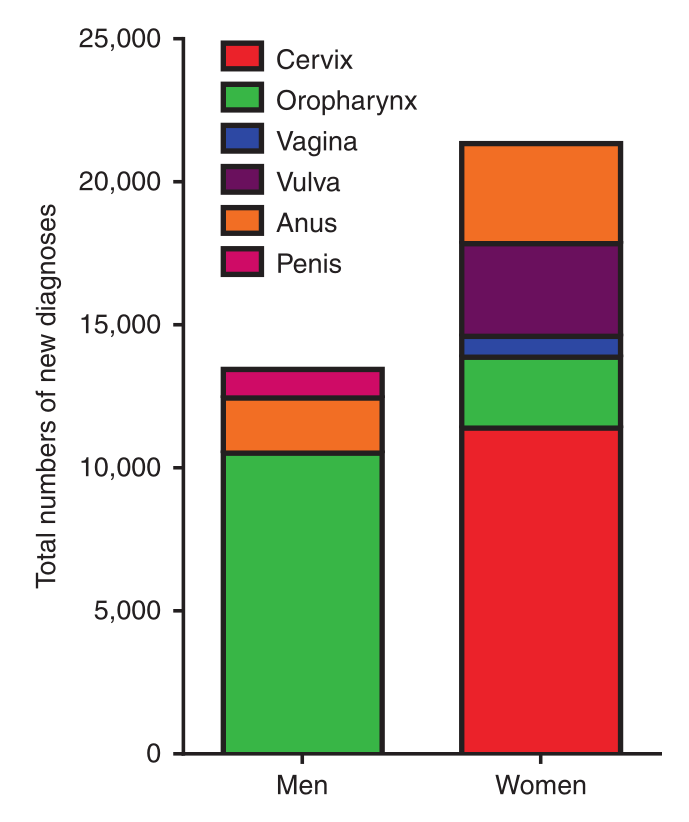
Fig 15.2 2009年与人乳头瘤病毒相关的新癌症数目
15.1.1 人乳头瘤病毒的感染生物学
人乳头状瘤病毒(HPV)是一种无包膜的双链DNA病毒,对黏膜组织具有嗜性。基因组由三个功能区域组成:(A)非编码调控区;(B)早期蛋白区域,编码6个早期蛋白(E1、E2、E4-E7);以及(C)晚期区域,编码病毒衣壳蛋白L1和L2。HPV感染基底上皮(皮肤或粘膜)细胞。目前已鉴定出200多种HPV基因型。致癌基因型包括HPV16、18、31、33、35、39、45、51、52、56、58、59和66。
宫颈鳞癌、其他肛门生殖道癌和头颈癌的发生是在持续感染致癌性HPV的情况下发生的。事实上,所有宫颈鳞状细胞癌(SCCx)及其前驱病变–高度鳞状上皮内病变/宫颈上皮内瘤变2/3 (HGSIL/CIN2/CIN3)都是由HPV引起的,最常见的是HPV 16(Fig. 15.3)。大多数宫颈癌都与HPV 16和18型有关。
宫颈癌和HGSIL/CIN2/CIN3的发展都与HPV基因组整合到宿主基因组中以及随后两个HPV早期基因产物E6和E7的表达有关,这两个基因产物分别使p53和pRb失活。病毒整合位点虽然随机分布在人类基因组内,但主要发生在人类DNA容易断裂的位点(例如,脆弱位点),并且似乎只影响HPV基因组本身的表达。具体地说,E1和E2在整合过程中最常被破坏,而E6和E7病毒癌基因被保留,导致结构性表达。E6和E7的表达在功能上是启动和维持肿瘤转化所必需的。在形态学上,在细胞水平上,高度上皮内病变的特点是核浆比高。而在组织学上,高度恶性病变表现为全厚度,细胞不成熟,有丝分裂活跃(Fig. 15.4)。
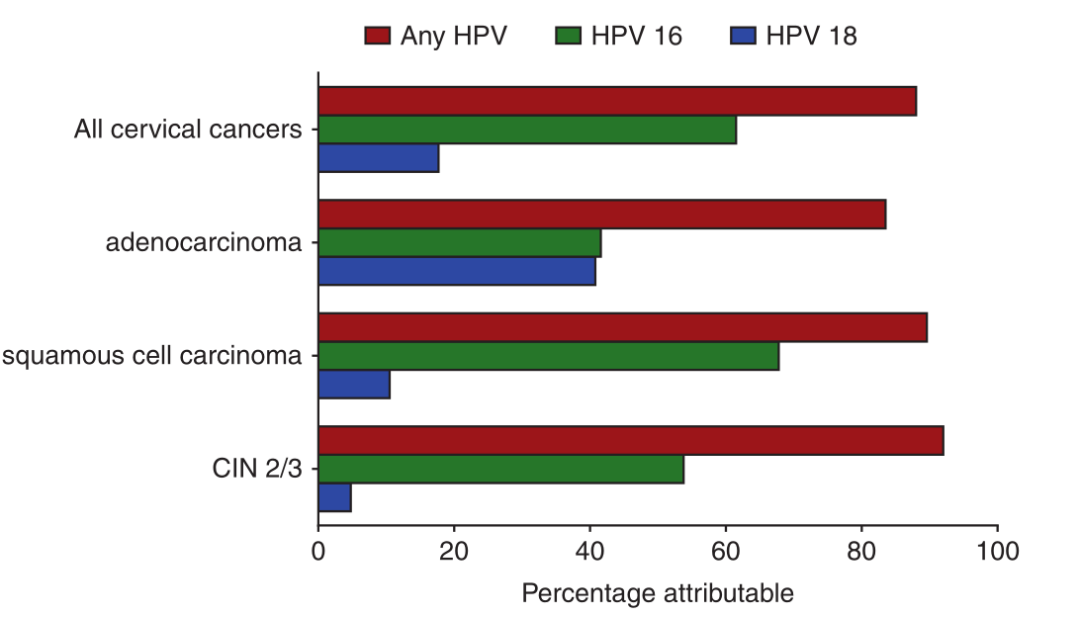
Fig 15.3 最常与宫颈疾病相关的HPV基因型别
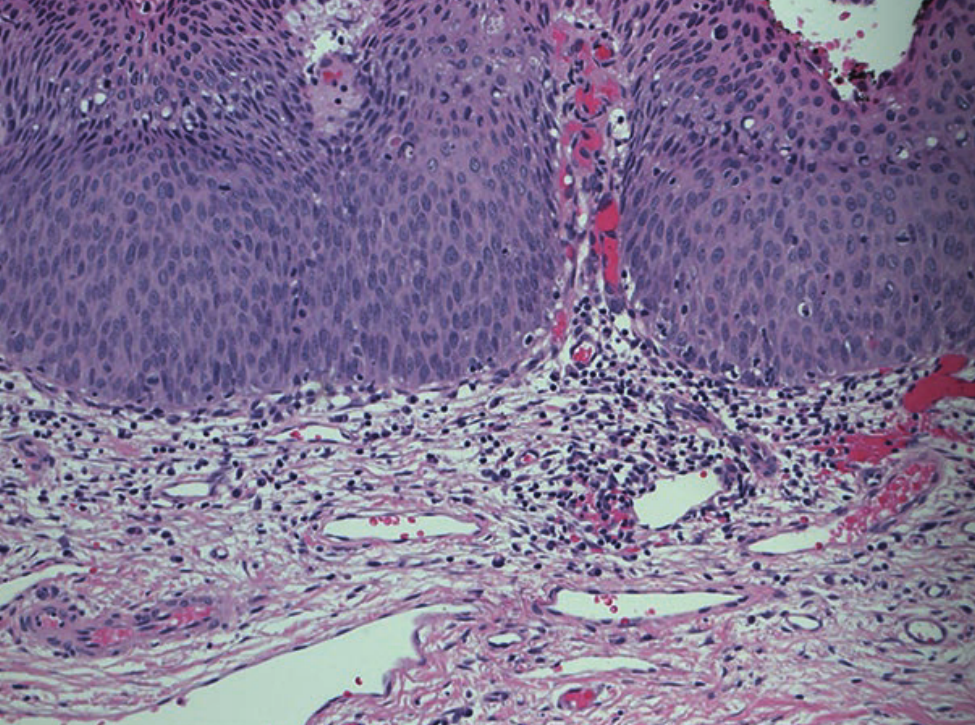
Fig 15.4 放大20倍CIN-2/CIN3组织苏木精-伊红染色
15.1.2 自然感染中的系统免疫反应
在HPV自然感染的背景下,对疾病起始和持续发展过程中所需的对HPV抗原的体液和适应性系统内源性免疫反应都很弱。病毒清除后,50-70%的人可检测到抗体滴度。由自然感染引起的记忆B细胞产生的抗体大多数亲和力低,是非中和的,不一定能预防相同HPV基因型的再次感染。同样,T细胞对病毒抗原的反应是比较弱的,需要体外刺激才能被检测到,而且不能可靠地区分病变会消退的人和不会消退的人。事实上,持续性的HPV感染和侵袭前的HPV病变仅限于鳞状上皮,表现在非炎症性环境中,没有全身性病毒血症。感染在解剖学上仅限于粘膜上皮,不会引起全身性症状。
通过体外刺激,在HPV 16+CIN2/CIN3携带者和宫颈癌患者的外周血中检测到了HPV 16 E7特异性细胞毒T细胞。然而,到目前为止,血液中对E7的反应程度和临床结果之间还没有明确的联系。相比之下,外周血细胞毒性T细胞对HPV 16 E6的反应与临床结果有关。特别是,CD4+T细胞对E6 IS的反应与更好的临床结果相关。相反,功能受损的E6特异性CD4+T细胞反应与宫颈癌相关。
尽管血液中HPV特异性记忆T细胞很少见,但一部分CIN2/CIN3携带者确实产生了有效的反应;并不是所有的CIN2/CIN3病变都进展为浸润性癌症。我们和其他人已经报道,在4-6个月的时间内,~35%的CIN2/CIN3病变经历了自发消退。同样,在一项针对HPV 16/18 E6和E7的治疗性合成DNA疫苗VGX-3100的第二阶段临床试验中,于计划的标准治疗切除之前,HPV 16或18+CIN2/CIN3携带者中,30%的接受安慰剂的受试者经历了组织病理学退化。与其他HPV基因型相比,由HPV 16单一感染所引起的病变不太可能消退:在这段时间内,大约有20-25%的与HPV16相关的CIN2/CIN3病变消退。
15.1.3 对自然感染的组织定位免疫反应
在血液中检测到的自然产生的T细胞反应的大小和广度都不是宫颈侵袭前HPV疾病消退的有力预测因素,这一事实提出了一个问题,即是否有可能在靶病变中识别可以预测疾病结局的因素或是消除感染、早期恶性肿瘤或癌症的免疫反应的特征。对HPV损害的组织研究正在确定与临床结果相关的因素。在没有消退的CIN2/CIN3病变中,虽然CD8+T细胞在粘膜中的浸润很强,但它们主要局限于间质,不能进入病变上皮。另一方面,上皮内CD8+T细胞的存在与随后的消退有关。同样,在HPV相关的宫颈癌和口咽癌中,肿瘤内CD8+T细胞的存在与较好的预后相关。尽管存在肿瘤浸润性T细胞,但持续的HPV感染可能会导致癌症的生长,这很可能是肿瘤微环境中免疫耐受的结果,这些因素包括调节性T细胞的存在,CTLA-4和PD-1的表达,或者细胞表面MHC-I类分子的下调。定量方法,包括图像分析导向的快速免疫激光捕获显微切割,将使分析从特定组织学背景中分离出特定的细胞亚群成为可能,并将它们与临床结果相关联。最后,对疾病所需的病毒蛋白的系统免疫反应很弱,不能可靠地预测临床行为,这突显了更好地了解粘膜微环境的必要性。
15.1.4 预防性疫苗
目前预防HPV疾病的策略包括筛查、使用细胞学或HPV检测,又或是两者结合。预防感染致癌HPV基因型的疫苗由L1的非感染性重组病毒样颗粒(VLP)组成,L1是两种HPV衣壳蛋白之一。这些VLP不含病毒DNA,因此完全不具感染性和致癌性。目前,有三种构建物可供选择:Cervarix©,靶向HPV 16和18型(bHPV)并辅以ASO4佐剂;Gardasil4©,靶向HPV 6、11、16和18型(qHPV);Gardasil9©,靶向HPV 6、11、16、18、31、33、45、52和58型(nHPV)(Table. 15.1)。所有配方都对HPV感染非常有效,不仅仅在宫颈,而且在其他解剖部位都非常有效,且无论男女。这些疫苗产生的强健抗体反应比自然感染引起的抗体反应大1-2个对数。在已知以前接触过HPV的人中,单次接种qHPV大大提高了抗体反应的强度和质量。与自然感染产生的非中和抗体不同,接种疫苗产生的抗体是中和抗体。虽然bHPV和qHPV疫苗都显示出对其他HPV类型的交叉保护,但Cervarix©对HPV 31、33、45、51和52提供交叉保护,而Gardasil4©被证明只对HPV 31具有交叉保护作用。Cervarix©的广泛交叉反应很可能归因于其佐剂ASO4,这是一种TLR4激动剂。现有的预防性疫苗Gardasil©和Cervarix©没有治疗效果。然而,来自四价HPV疫苗研究的新证据表明,CIN2/CIN3切除治疗后接种预防性疫苗可显著降低疾病复发的可能性。这种保护作用的作用方式尚不清楚,目前正在积极调查中。
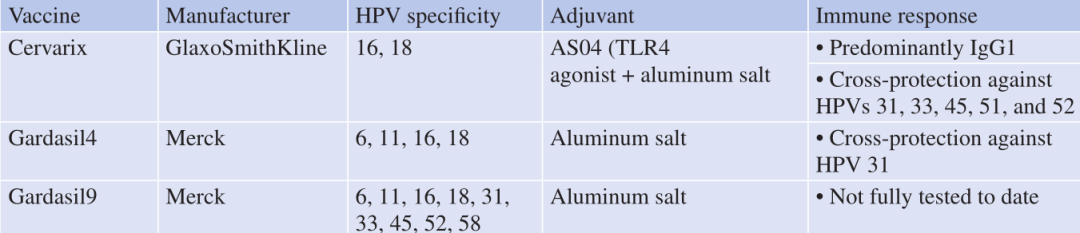
Table. 15.1 现有的预防性HPV疫苗
15.1.5 治疗性疫苗
与预防性疫苗不同,新的治疗性疫苗的开发重点是针对E6和E7的。效应T细胞对这些病毒、非自身癌蛋白的反应可能在介导病变消退中发挥作用,这些蛋白由转化细胞结构性表达。为患有侵袭前疾病的人提供了一个机会来证实免疫治疗策略的有效性。这些病变是可以检测到的且具有特异性的,这为在干预前后评估相关组织提供了机会。此外,有一部分病变会消退,因此可用于预测预处理和诱导免疫反应的治疗效果。研究组织还将提供确定HPV疾病不同阶段介导的免疫抑制机制的方法。
现已对几种平台的疫苗进行了评估,包括裸露DNA肌肉注射(IM)、DNA电穿孔IM注射、皮下注射包括改良的Vaccinia Ankara(MVA)病毒的病毒载体、通过划痕和IM注射注射的痘苗病毒(TA-HPV),皮下注射佐剂的多肽,细菌结构例如单核细胞增生李斯特氏菌等。尽管从临床前期模型获得的数据来看前景较好,但在人类身上作用效果不明显。到目前为止,在任何阶段的HPV疾病中,疫苗诱导的免疫反应都是微乎其微的。回想起来,这种明显的差异可能是由试验设计的不合理造成。大多数试验采用外周性免疫治疗,旨在评估传统的、相对二元的结果,例如血液中病毒特异性CD8+T细胞免疫反应的强弱和病变退化与持久性的对比。事实上,在对异源DNA引物、重组痘苗(TA-HPV)进行的I期临床试验评估中,HPV 16+CIN2/CIN3携带者中的这类人群:在计划的标准治疗切除之前,组织结果确实存在残留异型增生的患者中,接种疫苗后组织切除标本显示目标皮损中的免疫学发生了剧烈变化。这些变化包括间质和上皮室中强大的免疫细胞浸润,仅限于残留的CIN2/CIN3,并不直接累及邻近的正常粘膜。这些浸润物由克隆扩张的T细胞体组成,在许多情况下被区分成三级淋巴结构或直接生发中心,并具有TH-1表型。这项研究确定了两个关键点:一是有可能引起对以慢性方式存在的抗原产生效应性反应,二是外周血、肌肉注射疫苗产生的T细胞可以运输到相关的免疫靶点。在残留CIN2/CIN3的切除组织中,这些病变大量浸润CD8+T细胞,它们与凋亡的鳞状上皮细胞共存。这一发现表明,接种疫苗附近的计划切除基本上阻断了组织端点。根据常规方法,即外周血T细胞对疫苗抗原的反应及组织学的完全消退,该方案是失败的。然而,考虑到在目标组织中的发现,没有办法得出疫苗接种“失败”的结论。这一发现为后续侵袭前HPV疾病患者临床试验的设计提供了依据–在治疗干预后的较长时间间隔内获得组织终点。虽然测量的是外周血T细胞反应,但也包括病变微环境的定量测量。
随后的一项随机、安慰剂对照的第二阶段试验测试了使用合成DNA疫苗VGX-3100进行的HPV16或18+CIN2/CIN3治疗性疫苗接种,该疫苗先肌注后电穿孔,报告显示接种对象的组织学消退率为49%。尽管接受安慰剂治疗的受试者中有一部分也有组织学消退,但病毒清除率不同;在组织学消退的接种疫苗受试者中,80%的人无法检测到HPV,而自发消退的受试者中,这一比例为30%。在接种疫苗的受试者中可检测到的病毒的伴随清除表明,与接受安慰剂的人相比,接种疫苗的受试者的复发率可能较低;在切除侵袭前病变后持续的HPV感染是预测中复发风险最高的因素。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab学术星球现已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
用于OncoLab读者交流互助永久免费
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏