01
Gastroenterology. 20221126
✦
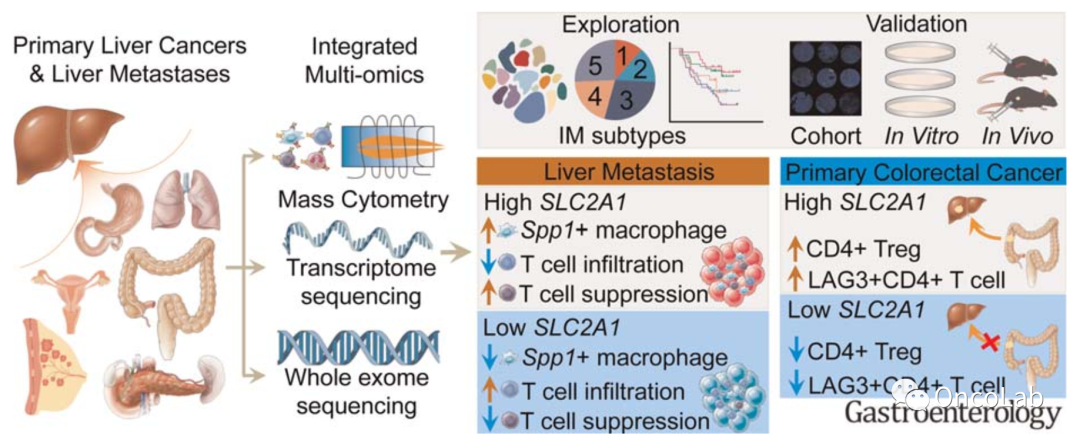
Integrated Multi-Omics Landscape of Liver Metastases
肝转移的整合多组学景观
Gastroenterology. 2023 Mar;164(3):407-423.e17.
doi: 10.1053/j.gastro.2022.11.029.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36574521/
Abstract
背景&目的:对各种肝转移瘤(LMs)中复杂的免疫微环境(IM)缺乏透彻的了解会导致治疗不当和预后不理想。我们旨在表征IM的各种亚型并研究肝转移的潜在机制。
方法:应用质谱细胞术表征原发性肝癌和肝转移队列的免疫景观。转录组和全外显子组测序用于探索不同IM亚型形成的潜在机制。采用单细胞转录组测序、多重荧光免疫组化、细胞培养、小鼠模型、蛋白质印迹、定量聚合酶链反应和免疫组化等实验进行验证。
结果:在100例LMs和50例原发性肝癌中发现了5种IM亚型。具有终末衰竭(IM1)或罕见T细胞炎症(IM2和IM3)免疫特征的患者预后较差。恶性亚型的形成与肿瘤内部异质性增加、体细胞TP53、KRAS、APC、PIK3CA突变丰富以及缺氧信号过度激活有关。SLC2A1通过增加肝转移病灶中Spp1+巨噬细胞的比例及其对T细胞的抑制作用促进免疫抑制。此外,SLC2A1在原发性结直肠癌中通过诱导Tregs和LAG3+CD4+ T细胞等调节性T细胞促进免疫逃逸和肝转移。
结论:该研究提供了肝转移的整合多组学景观,揭示了恶性IM亚型形成的潜在机制,并确认了SLC2A1在原发肿瘤和肝转移病灶中调节肿瘤微环境重构的作用。
Keywords:
肝转移;多组学;SLC2A1; 肿瘤免疫微环境
02
Nat Immunol. 20221221
✦
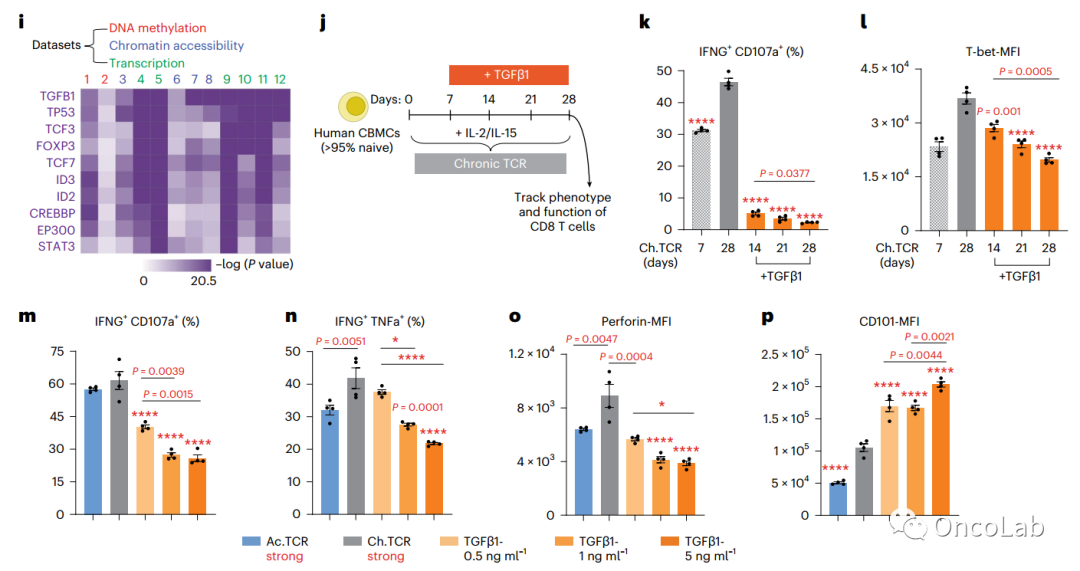
Rebalancing TGFβ1/BMP signals in exhausted T cells unlocks responsiveness to immune checkpoint blockade therapy
在耗竭性T细胞中重新平衡TGFβ1 / BMP信号可解锁对免疫检查点阻断治疗的反应
Nat Immunol. 2023 Feb;24(2):280-294.
doi: 10.1038/s41590-022-01384-y.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36543960/
Abstract
T细胞功能障碍可阻碍免疫系统对慢性感染和癌症的清除。此外,功能失调的CD8+ T细胞中的表观遗传编程限制了它们对免疫疗法的反应,包括免疫检查点阻断(ICB)疗法。然而,目前尚不清楚哪些上游信号驱动了功能失调的表观遗传程序的形成,以及靶向治疗这些信号是否可以将终末功能失调的T细胞重塑为可对ICB反应的状态。在这里,我们建立了一种稳定的人类T细胞功能障碍的体外模型系统,并表明效应后CD8+ T细胞中的慢性TGFβ1信号通过稳定的表观遗传变化加速了T细胞的终末功能障碍。相反,在阻断TGFβ1的同时增强骨形态发生蛋白(BMP)信号传导,在慢性刺激的人CD8+ T细胞中保留了效应和记忆相关程序,并且可诱导T细胞对肿瘤的显著反应,并可在慢性病毒感染期间协同ICB反应。因此,重新平衡TGFβ1 / BMP信号提供了一种新方法来拯救功能失调的CD8+ T细胞并增强T细胞免疫疗法。
03
Cell Death Differ. 20221220
✦
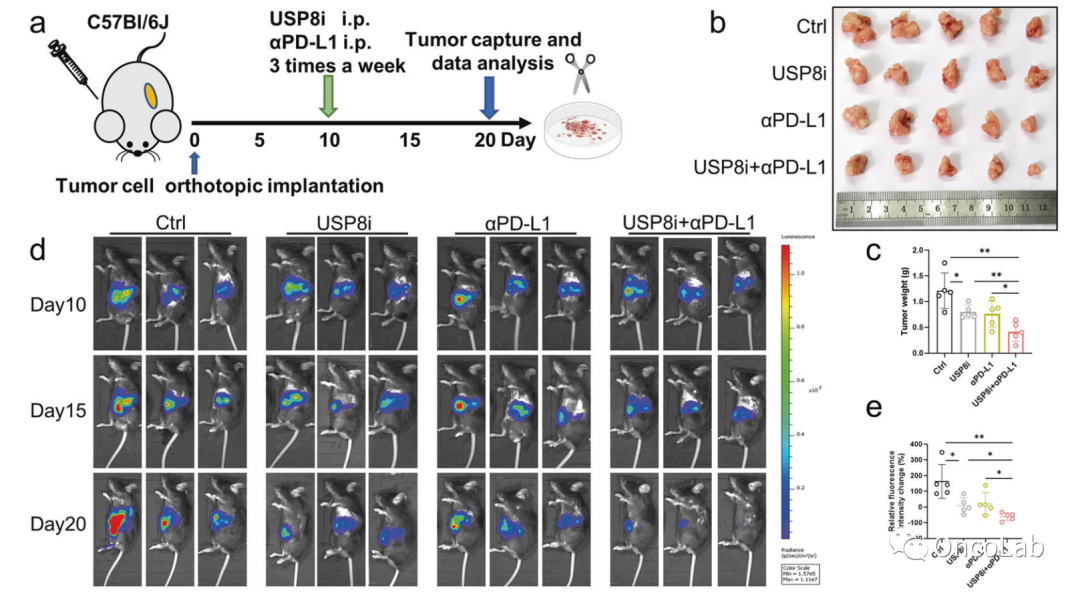
Targeting ubiquitin-specific protease 8 sensitizes anti-programmed death-ligand 1 immunotherapy of pancreatic cancer
靶向泛素特异性蛋白酶8可在胰腺癌中增效抗PD-L1免疫疗法
Cell Death Differ. 2023 Feb;30(2):560-575.
doi: 10.1038/s41418-022-01102-z.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36539510/
Abstract
PD-1及其配体PD-L1可帮助肿瘤细胞逃避免疫监视,被视为抗肿瘤免疫治疗的重要靶点。PD-L1的翻译后修饰在免疫抑制方面具有潜在价值。在这里,我们确定了泛素特异性蛋白酶8(USP8)可去泛素化PD-L1。与正常组织中相比,胰腺癌组织的USP8水平显着增加。临床上,USP8的表达与众多患者来源的胰腺癌队列中的肿瘤淋巴结转移的分期显著相关。同时,USP8缺乏可以以免疫依赖的方式减少肿瘤侵袭和迁移以及肿瘤大小,并提高抗肿瘤免疫原性。USP8抑制剂预处理导致肿瘤发生减少,并且Usp8敲低后的肿瘤接种的免疫功能正常的小鼠表现出更长的生存期。此外,USP8与PD-L1具有正向相互作用,在胰腺癌中可通过抑制泛素化调节的蛋白酶体降解途径上调PD-L1的表达。USP8抑制剂和抗PD-L1联合治疗可通过激活细胞毒性T细胞有效抑制胰腺肿瘤生长,这种抗肿瘤免疫主要依赖于PD-L1通路和CD8+T细胞。我们的研究结果强调了靶向USP8的重要意义,USP8可以使胰腺癌对抗PD-L1免疫疗法更敏感,这种尝试可能成为未来治疗胰腺肿瘤的新策略。
04
Immunity. 20221219
✦
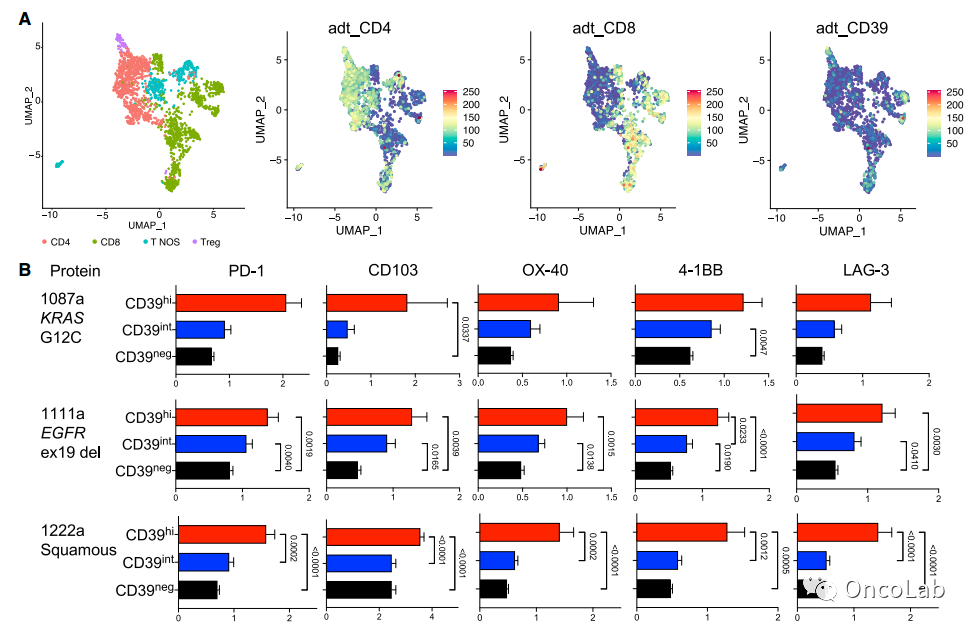
The ectonucleotidase CD39 identifies tumor-reactive CD8+ T cells predictive of immune checkpoint blockade efficacy in human lung cancer
外核苷酸酶CD39鉴定肿瘤反应性CD8+ T细胞,从而预测人类肺癌中免疫检查点阻断疗法的功效
Immunity. 2023 Jan 10;56(1):93-106.e6.
doi: 10.1016/j.immuni.2022.12.001.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36574773/
Abstract
为了推进癌症免疫疗法,更精确地鉴定肿瘤反应性T细胞非常必要。CD39表达有希望成为肿瘤反应性CD8+ T细胞的鉴定标志。在这里,我们全面分析了CD39在人类肺癌中的表达。CD39表达富集于具有耗竭性、肿瘤反应性和克隆扩增特征的CD8+ T细胞。对440份肺癌生物标本进行了流式细胞术,结果显示CD39+ CD8+ T细胞与一些肿瘤特征(如PD-L1、肿瘤突变负荷和驱动突变)之间的相关性较弱。免疫检查点阻断(ICB)可增加肿瘤内的CD39+ CD8+ T细胞。而CD39+ CD8+ T细胞的基线频率越高,ICB治疗的临床结局就越好。此外,在非小细胞肺癌的III期临床试验中发现,CD39+ CD8+ T细胞的基因表达特征可预测ICB治疗的潜在效果。这些发现证明了CD39可成为人类肺癌中肿瘤反应性CD8+ T细胞标志物的可能性。
Keywords:
CD8+ T 细胞;T细胞受体;免疫检查点阻断;非小细胞肺癌;肿瘤突变负荷
05
Sci Adv. 20221216
✦
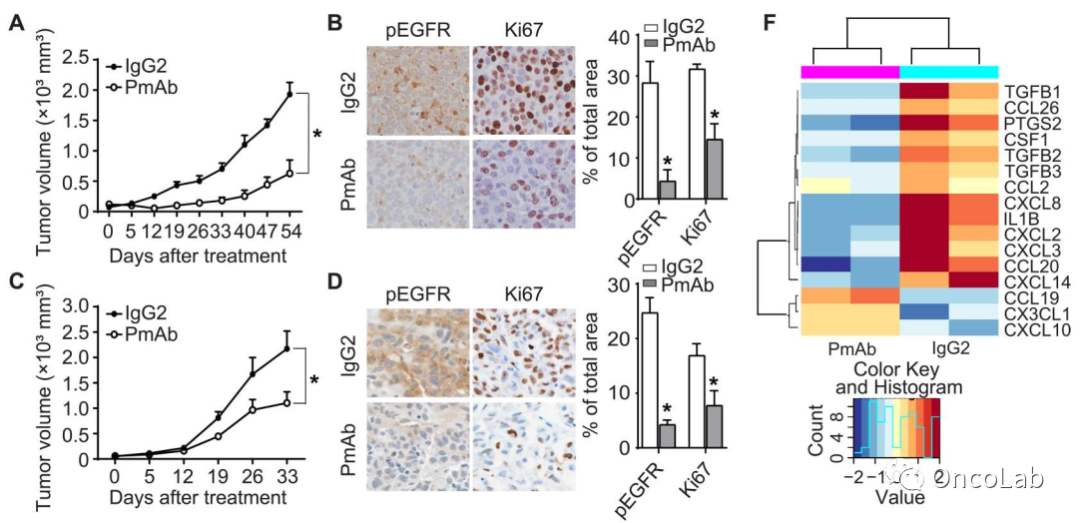
EGFR is a master switch between immunosuppressive and immunoactive tumor microenvironment in inflammatory breast cancer
EGFR是炎性乳腺癌中免疫抑制性和免疫激活性肿瘤微环境之间的主开关
Sci Adv. 2022 Dec 16;8(50):eabn7983.
doi: 10.1126/sciadv.abn7983.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36525493/
Abstract
炎性乳腺癌(IBC)是最具侵袭性的乳腺癌亚型,由免疫抑制肿瘤微环境(TME)驱动。目前对IBC的治疗效果有限。在一项临床试验(NCT01036087)中,抗EGFR抗体联合新辅助化疗(实施局部治疗方法前所做的全身化疗)在具有三阴性受体状态的IBC患者中产生了有史以来最高的病理完全缓解率。我们研究并确定了这种良好临床结果背后的分子和免疫机制。使用新型人源化IBC小鼠模型,我们发现EGFR靶向治疗通过增加细胞毒性T细胞和减少免疫抑制调节性T细胞以及M2型巨噬细胞来重塑IBC的TME。这些变化是由于转录因子EGR1调节的免疫抑制趋化因子的表达减少导致的。我们还证明了,通过抗EGFR抗体诱导免疫激活型的的IBC TME,提高了抗PD-L1抗体疗法的抗肿瘤功效。我们的研究结果为EGFR靶向治疗联合免疫检查点抑制剂治疗癌症患者的临床试验奠定了基础。
06
Nature. 20221214
✦
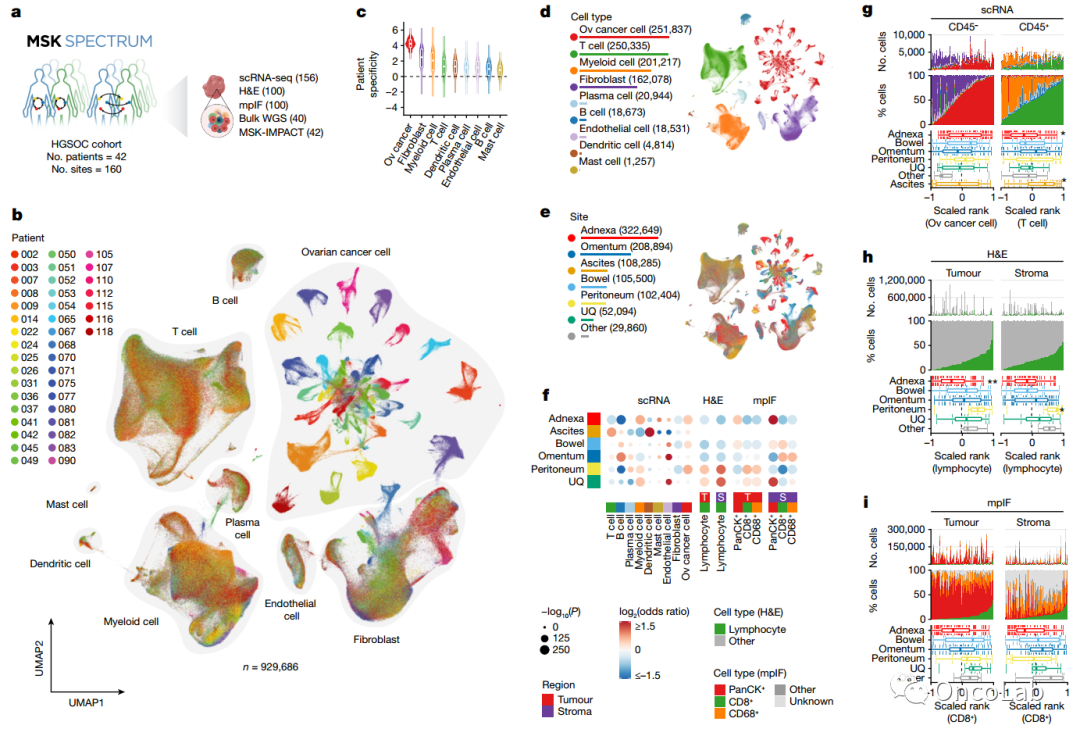
Ovarian cancer mutational processes drive site-specific immune evasion
卵巢癌突变过程驱动位点特异性免疫逃逸
Nature. 2022 Dec 14.
doi: 10.1038/s41586-022-05496-1.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36517593/
Abstract
高级别浆液性卵巢癌(HGSOC)是一种基因组不稳定的典型癌症,可表现为不同的突变驱使的肿瘤异型性和腹膜内扩散。免疫疗法在高级别浆液性卵巢癌中的疗效有限,突显了评估突变过程和肿瘤病灶的解剖部位如何决定肿瘤微环境免疫状态的迫切需要。在这里,我们对来自42名未经治疗的HGSOC患者的160个肿瘤部位进行了全基因组测序,单细胞RNA测序,数字组织病理学和多重免疫荧光的综合分析。缺乏同源重组修复(HRD)的基因突变(类似BRCA1)和HRD-Del(类似BRCA2)的肿瘤具有炎症信号和持续的免疫编辑,表现为HLA多样性的丧失和高度分化的功能失调CD8+ T细胞的肿瘤浸润。相比之下,携带折返倒位的肿瘤表现出增高的免疫抑制性TGFβ信号和免疫排斥,它们的肿瘤免疫微环境中主要是幼稚/干细胞样的T细胞和记忆T细胞。肿瘤的特定解剖部位与表型状态有关,附件肿瘤和远端腹膜病灶之间的组成、拓扑和功能都有明显差异。我们的发现表明解剖部位和突变过程是HGSOC进化出表型差异和免疫抵抗机制的决定因素。我们的研究提供了一种多组学细胞表型的数据基础,有望从中开发和诠释未来的个性化免疫治疗方法和早期检测研究。
07
Pharmacol Ther. 20221213
✦
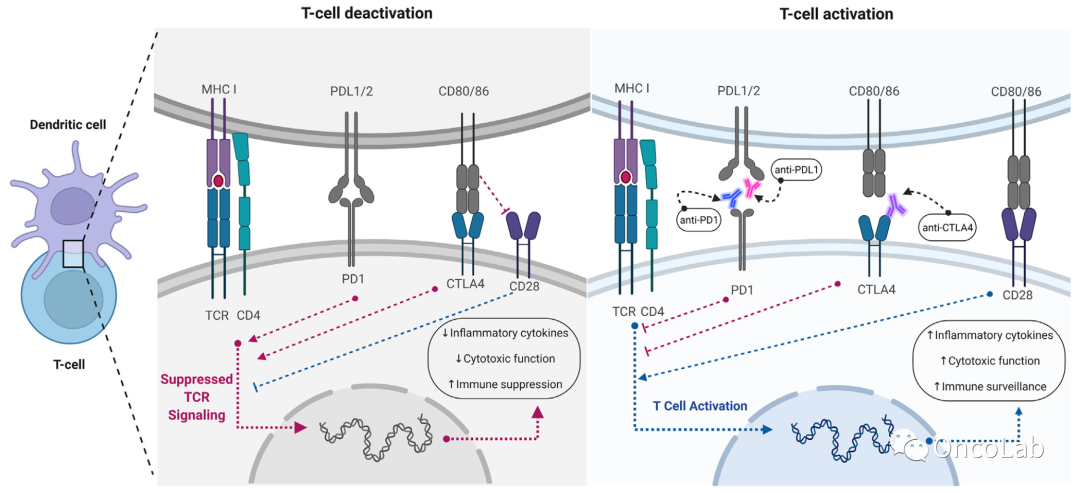
Tumor-derived extracellular vesicles in the colorectal cancer immune environment and immunotherapy
结直肠癌免疫环境与免疫治疗中的肿瘤源性外泌体
Pharmacol Ther. 2022 Dec 13;108332.
doi: 10.1016/j.pharmthera.2022.108332.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36526013/
Abstract
尽管在结直肠癌(CRC)的筛查、诊断和治疗方面取得了重大进展,但免疫检查点抑制剂(ICIs)在高微卫星不稳定疾病之外的效用仍然有限。鉴于恶性肿瘤对免疫治疗的反应较为持久,提高CRC对ICI治疗的有效率是临床研究的一个活跃领域。越来越多的研究表明,肿瘤衍生的细胞外囊泡(TEV)是肿瘤信号传导的关键调节剂,也是肿瘤微环境的决定因素。临床前模型表明,TEV直接参与抗原呈递,并参与辐射诱导的DNA损伤信号的传导。这些TEV的直接和间接修饰都可以改变CRC免疫原性和ICI治疗效果,使得TEV修饰成为潜在的开发治疗药物的靶标。此外,可以使用几种不同的方式开发修饰后的TEV,包括micro-RNA和小肽分子。最近的研究提供了有力的临床前证据:注射修饰的TEV可诱导ICI的活性,TEV中micro-RNA miR-424的敲低改善了小鼠模型中的CRC免疫原性并增加了抗PD-1活性。临床试验正在进行中,为评估修饰后TEV对癌症治疗的效果,相应的临床试验正在进行中。TEV有望成为CRC的新的治疗靶点。
Keywords:
结直肠癌;免疫疗法;肿瘤衍生的细胞外囊泡;micro-RNA
08
Cell Metab. 20221212
✦
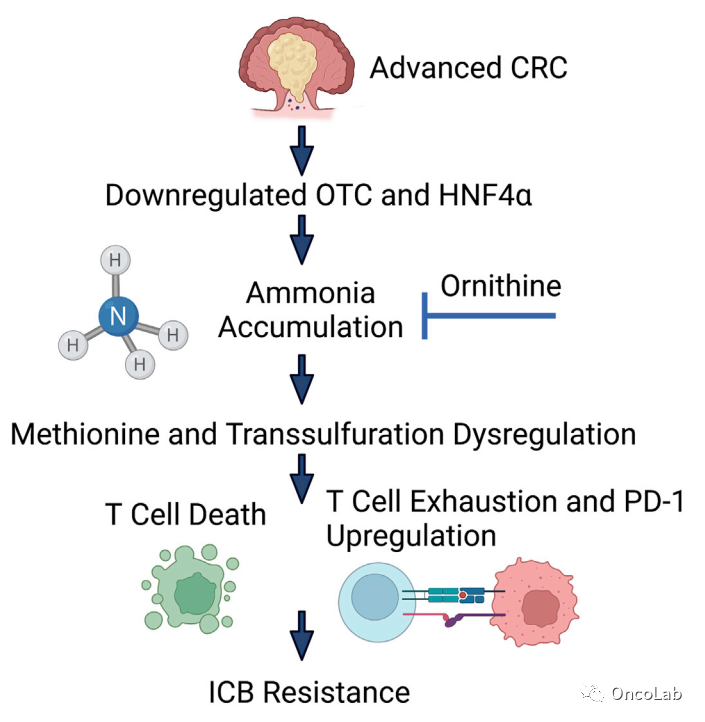
Microenvironmental ammonia enhances T cell exhaustion in colorectal cancer
微环境中的氨加重了结直肠癌中的T细胞耗竭
Cell Metab. 2022 Dec 12;S1550-4131(22)00504-6.
doi: 10.1016/j.cmet.2022.11.013.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36528023/
Abstract
迄今为止仍缺乏晚期结直肠癌(CRC)的有效治疗手段。由于代谢的改变和与微生物群的接触,CRC肿瘤微环境中存在代谢废物的积聚。而代谢废物在肿瘤发展、进展和治疗抵抗中的作用尚不清楚。我们开发了一个结直肠癌(CRC)的自体转移小鼠模型,并使用无偏倚的多组学分析揭示了肿瘤中氨的明显累积。高浓度的氨诱导了T细胞代谢重编程,增加T细胞的衰竭,并减少了T细胞增殖。癌症患者的血清氨增加、氨相关的基因特征与T细胞反应的改变、患者的不良后果以及对免疫检查点阻断治疗的耐受有关。我们证明,通过氨的清除可以重新激活T细胞,减少肿瘤的生长,并延长生存期。此外,减少肿瘤相关的氨增强了抗PD-L1的疗效。这些发现表明,加强氨的解毒可以重新激活T细胞,这很可能成为提高免疫疗法疗效的一种新方法。
Keywords:
氨;肿瘤代谢;免疫治疗;肿瘤微环境
09
Nat Commun. 20221212
✦

PRDM1/BLIMP1 induces cancer immune evasion by modulating the USP22-SPI1-PD-L1 axis in hepatocellular carcinoma cells
PRDM1/BLIMP1在肝癌细胞中通过调节的USP22-SPI1-PD-L1轴诱导肿瘤免疫逃逸
Nat Commun. 2022 Dec 12;13(1):7677.
doi: 10.1038/s41467-022-35469-x.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36509766/
Abstract
程序性死亡受体-1 (PD-1)阻断已经取得了一些疗效,但仅在一小部分肝细胞癌(HCC)患者中有效果。程序性细胞死亡配体1 (PD-L1)与T细胞上的受体PD1结合以抑制抗原特异性的肿瘤免疫反应。然而,PD-L1调控的机制尚未完全阐明。在此,我们发现肿瘤Prdm1的过表达抑制了免疫缺陷小鼠模型的肿瘤细胞生长。此外,肿瘤Prdm1的过表达会上调PD-L1的水平,抑制体内的抗肿瘤免疫力,并中和了Prdm1过表达在免疫功能正常的小鼠模型中的抗肿瘤功效。机制上,PRDM1增强USP22的转录,从而通过去泛素化减少了SPI1蛋白的降解,从而增强了PD-L1的转录。在功能上,在免疫功能正常的小鼠肝癌模型中,prdm1过表达增强了PD-1单抗治疗的效果。总之, 本研究证明了PRDM1-USP22-SPI1轴可调节PD-L1的水平,导致浸润性CD8+T细胞耗竭。此外,PRDM1过表达联合PD-(L)1 mAb治疗为HCC治疗提供了一种治疗策略。
10
Semin Cancer Biol. 20221207
✦
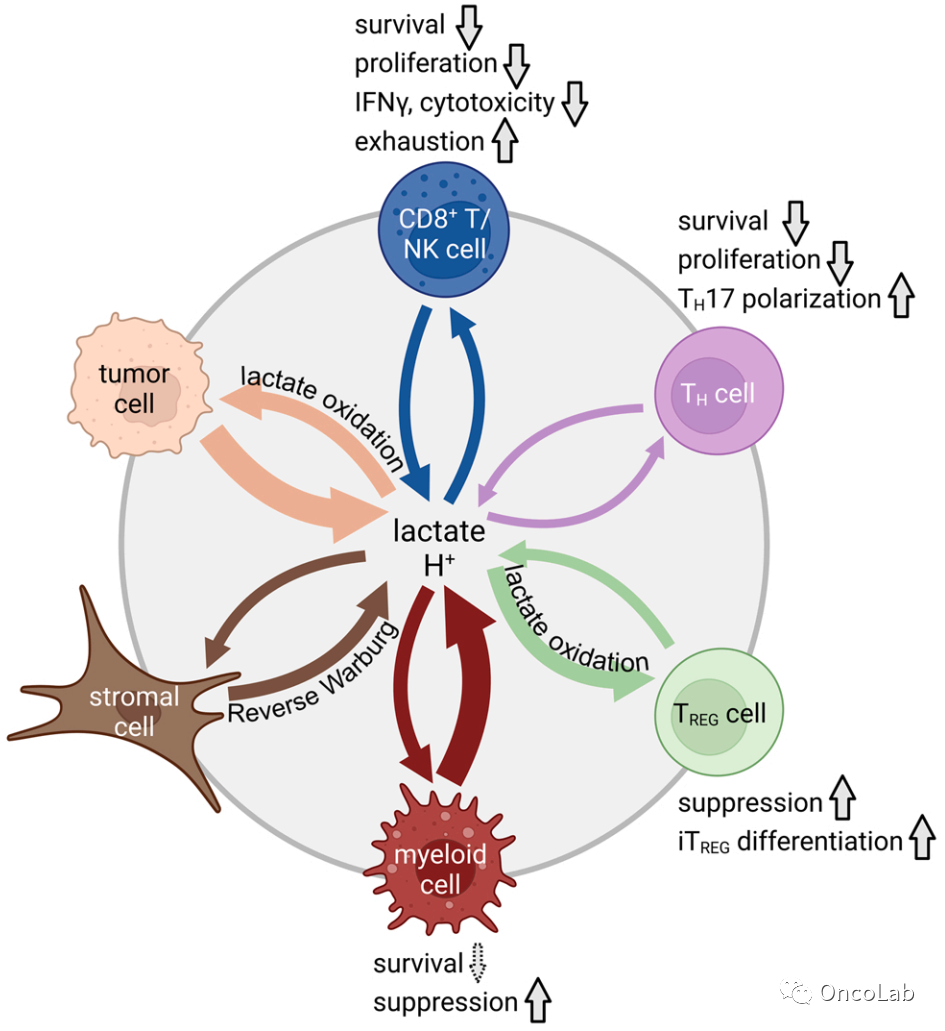
Targeting lactate metabolism for cancer immunotherapy – a matter of precision
靶向乳酸代谢进行癌症免疫治疗 – 精度问题
Semin Cancer Biol. 2022 Dec 7;88:32-45.
doi: 10.1016/j.semcancer.2022.12.001.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36496155/
Abstract
免疫检查点抑制剂和过继性T细胞疗法已经成为抗击癌症的重要辅助工具。这些治疗方法使有望恢复无癌症生活的患者数量极大增加。然而,肿瘤免疫疗法在一些患者和实体肿瘤中迄今仍然无效。在实体瘤中,影响治疗效果的实质性因素是免疫排斥和免疫抑制性的肿瘤微环境。肿瘤中免疫细胞抗肿瘤活性低下的一个主要因素是它们常处于恶劣的代谢环境。缺氧、与肿瘤和基质细胞的营养竞争,以及包括乳酸在内的有害废物的累积,这些因素都对抗肿瘤的免疫细胞产生了巨大的影响。目前许多抗肿瘤治疗策略寄希望于找出肿瘤细胞的代谢缺陷,通过改善它们来减轻代谢引起的免疫抑制。这种尝试虽然从理论上来看很有希望,特别是可以与免疫疗法相结合,但需要仔细研究这些策略对抗肿瘤免疫细胞的影响,因为免疫细胞与肿瘤细胞有一些共同的重要代谢特性。在此,我们综述了那些通过寻求解决肿瘤或免疫细胞中的乳酸堆积现象以改善抗肿瘤免疫反应的治疗方法,从而为那些目前无法治疗的肿瘤患者开辟新的治疗方案。
Keywords:
酸化;过继细胞免疫治疗;免疫检查点抑制;糖酵解;免疫疗法;乳酸;代谢
11
Nat Rev Cancer. 2022120
✦
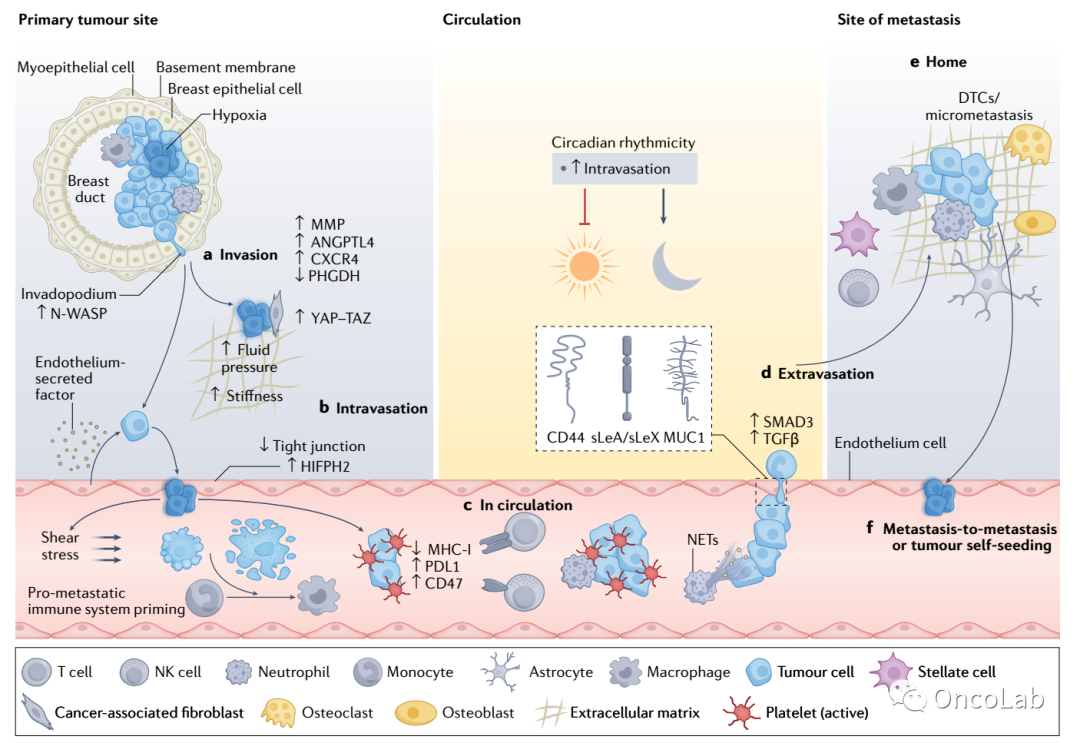
Biology, vulnerabilities and clinical applications of circulating tumour cells
循环肿瘤细胞的生物学特征、易感性和临床应用
Nat Rev Cancer. 2022 Dec 9;1-17.
doi: 10.1038/s41568-022-00536-4.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36494603/
Abstract
近年来,技术进步使得我们能够从患者的血液样本中识别和寻找罕见的循环肿瘤细胞(CTC),这开辟了新的研究领域,并为基于液体活检的临床应用带来了希望。CTC的分析揭示了不同的生物学表型,包括CTC簇的存在以及CTC与免疫或基质细胞之间的相互作用,影响转移形成,并为癌症易感性提供了新的见解。在这里,我们回顾了CTC生物学特征方面取得的进展,并为利用这些发展来设计未来的临床工具以改进癌症的诊断和治疗提供了见解。
12
J Extracell Vesicles. 20221209
✦
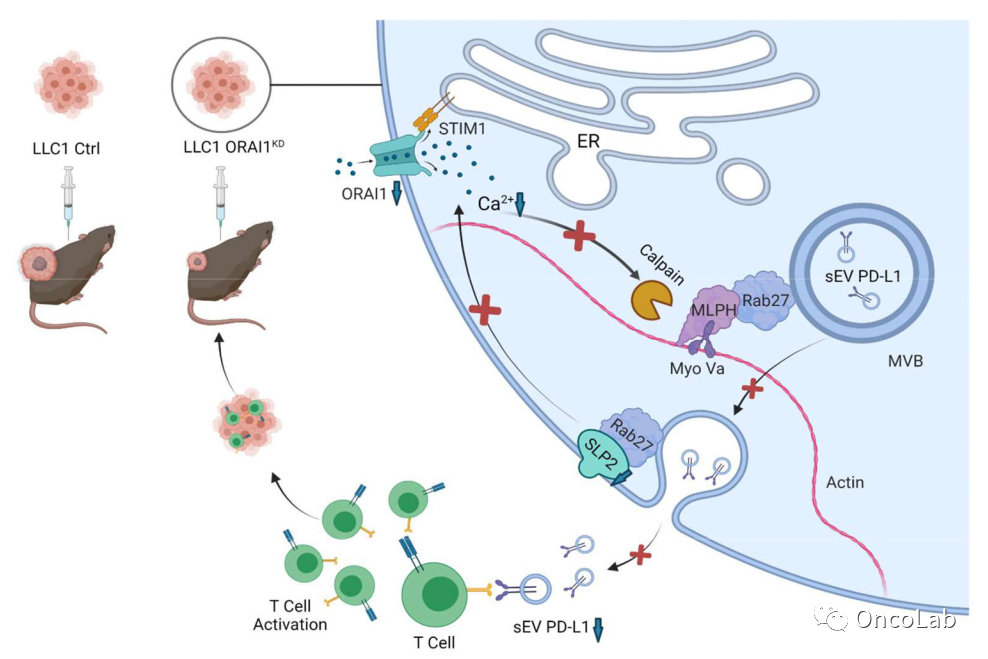
Suppression of PD-L1 release from small extracellular vesicles promotes systemic anti-tumor immunity by targeting ORAI1 calcium channels
抑制PD-L1从外泌体中释放可通过靶向ORAI1钙通道增强全身性抗肿瘤免疫力
J Extracell Vesicles. 2022 Dec;11(12):e12279.
doi: 10.1002/jev2.12279.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36482876/
Abstract
免疫检查点阻断作为癌细胞克服免疫反应的一种策略,最近在癌症研究领域得到了广泛关注。特别是各种癌细胞对PD-L1的表达调控已经成为热门研究方向。PD-L1可通过局部扩散或通过细胞外小泡(sEVs,通常被称为外泌体)的运输到达其作用部位。迄今已对sEVs的形成、与PD-L1的包装和释放到细胞外空间的许多步骤进行了详细的研究。然而,PD-L1可能通过Ca2+信号依赖的方式释放却很少受到关注。这是令人惊讶的,因为细胞内的Ca2+浓度被认为是许多分泌过程的一个重要调节因素。在这里,我们报道了三种Ca2+依赖性蛋白在调节含PD-L1的sEVs释放中的作用,以及对小鼠模型中肿瘤生长情况的影响。我们的研究表明,癌细胞系中的sEVs释放是Ca2+依赖性的,编码Ca2+通道蛋白ORAI1的基因被敲除后,会减少Ca2+信号和sEVs的释放。因此,T细胞反应被重新激活,小鼠模型中肿瘤进展被延缓。此外,对人类癌症组织样本的蛋白质表达模式的分析表明,ORAI1基因明显上调。这种上调被确定为非小细胞肺癌患者生存的一个不利的预后因素。我们表明,敲低ORAI1基因后,Ca2+信号的减少也抑制了嗜黑素和Synaptotagmin样蛋白2的活性,这两种蛋白对于分泌细胞器在癌细胞内的正确定位以及将其运送到外分泌部位非常重要。因此,Ca2+通道ORAI1和分泌途径的Ca2+依赖性蛋白成为了研究和控制PD-L1的免疫检查点阻断的重要目标。
Keywords:
Ca2+; ORAI1; PD-L1; 外泌体; 肺癌
13
Nat Rev Immunol. 20221208
✦
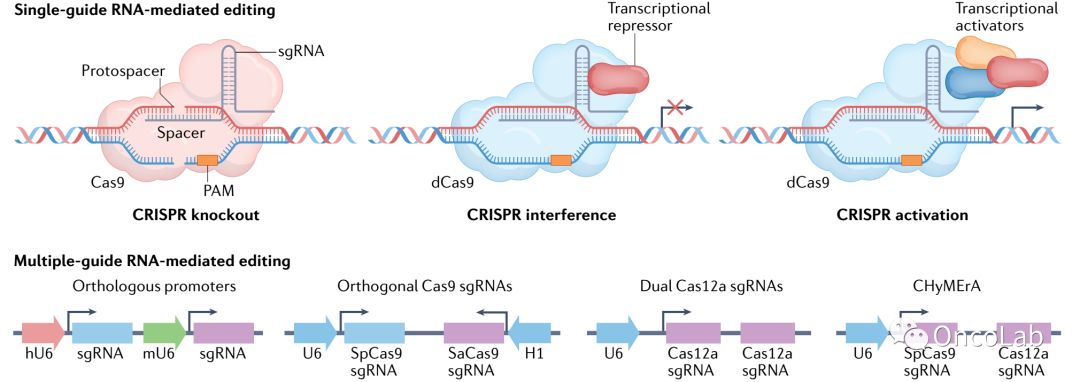
CRISPR screens for functional interrogation of immunity
免疫功能相关的CRISPR筛选
Nat Rev Immunol. 2022 Dec 8.
doi: 10.1038/s41577-022-00802-4.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36481809/
Abstract
基于CRISPR的技术代表了生物医学科学的一个重大突破,因为它们为包括免疫学在内的各个领域提供了一个强大的客观的筛选和功能基因组学平台。CRISPR筛查发现了以前未知的先天性和适应性免疫细胞的免疫调节的细胞内驱动因素,以及介导细胞-细胞相互作用的细胞间调节器。最近的单细胞CRISPR筛选平台将读数扩展到了转录组,并能推断出基因调控网络,这使探究更详细的机制成为可能。CRISPR筛查还允许绘制遗传相互作用图,以确定协同或减轻复杂免疫表型的基因。在这里,我们回顾了CRISPR技术的进展和新兴的适用领域,以推进我们的基础免疫学知识,并为感染、炎症和癌症的免疫疗法确定新的目标。
14
N Engl J Med. 20221208
✦
Tumor-Infiltrating Lymphocyte Therapy or Ipilimumab in Advanced Melanoma
晚期黑色素瘤的肿瘤浸润淋巴细胞治疗或伊匹单抗治疗
N Engl J Med. 2022 Dec 8;387(23):2113-2125.
doi: 10.1056/NEJMoa2210233.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36477031/
Abstract
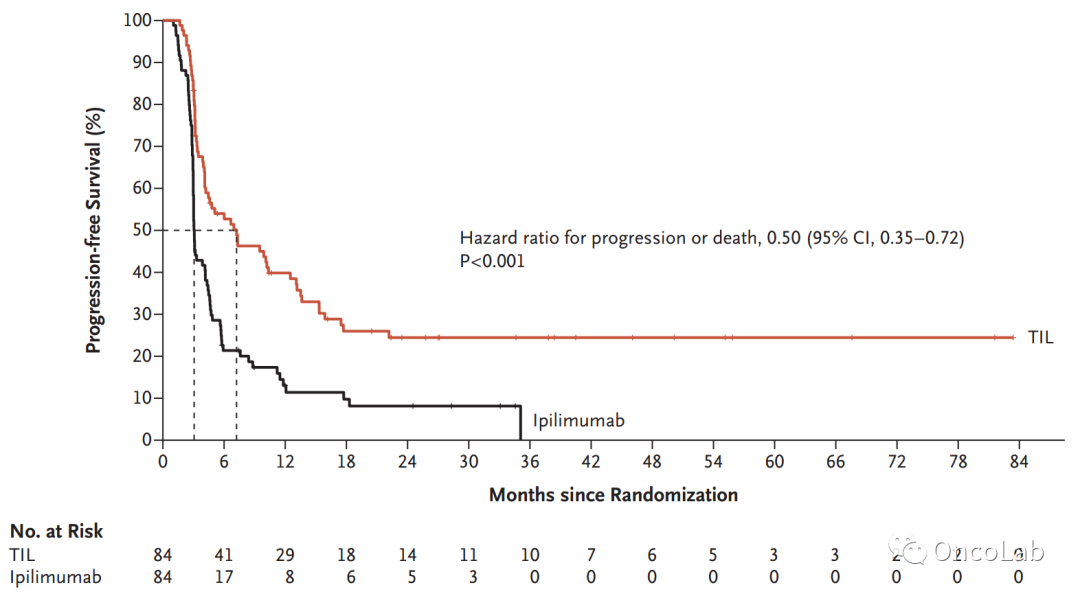
背景:免疫检查点抑制剂和靶向治疗显著改善了晚期黑色素瘤患者的预后,但这些患者中约有一半不会有持久的疗效。采用肿瘤浸润淋巴细胞(TIL)进行过继细胞治疗的1-2期试验结果预示着可能有效,但缺乏3期试验的数据来确定TIL在治疗晚期黑色素瘤中的作用。
方法:在这项3期、多中心、开放的试验中,我们以1:1的比例随机分配不可切除的IIIC或IV期黑色素瘤患者接受TIL或抗细胞毒性T淋巴细胞抗原4疗法(每公斤体重3毫克的伊匹单抗)。在输注至少5×109个TILs之前,先进行非去髓化疗、去淋巴化疗(环磷酰胺加氟达拉滨),然后再进行大剂量白细胞介素-2冲击。判断试验结果的主要观察终点是患者的无进展生存期。
结果:共有168名患者(86%患有对抗PD-1疗法无效)被分配接受TIL(84名患者)或伊匹单抗治疗(84例患者)。在意向治疗人群中,TIL组的中位无进展生存期为7.2个月(95%可信区间[CI],4.2至13.1),伊匹单抗组为3.1个月(95%CI,3.0至4.3)(进展或死亡风险比,0.50;95%CI,0.35至0.72;P<0.001);49%(95%可信区间,38至60)和21%(95%置信区间,13至32)的患者有客观反应。TIL组的中位总生存期为25.8个月(95%可信区间,18.2至未达到),伊普利单抗组为18.9个月(95%CI,13.8至32.6)。所有接受TIL的患者和57%接受伊匹单抗的患者发生了3级或更高的治疗相关不良事件;在TIL组中,这些不良事件主要是化疗相关的骨髓抑制。
结论:在晚期黑色素瘤患者中,接受TIL治疗的患者的无进展生存期明显长于接受伊匹单抗治疗的患者。(由荷兰癌症协会等资助;ClinicalTrials.gov number, NCT02278887。)
15
Nat Commun. 20221207
✦
Multiregional single-cell dissection of tumor and immune cells reveals stable lock-and-key features in liver cancer
肿瘤和免疫细胞的多区域单细胞解析揭示了肝癌的稳定锁钥特征
Nat Commun.2022 Dec 7;13(1):7533.
doi: 10.1038/s41467-022-35291-5.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36476645/
Abstract
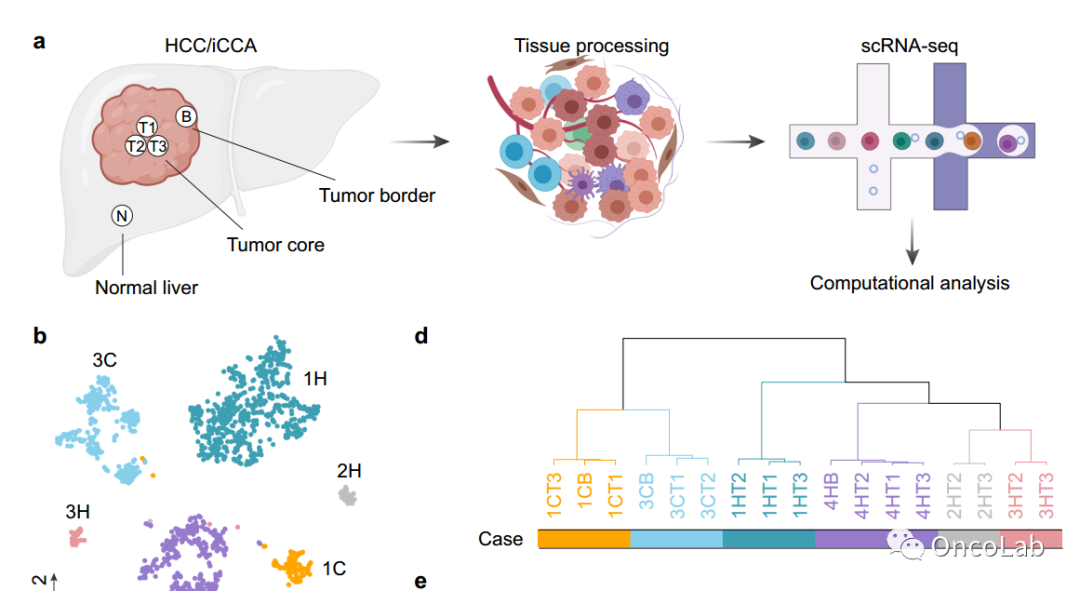
肿瘤内细胞间的异质性可能来自于肿瘤细胞的进化以及它们与肿瘤微环境的持续互动,这共同推动了肿瘤的发生。然而,细胞和分子异质性的出现给定义与肿瘤恶性相关的分子特征带来了挑战。在此,我们对七名肝癌患者(四名肝细胞癌,HCC和三名肝内胆管癌,iCCA)进行了多区域单细胞RNA测序(scRNA-seq)分析。我们确定了恶性细胞的细胞动态特征及其与肿瘤相关免疫细胞的通讯网络,并利用另外25名HCC和12名iCCA患者的scRNA-seq数据进行验证,这些数据作为嵌入恶性生态系统的稳定指纹,代表了肿瘤侵略性的特征。我们进一步验证了在另外542名HCC患者中与特异性转录组相关性最强的配体-受体相互作用对(即肿瘤细胞和巨噬细胞之间的LGALS9-SLC1A5和SPP1-PTGER4)。我们的研究揭示了恶性生态系统的稳定分子网络,这可能为治疗探索开辟了道路。
16
Nature. 20221205
✦
Dendritic cells direct circadian anti-tumour immune responses
树突状细胞调控昼夜节律性抗肿瘤免疫反应
Nature. 2022 Dec 5.
doi: 10.1038/s41586-022-05605-0.
PubMed: https://pubmed.ncbi.nlm.nih.gov/36470303/
Abstract
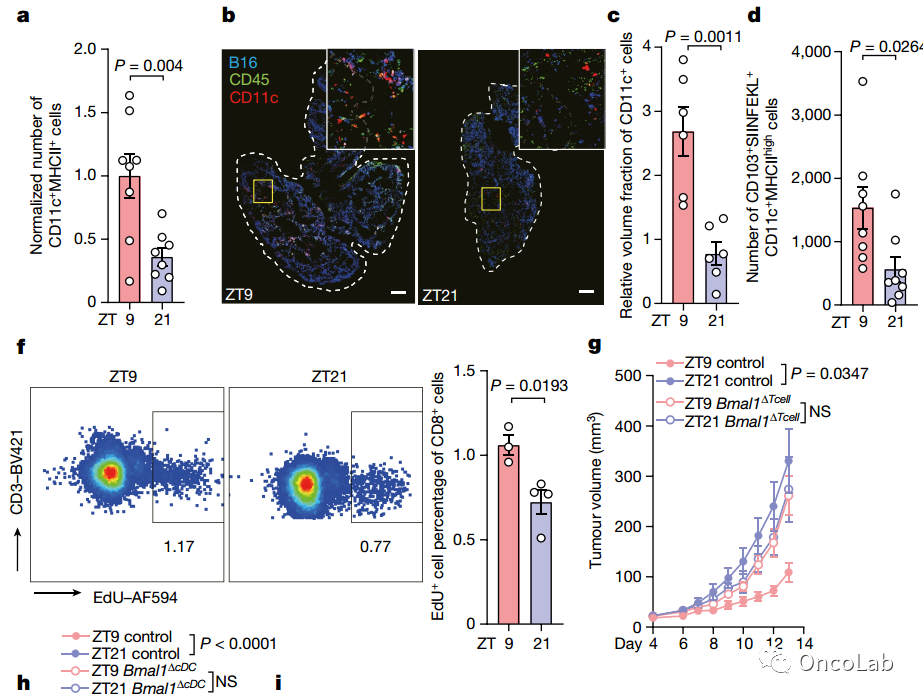
癌症免疫监视的过程是一种抗癌机制,可以保护宿主在免疫监视的情况下不发生癌症。然而,癌症免疫监视的有效性是否会在一天内发生波动尚不清楚。在这里,我们证明了肿瘤移植的最初一天的时间决定了随后小鼠癌症模型的肿瘤大小。我们使用免疫缺陷小鼠以及缺乏谱系特异性昼夜节律功能的小鼠,表明树突状细胞(DCs)和CD8+T细胞发挥昼夜节律抗肿瘤功能,并控制着黑色素瘤的体积。具体而言,我们发现树突状细胞有节律地转运到肿瘤引流淋巴结,控制着肿瘤抗原特异性CD8+T细胞的昼夜节律反应,这种反应依赖于共刺激分子CD80的昼夜节律表达。因此,当癌症免疫治疗刚好与树突状细胞的节律同步时,其治疗效果更好。这一结果得到了小鼠实验的验证,并在人类中显示出类似的效果。这些数据表明,抗肿瘤免疫细胞的昼夜节律不仅对控制肿瘤的大小至关重要,而且利用这一点可能还对治疗具有指导意义。
▉ 强烈推荐
▉ OncoLab实验室网站
本公众号上的往期文章同步发布至对应网站OncoLab实验室。
网站自带检索功能,可以根据关键词进行检索,并且可以根据日期及内容分类进行查看 ,大家可以收藏方便在电脑上查看。
网址是:oncolab.cn
▉ OncoLab学术导航
此外,梳理了一下这几年攒的收藏夹,做了一个导航网页,包含常用网站、文献阅读、试剂订购、基金相关、实用工具、常用数据库等分类内容,并且整合了百度、谷歌、必应三大搜索引擎到检索工具中,欢迎收藏或设置为主页使用~
网址是:dh.oncolab.cn
▉ OncoLab知识星球
OncoLab知识星球也已开通,在学习本公众号内容的过程中如果有什么需要讨论交流的地方可以在星球发表留言,也可以分享一下自己的学习心得体会,其他小伙伴看到了可以积极留言回复,我也会积极参与其中,并时常放一些学习资料在上面,希望大家能够在积极交流互帮互助中共同进步~
该星球用于OncoLab公众号读者交流学习使用,永久免费。

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏