上期内容:
24.2.6 三期临床试验
在对436名不能切除的IIIB-IV期黑色素瘤患者进行的随机III期OPTIM试验中,比较了瘤内注射T-VEC和GM-CSF的疗效。主要终点是持久反应率(DRR),其定义是根据世界卫生组织标准评估的、在开始治疗的前12个月内持续≥6个月的反应。T-VEC组的DRR明显优于GM-CSF组(16.3%比2.1%;p<0.001)。与GM-CSF组相比,T-VEC组的总体反应率(ORR)也更高(26.4% vs 5.7%), T-VEC组的完全缓解率(CR)为10.8%。T-VEC组的总生存期(OS)有改善的趋势,中位OS为23.3个月,而GM-CSF组为18.9个月。探索性分析表明,T-VEC 对早期疾病(IIIB、IIIC 或 IVM1a 期)患者和对治疗不敏感的患者的 DRR 和 OS 的影响更为明显(Fig. 24.4)。
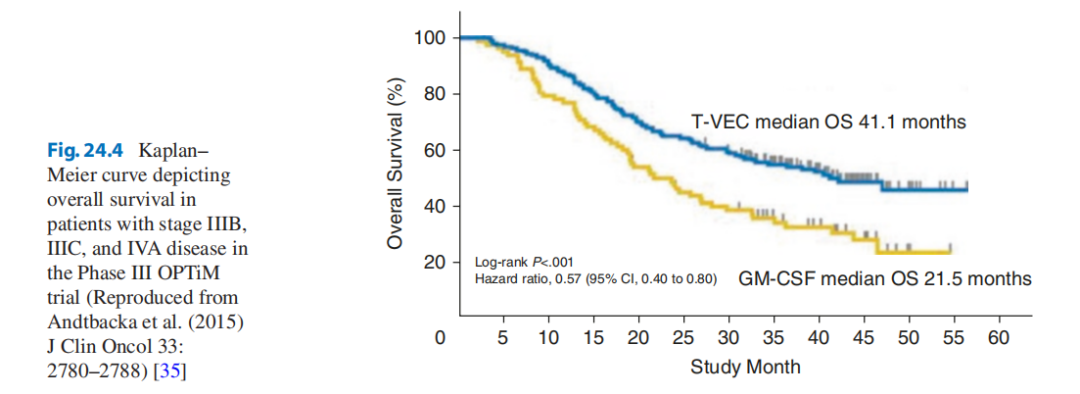
Fig 24.4 Kaplan-Meier曲线描绘了在III期OPTIM试验中患有IIIB、IIIC和IV A期疾病的患者的总存活率
Andtbacka 等人在另一项研究中报告了 OPTiM 研究中使用 T-VEC 的反应模式,指出即使在未注射的非内脏和内脏病变中,反应率也相当可观。注射病灶、未注射的非内脏病灶和内脏病灶的 ORR 分别为 32%、18% 和 14%,相应的 CR 率分别为 15%、6% 和 3%。注射病灶的反应时间较短,约为9.3周,而未注射部位的反应时间为12.3-12.9周。16%接受T-VEC治疗的患者有持久的反应。反应前进展(PPR)不是预测DR持续时间或OS的指标。然而,近 50% 的 T-VEC 持久应答者出现了 PPR,主要是由于出现了新的病变。
24.2.7 不良事件
T-VEC给药通常只会出现轻微不良事件。在Hu等人的I期试验中,注意到的主要副作用是1/2级发热,这在HSV血清阴性的患者中更为明显。其他一些常见的副作用是疲劳、恶心、呕吐和厌食。在第二阶段研究中,85%的晚期黑色素瘤患者经历了最常见的1/2级流感样症状的不良事件。3 名有反应的患者出现了白癜风,这是其他免疫疗法(如 IL-2)的常见症状。在 III 期 OPTiM 研究中,T-VEC在研究人群中总体耐受性良好,报告的常见不良事件(AEs)包括疲劳、寒战和发烧。3/4级不良事件非常罕见,唯一报告的不良反应是蜂窝组织炎,T-VEC 组的受试者中仅有 2% 以上出现这种不良反应。对乙酰氨基酚或吲哚美辛可用于预防或治疗 T-VEC 治疗后引起的疼痛、发热或寒战。甲哌啶可用于控制痉挛。肾上腺功能不全的患者或每天服用泼尼松 10 毫克或更少剂量的肾上腺功能减退症患者可以接受 T-VEC 治疗。如果注射后出现发热或流感样症状等不良反应,可增加皮质类固醇的剂量。蜂窝组织炎是T-VEC给药的已知不良事件。疱疹蜂窝织炎通常是自限性的,最长在48小时内清除。如果出现发热和白细胞增多,必须考虑叠加细菌感染。如果怀疑有脑炎或病毒血症,从血液和脑脊液中检测HSV DNA的PCR检测是可靠的。如果意外接触T-VEC,可考虑使用阿昔洛韦或类似的抗病毒药物。尽管理论上仍然担心病毒可能变异并重新获得致病性,但这尚未在临床上观察到。
根据一些研究,T-VEC不应用于活动性疱疹感染患者或每日服用阿昔洛韦等抗病毒药物的患者。鉴于T-VEC是一种改良的减毒活病毒,不推荐用于免疫状态严重受损的患者,如人类免疫缺陷病毒感染、白血病或淋巴瘤患者或接受高剂量免疫抑制治疗的患者。没有足够的证据来确定T-VEC在孕妇或儿童中的安全性,因此不推荐在这一人群中使用。
24.2.8 经批准的用途
T-VEC是首个经美国联邦食品药品监督管理局批准的溶瘤病毒,用于治疗初次手术后出现皮肤、皮下和淋巴结病变的黑色素瘤患者。这一批准是在2015年10月宣布的。此后不久,即2015年12月,欧洲医疗机构(EMA)批准其在欧洲使用。T-VEC于2016年5月获得澳大利亚治疗商品管理局(TGA)监管部门的批准,用于治疗黑色素瘤。在欧洲和澳大利亚获得批准仅限于患有无法切除的III期或IVa期疾病的黑色素瘤患者,其依据是 OPTiM 研究中发现的这部分人群的卓越反应率 。
BioVex股份有限公司最初以OncoVEXGM CSF的名义开发了T-VEC。在2011年被安进(Amgen)收购后,它现在以Imlygic的名称生产和销售。其使用的两大局限性是(1)不能提高总体存活率和(2)对内脏转移没有影响。目前,还没有明确的生物标志物可以帮助临床医生选择适合T-VEC治疗的患者。T-VEC治疗的患者选择的一些建议标准是可触及疾病的患者;内脏疾病负担较轻,可先接受 T-VEC 治疗以控制局部疾病,然后再接受检查点阻断剂等全身治疗的患者;老年人或患有严重自身免疫性疾病或其他合并症且不适合接受其他形式治疗的患者;以及经过其他治疗方法后病情仍在进展的患者。。
24.2.9 T-VEC的未来
尽管T-VEC对局部疾病控制有显著作用,但全身作用较弱,这为联合治疗提供了理论基础。与其他免疫疗法类似,使用传统的肿瘤反应评估方法,如RECIST和WHO,而传统的肿瘤反应评估方法区分真实进展和假性进展是具有挑战性的。目前,免疫肿瘤学界广泛讨论后得出,在评估免疫疗法的应答时,应特别使用基于免疫的应答标准。
同时,我们需要进一步的研究来确定T-VEC与其他免疫治疗药物的适当结合。此外,从正在进行的研究中,我们将在未来获得更多关于T-VEC治疗顺序的信息。T-VEC的大部分成功案例都是通过局部注射获得的。有必要进一步研究其他给药方法,以探索其对非皮肤恶性肿瘤的治疗效果。
24.3 其他溶瘤病毒
24.3.1 呼肠孤病毒
Pelareorep(REOLYSIN®)是一种活的3型呼肠孤病毒(T3D)株,能够通过激活的Ras途径在肿瘤细胞中复制。蛋白激酶R(PKR)是一种丝氨酸/苏氨酸激酶,参与抵御病毒感染,在Ras转化细胞中不被激活/磷酸化。由于许多肿瘤含有激活的Ras途径,而PKR处于失活或非磷酸化状态,因此呼肠孤病毒溶瘤疗法可用于实体肿瘤的治疗。
在复发性恶性胶质瘤患者瘤内注射呼肠孤病毒的I期研究(REO 003)中,未发现剂量限制性毒性。在11名可评估疾病患者中,10名患者病情进展,1名患者病情稳定。中位生存期为21周,中位进展时间为4.3周。在一项IIb期试验(GOG 186H)中,比较了复发性或持续性卵巢癌、输卵管癌或腹膜癌患者中REOLYSIN®加紫杉醇与单独使用紫杉醇的情况,两组患者的总体生存率没有差异,两组的毒性特征相似。在一项针对NSCLC(鳞状和腺癌组织学)的随机II期试验中,接受多西紫杉醇或培美曲塞联合REOLYSIN®治疗的女性腺癌患者的PFS明显优于单独使用培美曲塞的女性患者。
REOLYSIN®已获得美国食品和药物管理局对恶性胶质瘤、胰腺癌、腹膜癌、卵巢癌和输卵管癌的罕用药指定。
24.3.2 柯萨奇病毒
柯萨奇A21病毒,也被称为CA-V-A-TAK,是一种自然产生的微小核糖核酸病毒,已被证明会导致人类轻度呼吸道疾病。它已被证明,除了前列腺癌、乳腺癌和多发性骨髓瘤等其他类型的肿瘤外,它还优先感染黑色素瘤中常见的ICAM-1表达细胞。它是一种基因上未经修饰的病毒,根据不可切除的III/IV期黑色素瘤进行的II期CALM研究的初步结果,显示有较好的的缓解率。irRC评估的最佳总体缓解率为28%(8个完全缓解,8个部分缓解)。6个月时的irPFS率为39%,持久缓解率为21%。12个月OS率为73%。在注射部位和非注射部位(包括淋巴结、肺和其他远处部位)均观察到活性。另一项CVA21与pembrolizumab联合的I期试验计划用于晚期非小细胞肺癌。
另一种仍在进行临床前测试的柯萨奇病毒已显示出治疗晚期非小细胞肺癌(NSCLC)的希望。柯萨奇病毒B3(CVB3)对NSCLC细胞系显示出选择性倾向,并显示出强效性。这与非小细胞肺癌中柯萨奇和腺病毒受体(CARs)的表达相关。吉非替尼对放射抵抗和EGFR阻断的A549腺癌移植瘤有抗肿瘤作用。
24.3.3 腺病毒
Onyx-015是通过删除腺病毒中的E1B基因来改造的,以选择性地复制和摧毁p53缺失的肿瘤细胞。这在单独或与化疗联合治疗复发性/难治性头颈部鳞状细胞癌方面已显示出疗效。它在中国被批准用于治疗头颈癌,名称为H101。
Delta-24-RGD(DNX-2401)是一种针对肿瘤细胞选择性靶向整合素的腺病毒。在临床前,它已在胶质母细胞瘤模型中显示出巨大的前景。目前,有一项临床试验正在测试DNX-2401和pembrolizumab联合治疗复发性胶质母细胞瘤。一种表达人GM-CSF的嵌合腺病毒(Ad5/3-D24-GMCSF)已经在21例晚期实体瘤患者中进行了I期试验。根据RECIST标准评估,67%的患者获得了客观的临床益处。总体而言,该药物耐受性良好,主要为1/2级不良事件。目前正在进行一项Ad5/3-D24-GMCSF与低剂量持续环磷酰胺联合的I/II期研究。另外还有一项I期试验正在进行,该试验使用表达L523S蛋白的重组DNA和腺病毒治疗早期非小细胞肺癌。
24.3.4 痘苗病毒
Pexastimogene deval iepvec(PexA-V EC或JX-594)是一种基因工程的牛痘病毒惠氏株,表达GM-CSF,但也有胸苷激酶基因的缺失,这有助于该病毒在胸苷激酶水平高的细胞中选择性复制,就像在ras或p53基因改变的肿瘤细胞中看到的那样。在PexA-V EC和索拉非尼联合治疗的晚期肝癌的II期研究中,单独使用PexA-V EC的疾病控制率为62%,启动索拉非尼后的疾病控制率为59%。观察到暂时性3/4级淋巴细胞减少。除此之外,该方案耐受性良好,仅出现了类似流感的症状、恶心和腹痛。
在另一项治疗难治性结直肠癌的Ib期研究中,静脉注射Pexa Vec可达到67%的稳定发病率,最常见的不良反应为1/2级发热和寒战。
PROSTVAC®是一种主要的皮下用药方案,已在症状轻微的去势抵抗前列腺癌患者中进行了研究。痘苗病毒作为主要免疫治疗剂,随后是一系列六种禽痘病毒增强剂,它们都被设计成表达前列腺特异性抗原(PSA)和三种共刺激分子:ICAM-1/CD54、LFA-3/CD58和B7.1/CD80(称为共刺激分子的TRIad或TRICOM)。在II期研究中,参与者被随机分配接受PROSTVAC加GM-CSF或空白载体和盐水注射的对照组。尽管两组在PFS方面没有显著差异,但在3年时,研究药物组的生存期比对照组长8.5个月,风险比为0.56(p=0.0061)。这推动了第三阶段前瞻性试验的开展,该试验已完成登记,预计很快就会有结果。
24.3.5 麻疹病毒
MV-NIS是表达人甲状腺NIS(钠铁转运体)的Edmonston谱系麻疹病毒的工程化形式。NIS是一种在甲状腺组织中表达的膜离子通道,有助于碘捕获,这一特征对于甲状腺扫描(123I或Technitium 99m)或消融(131I)是有利的。这通过合胞体形成诱导选择性癌细胞死亡。在一项复发、进展性卵巢上皮癌或原发性腹膜癌的I期研究中,16名接受MV-NIS治疗的患者平均OS为26.5个月,最常见的不良反应是1/2级腹痛、发热、乏力和中性粒细胞减少。
24.3.6 脊髓灰质炎病毒
PVSRIPO是一种基因工程的脊髓灰质炎病毒Sabin 1型,其内部核糖体进入位点(IRES)被人鼻病毒2型的IRES所取代。这种修饰消除了脊髓灰质炎病毒的神经毒力,并选择性地在表达CD155/Necl5(Necl5)的细胞中复制,这种分子在实体癌中可见。复发性胶质母细胞瘤单次瘤内注射PVSRIPO的一期研究的初步结果显示,1年总生存率为56%,最常见的3级不良事件为高血糖、淋巴细胞减少和偏瘫。2016年,美国FDA授予PVSRIPO突破性疗法认定,以促进该药物在潜在的治疗胶质母细胞瘤方面的加速发展。
24.3.7 逆转录病毒
Vocimagene Amireptorepvec或Toca 511是一种基于鼠白血病病毒的非溶解性逆转录病毒,其基因工程是编码胞嘧啶脱氨酶转基因。与新型口服缓释前药5-氟胞嘧啶(TOCA FC)一起服用,它可以催化该前药转化为5-氟尿嘧啶。17例使用Toca 511和Toca FC治疗的复发性高级别胶质瘤患者表现出良好的耐受性,只有1例患者的3级剂量限制性毒性为血管源性水肿。经治疗后,76%的切除肿瘤中发现病毒DNA。与使用外部洛莫司汀的历史对照7.1个月相比,该方案有13.6个月的良好OS。2015年,Toca 511和Toca FC被美国食品和药物管理局(USFDA)指定为胶质母细胞瘤的罕用药。2017年2月,美国食品和药物管理局为这些治疗胶质母细胞瘤的药物进行了突破性的认定。一项II/III期试验(Toca 5)将Toca 511和Toca FC与接受手术的复发性神经胶质瘤的护理标准进行比较,该试验已完成登记,预计将于2018年上半年取得结果。
24.3.8 细小病毒
细小病毒H-1(H-1PV)是一种啮齿动物单链DNA病毒,对人类无致病性,已知可激活Caspin介导的癌细胞死亡途径。在一项单中心的I/IIa期试验中,肿瘤内或静脉注射H-1PV治疗进展性原发或复发的胶质母细胞瘤患者,没有发现剂量限制性毒性。33%的参与者的PFS为6个月或以上,80%的参与者有6个月以上的OS。该试验已完成登记,最终结果尚待公布。与此同时,一项针对不能手术的转移性胰腺癌患者使用H-1PV的I/II期试验目前正在进行中。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
作者 | Rutika Mehta and Igor Puzanov
初稿翻译 | 李安琪 潘君君
编辑排版 | 郭子
审核修改 | 王坤 胡珊
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏