32.2.6 反应及疗效评价
免疫疗法的作用机制独特,其治疗反应可能表现出一些非典型特征,如解离性反应、延迟反应、超进展和假进展(最初观察到肿瘤体积增大,随后出现缩小)。这些现象主要是因为免疫激活需要时间,免疫效应的临床表现可能有所延迟,且由于免疫细胞被招募至肿瘤床可能暂时增加肿瘤体积,使得肿瘤在有效缩小之前先表现为体积增大。
因此,传统的世界卫生组织(WHO)评价标准和实体瘤反应评价标准1.1版(RECIST v1.1)并不完全适用于评价免疫治疗的反应。为了更准确地评估免疫检查点阻滞剂的临床效果,最近在多数一期临床试验中,已经开发并引入了一种名为免疫相关反应标准(irRC)的新评价体系,该体系被添加到传统的RECIST标准中,以更好地反映免疗疗法的疗效和反应特点。
这些标准更好地考虑了免疫检查点阻滞剂所触发的非典型反应模式,包括可能出现的新非靶向病变、在肿瘤缩小前现有病变的增长,以及长期疾病稳定,有时甚至在停止治疗后还会观察到延迟反应。例如,在Keynote-001研究中,使用抗PD-L1药物派姆单抗治疗的黑色素瘤患者中,7.3%(24/327)表现出非典型反应,其中4.6%(15/327)为早期假进展,2.8%(9/327)为延迟假进展。此外,根据RECIST v1.1,14%(84/592)的患者被诊断为病情进展,而在免疫相关反应标准(irRC)中,这些患者被评估为非进展性疾病。基于这两种标准,非进展性疗效患者的两年总生存率为78%,而根据RECIST v1.1评估的进展性疾病患者的两年总生存率为37%,显示RECIST v1.1可能导致治疗过早中断,从而低估了免疫检查点阻滞剂的潜在益处。
尽管在黑色素瘤患者中非典型反应模式似乎更常见,使用irRC标准在该人群之外的益处尚未得到充分验证,但当前大多数评估免疫疗法的一期试验都建议使用RECIST v1.1标准来进行初步的反应评估,同时在治疗停止时采用irRC标准。这意味着在初步诊断为病情进展后4周内,需要进行第二次影像学评估以确认病情进展,这是在患者退出研究前的必要步骤。即将发布的iRECIST标准旨在整合irRC和RECIST v1.1标准,提供一个更广泛适用的框架,更好地反映这些非典型的响应情况。最后,建议在临床获益的情况下,允许在确认病情进展后继续治疗,这需要研究发起人、患者的书面批准,并基于所有合作研究者的共识。基于这些考虑,非进展率或临床获益率可能是评估一期免疫治疗疗效的潜在相关替代方案(Fig 32.4)。
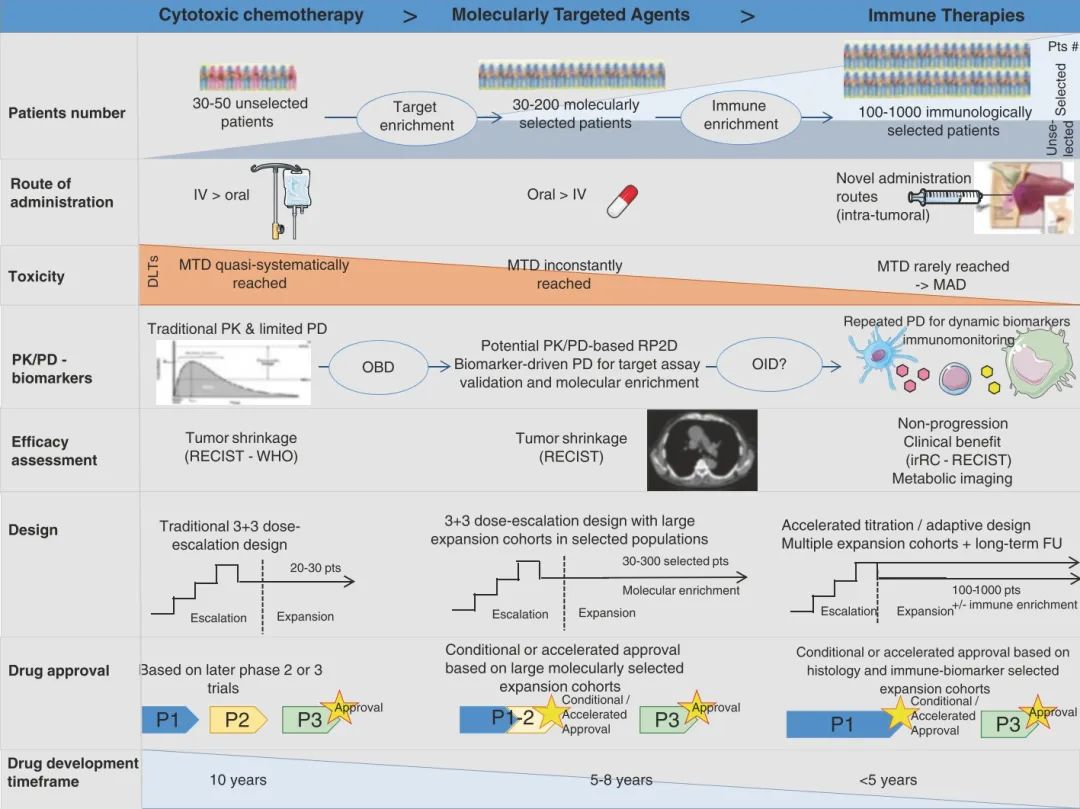
Fig .32.4 展示了自细胞毒性化疗时代以来,一期临床试验在进入免疫肿瘤学时代后的演变(改编自Postel-Vinay等人,经《肿瘤学年鉴》编辑部许可)。自细胞毒性化疗时代以来,一期临床试验已经发生了显著的变化。这些试验已经从小规模研究转变为大规模研究,能够在平行扩展队列中纳入数百名根据分子特征或表型精选的患者。随着最大耐受剂量(MTD)不经常达到,新的给药途径和剂量推荐方法已经被开发。药效学和药代动力学参数在确定后期试验的推荐剂量方面发挥着越来越重要的作用。基于免疫监测的药代动力学(PK)和药效学(PD)数据推导出的免疫最佳剂量,其概念是否可以类似于靶向制剂的最佳生物剂量用于免疫刺激剂,这一点值得进一步探索。同时,早期试验的设计也在平行发展,旨在保持快速的剂量递增阶段,并评估大型选择性队列的疗效。因此,传统的1-2-3期药物开发策略正在被整合的1/3期试验所取代,这些试验绕过了传统的二期研究。所有这些进化显著缩短了药物开发的时间,并且对患者更为有利。
总的来说,现行的评估标准——无论是RECIST、irRC还是iRECIST——都可能不完全足以捕捉免疫疗法中观察到的所有特殊反应模式。因此,一期试验中应系统地考虑和实施替代策略。这些策略包括动态评估(如肿瘤生长速度)、代谢成像技术以及外周免疫监测——后者也可能成为一种反应指标。最终,在免疫治疗的一期试验中是否应该系统地记录总生存期是一个当前的问题。
这一终点在传统上并未在早期试验中注册,因为这些试验的主要目的是评估安全性。初步疗效数据通常作为次要终点,主要通过缓解率或无进展生存期(PFS)进行评估。然而,考虑到免疫疗法可能显著影响生存曲线的尾部,总生存期成为一个相关的终点来评估其长期疗效。
尽管如此,一期试验——即使在当前转变为“一期注册试验”的情况下——仍不是评估总体生存的理想场所,原因包括:(1) 一期试验不包含任何对照组;(2) 患者在试验之后可能接受多种治疗方案,这些方案会引入多种混淆因素;(3) 这会无谓地增加与一期试验相关的工作量,尤其是一期患者经常从外部中心转诊,并在试验结束后返回原医院;以及(4) 随着一期研究越来越早地进入患者的治疗线,这些数据很可能只有在试验结果已经报告和发表后才可用,因此几乎永远不会被及时更新。
32.2.7 试验设计:“第一阶段注册”试验
过去五年中,一期临床试验的设计发生了显著变化(Fig 32.2和Fig 32.4)。传统上,早期试验会招募大约30至60名患者,如ipilimumab的一期研究。然而,最近的免疫疗法一期研究由于其模块化设计和连续修订,已在多个扩展队列中纳入了超过1000名患者。以抗PD-1药物派姆单抗的开发为例,多个Keynote研究中这种范式的转变得以体现。
考虑到最初在黑色素瘤和非小细胞肺癌(NSCLC)患者中进行的首次人体一期研究中观察到的高效活性,特别为这些肿瘤类型增设了专门队列。这些队列不仅旨在确认研究药物的安全性和药代动力学(PK)特征,还要评估其疗效——这是传统二期试验的终点。在对这些队列中数百名患者进行治疗后,临床疗效的确认促成了派姆单抗在2013年9月针对不可切除或转移性黑色素瘤获得加速批准,以及在2015年10月针对转移性PD-L1阳性NSCLC获得批准,分别是在第一位患者使用该药物治疗3年及5年后的结果。值得注意的是,免疫组织化学辅助诊断的22C3 PharmDx试验也同时获得批准,这进一步验证了该药物开发模型的成功。这种“第一阶段注册”试验模式不仅加快了药物的上市进程,也为免疫疗法提供了一条高效快捷的临床验证路径。
这种适应性设计目前在免疫检查点阻滞剂的一期试验中得到了广泛应用,不仅可以扩展到选定的肿瘤类型,还可以测试与共同免疫治疗主干并行的多种组合(Fig 32.2)。这种方法非常值得肯定,因为它允许快速且高效的药物开发。例如,当前的MASTERKEY-265一/三期试验就是评估溶瘤病毒(T-VEC)与帕博利珠单抗注射液组合的相关性,展示了“一期注册试验”模型的进一步演化。
然而,我们必须记住,一期试验的主要目的是确定在后期试验中可以安全使用的最佳剂量。一旦这个剂量被确定,它很少被重新评估。因此,在开展旨在探索疗效的队列时,这一目标不应被过快忽略,因为这可能不符合伦理,让大量患者暴露于次优剂量的实验药物。此外,一旦纳入的患者数量超过了获取令人满意的安全性、药代动力学(PK)和药效学(PD)数据所需的人数,这种扩大的队列应有明确的预先规定的无疗效停止规则。最后,应充分利用这些队列的结果,以最佳方式为药物的注册和后续的大型随机试验做好准备。
32.3 其他免疫疗法及其特异性:精选例子
免疫疗法的类型极其丰富,当前激活的一期试验数量超过1500项,这使得全面描绘每一种疗法的独特性变得极为复杂(Fig 32.5)。因此,在此,我们专注于介绍三种免疫疗法的例子,这些例子不仅展示了与常规针对免疫检查点的抗体治疗不同的独特发展路径,其中两种疗法最近已获批准使用。
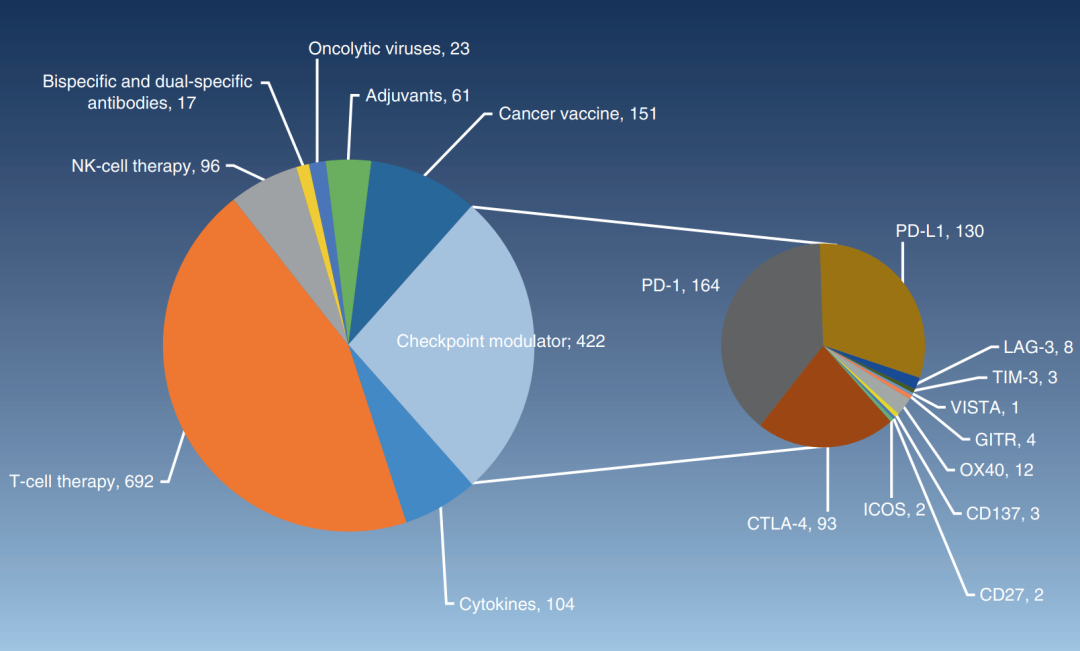
Fig 32.5 免疫肿瘤学(I-O)疗法的一期临床试验(来源:ClinicalTrials.gov,访问日期:2017年1月10日)。此图仅展示了使用关键词“抗癌类”和“癌症”进行搜索的一期试验结果,其中“抗癌类”涵盖了图中详细说明的每个疗法类别。这样的分类有助于更好地理解当前免疫疗法试验的分布和重点研究领域。
32.3.1 博纳吐单抗
Blinatumomab(Blincyto®,由Amgen生产)是一种双特异性抗体,于2014年12月获得美国食品和药物管理局(FDA)的加速批准,用于治疗费城染色体阴性的复发或难治性B细胞前体急性淋巴细胞白血病。
Blinatumomab作为一种双特异性CD19靶向CD3 T细胞接合剂,能够激活表达CD19的靶细胞上的内源性T细胞。这种药物的疗效和安全性与免疫检查点抗体有显著差异,特别是在免疫系统激活方面。首先,与治疗相关的免疫相关不良事件(irAEs)频发且严重,其中11%的患者出现了可能危及生命的细胞因子释放综合征。此外,约有一半的患者表现出特定的中枢神经系统毒性反应,包括定向障碍、抽搐、震颤和语言障碍,这些症状在停止治疗后通常可逆。
因此,该药物的产品标签中包含了关于细胞因子释放综合征和神经毒性的警告,并通过了风险评估与缓解策略(REMS)计划,以向医疗保健提供者通报这些严重风险及潜在的制备和给药错误。在治疗的初期,轻度但频繁的irAEs(如发热、白细胞减少、寒战和C反应蛋白增高)常见,但通常随着治疗的深入会逐渐减轻。此外,研究观察到剂量水平与抗肿瘤活性之间存在明显的相关性。
32.3.2 溶瘤病毒 (T-VEC)
转基因溶瘤病毒疗法T-VEC(Imlygic®,Amgen)于2015年10月获得FDA批准,用于治疗复发性黑色素瘤患者不可切除的皮肤、皮下和淋巴结病变。在最初的一期研究中,使用的OncoVEXGM-CSF的注射剂量逐步增加,对于单剂量治疗后仍为血清阴性的患者,剂量限制在107 PFU/mL。然而,对于接受多次剂量治疗并血清转化为阳性的患者,这一剂量最终可以增加到108 PFU/mL。在多剂量组中,无法确定最大耐受剂量(MTD)。
除了注射部位反应外,T-VEC观察到的最常见不良事件包括疲劳、发热、发冷和流感样症状,这些通常发生在治疗的前三个月,一般为轻度或中度,并在3至4天内消退。这个案例特别强调了在设计原位给药的免疫疗法时,需要考虑严重局部毒性。在没有全身毒性的情况下,这些毒性也可能成为剂量限制因素,并应被纳入剂量限制毒性(DLT)的定义中。
32.3.3 CAR-T细胞疗法
嵌合抗原受体T (CAR-T) 细胞疗法是一种领先的癌症免疫疗法,但它伴随着一些特有的安全挑战。这种疗法可能导致潜在致命的细胞因子释放综合征(CRS),以及与其他特定毒性相关的病症,如巨噬细胞激活综合征和噬血细胞淋巴组织细胞增多症。这些问题促使免疫学专家建议使用非特异性免疫抑制剂(如皮质类固醇)以及针对IL-6受体的抗体tocilizumab(Actemra®,Genentech)。此外,2014年3月,在纽约纪念斯隆-凯特琳癌症中心(MSKCC)进行的一些CAR-T临床试验在发生了几起与输液相关的患者死亡事件后被暂时中止。
尽管有专家假设这些毒性事件是药物发挥最大疗效的必要条件,但这些反应似乎与患者特定的参数(如肿瘤负荷)更为相关,而非药物本身。因此,试验方案进行了调整,减少了肿瘤负担较大的患者的剂量,并排除了那些在严重CRS情况下无法接受积极支持性护理的患者。
CAR-T细胞疗法还面临其他挑战,比如与健康组织上的正常抗原发生交叉反应的脱靶效应,这在一些情况下导致了致命后果。例如,针对黑色素瘤相关抗原3(MAGE-3)的亲和力增强的T细胞受体与横纹肌上的一种非相关肽——肌肽发生交叉反应,导致首两名接受治疗的患者出现致命的心源性休克。
32.4 联合治疗
联合治疗的目标是克服对免疫疗法的原发性或获得性耐药,或延长治疗的反应时间。鉴于这一目标,本节将重点讨论优化免疫肿瘤学(I-O)组合开发的关键概念。免疫系统是一个受到严格调控的平衡系统,需要精确的调整来有效激活,同时避免过度刺激,这可能导致慢性自身免疫性疾病或致命的急性并发症。
在开发联合疗法时,必须考虑到所使用药物的性质。将免疫药物与非免疫药物(包括细胞毒性药物、靶向疗法或抗血管生成药物)结合使用在许多情况下是可行的,尤其是在两种药物的全剂量下,因为它们预期具有有限的重叠毒性或药物代谢动力学(PK)相互作用。然而,必须格外谨慎。例如,尽管某些组合在全剂量下的细胞毒素、小分子或靶向血管生成的抗体是可行的,其他组合则被证明是不可容忍的,如评估vemurafenib与ipilimumab联合治疗黑色素瘤的一期试验因肝毒性而提前终止。
相比之下,在BRAF突变型和野生型黑色素瘤患者中,durvalumab可与曲美替尼和/或达拉法非尼全剂量联合使用。
在两种免疫疗法联合使用时,如ipilimumab与nivolumab的联合,常见的高发严重毒性也是一大挑战。然而,通过特定的给药途径,尤其是原位免疫策略,可以在降低毒性的同时提高疗效。
总体而言,将免疫疗法与其他免疫肿瘤药物结合的可能性是巨大的,目前有数百种组合正在早期试验阶段进行探索(Fig 32.6)。这种组合的多样性不仅体现在可调节的靶标数量上,还体现在剂量的多样性、给药途径和组合时间表上。例如,表观遗传药物可以在无毒剂量下作为免疫调节剂使用,从而为治疗提供新的机会。
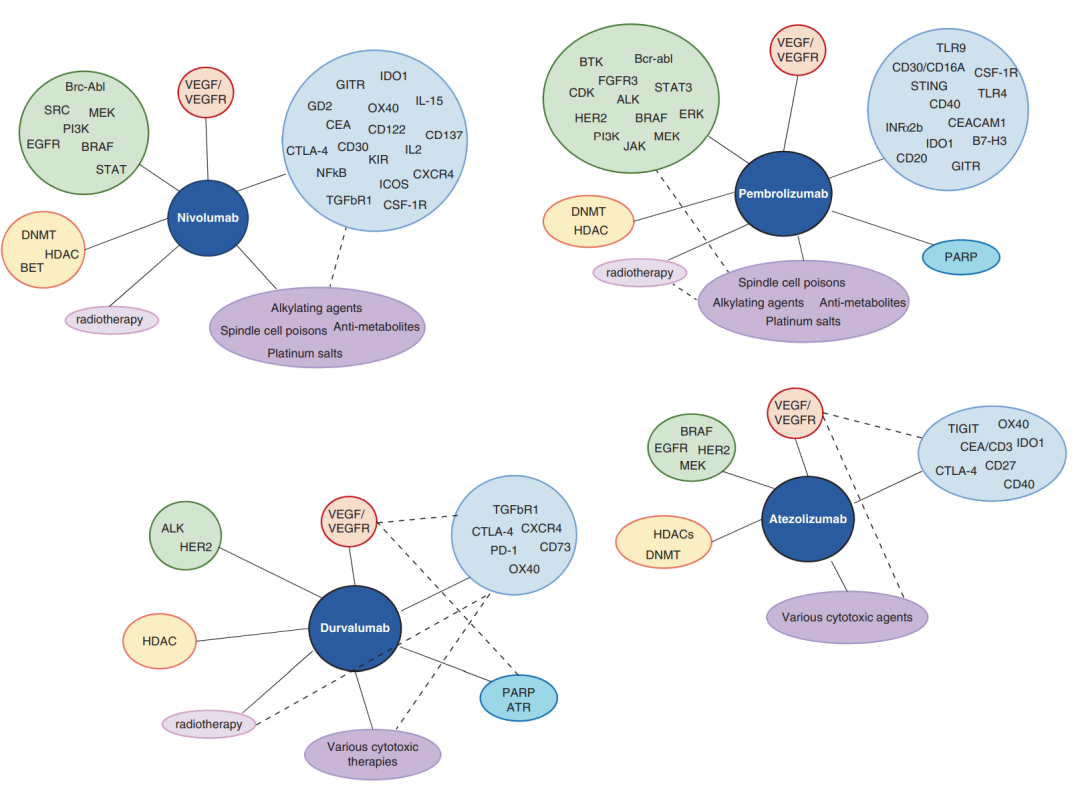
Fig 32.6 展示了当前正在进行的一期试验,这些试验评估联合抗PD-1或抗PD-L1治疗的实例。图中显示了与某些抗PD-1或抗PD-L1药物相关的主要靶点类别,其中绿色代表靶向治疗,橙色代表表观遗传修饰剂,紫色代表常规细胞毒性化疗,蓝色代表DNA修复抑制剂,浅蓝色代表免疫治疗,红色代表抗原性药物。虚线表示三种不同治疗类别与抗PD-1或抗PD-L1治疗主干的关联。本图只描述了一部分正在进行的试验,实际上可能还有更多相关的试验。这些信息来源于2017年1月14日访问的ClinicalTrials.gov,其中仅包括正在招募参与者的一期试验。这张图表提供了一个关于联合免疫治疗策略的全面概览,展示了免疫检查点抑制剂如何与多种不同类型的治疗方法结合,旨在提高疗效和探索新的治疗潜力。
32.5 结论和实际考虑
免疫肿瘤学(I-O)疗法的出现引发了药物开发范式的转变。显而易见,传统的一期试验模式并不完全适合这类新兴疗法。因此,早期试验设计必须适应并不断刷新思路,以便更有效地应对这些疗法所带来的具体挑战。这些挑战不仅包括传统的一期终点——如安全性、毒性评估与管理、剂量建议、药代动力学/药效学(PK/PD)特性及初步活性——还涉及到伴随生物标志物的开发、疗效评估和潜在的药物注册。
早期临床试验必须迅速适应临床和科学的变化,并准备好面对这些实际挑战。鉴于参与中心数量的增加,确保参与药物开发的所有研究者、医疗监管者和科学家之间进行最佳沟通至关重要,以便及时且广泛地共享相关的安全信息。
此外,鉴于I-O特有的安全性问题,一期试验协议中应明确实施有关毒性管理的算法,并尽可能提高报告的质量。这一点尤其重要,因为一些研究人员可能对这些毒性不太熟悉,考虑到I-O疗法在临床上的广泛应用是近期才开始的,并且其应用速度前所未有。最后,任何方案的修改都应基于可靠的临床数据或科学假设。
在免疫肿瘤学的早期药物开发中,我们正处在一个激动人心的时代。高水平的临床、科学和伦理严格性将有助于成功地优化和加速药物的开发过程。
本文由Oncolab微信公众号翻译整理自Oncoimmunology: A Practical Guide for Cancer Immunotherapy,仅用于学习交流使用,如需购买原版书籍可点击阅读原文购买。
— THE END —
来源 | Oncoimmunology: A Practical Guide
for Cancer Immunotherapy
初稿翻译 | 冼金欢
图文排版 | 潘君君
审核修改 | 王坤
(转载请保留此部分内容)

关注本号~

加入读者交流群~
(添加请备注单位姓名)

加入知识星球~
点亮赞与在看
让更多人看到
本篇文章来源于微信公众号: OncoLab
 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏